Clear Sky Science · sv
Hämning av ZBTB7B-medierad ADPGK-transkription av NEDD4 hämmar glykolys och progression av lungadenokarcinom
Varför denna forskning är viktig
Lungadenokarcinom är den vanligaste formen av lungcancer och upptäcks ofta först efter att det tyst har avancerat, när behandlingar fungerar sämre. En anledning till att dessa tumörer är svåra att kontrollera är att cancerceller omkopplar hur de förbränner socker, vilket ger dem extra bränsle för att växa, sprida sig och motstå läkemedel. Denna studie avslöjar en tidigare okänd molekylär ”termostat” som skruvar upp eller ner detta sockerförbrukningssystem i lungadenokarcinomceller, och pekar på nya sätt att svälta tumörer utan att skada resten av kroppen.
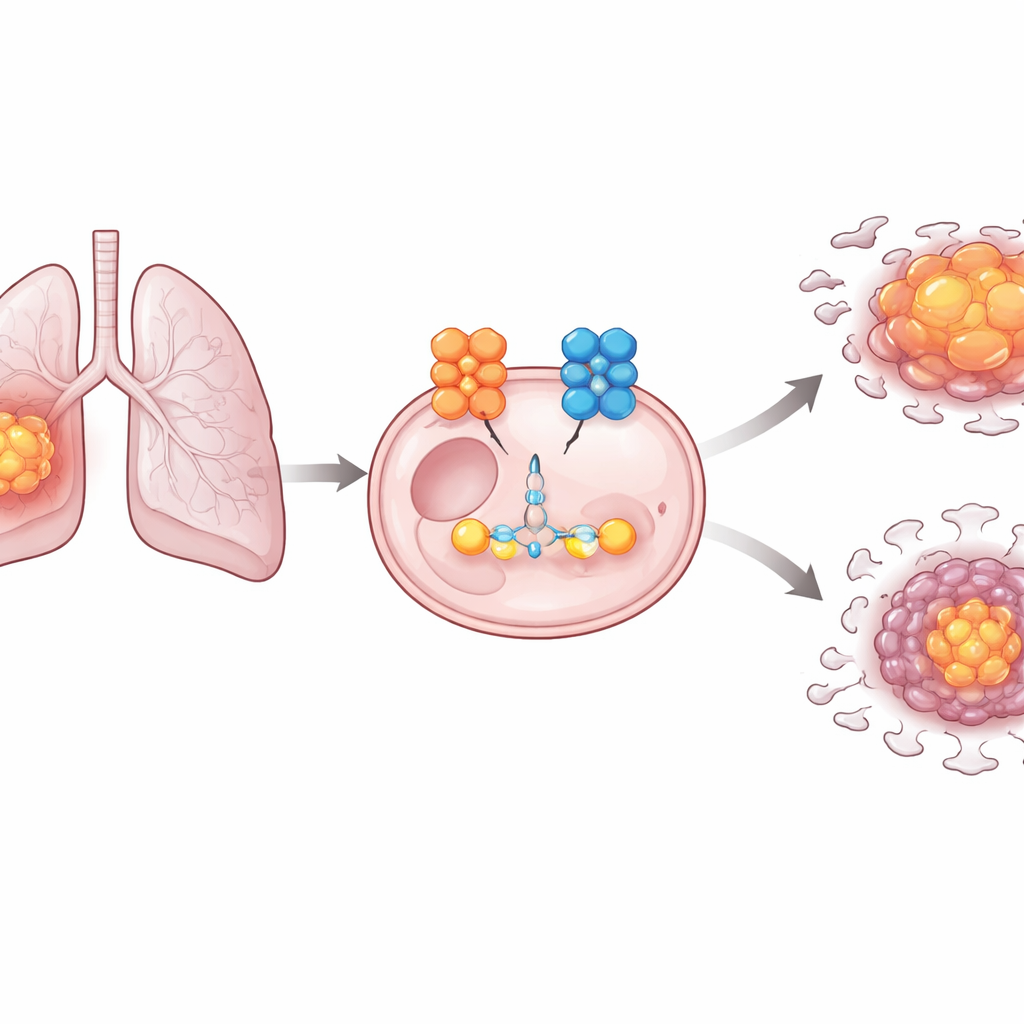
En cancer som lever på socker
Cancerceller är ofta starkt beroende av glykolys, ett snabbt men ineffektivt sätt att omvandla glukos till energi och byggstenar, även när syre finns tillgängligt. Detta metabola skifte hjälper tumörer att växa snabbt och överleva i hårda förhållanden, som dålig blodtillförsel eller behandlingstress. I lungadenokarcinom är många av de enskilda enzymerna i glykolysen välkända, men de brytare som styr när de tillverkas och i vilken grad de används har varit mindre klara. Författarna gav sig därför i kast med att identifiera nyckelregulatorer som kopplar genreglering, proteinstabilitet och förändrad sockeranvändning i denna sjukdom.
En oväntad pådrivare av tumörtillväxt
Forskarna fokuserade på ett protein kallat ZBTB7B, tidigare känt för roller i immunceller och fettmetabolism. Genom att analysera stora patientdatauppsättningar och tumörprover fann de att ZBTB7B-proteinnivåer konsekvent är högre i lungadenokarcinomvävnad och cellinjer än i normala lungceller, och att patienter vars tumörer innehåller mer av detta protein tenderar att få sämre utfall. När ZBTB7B minskades i lungcancerceller odlade i labbet delade cellerna sig långsammare, bildade färre kolonier och migrerade mindre — alla tecken på försvagat tumörbeteende. Samma celler konsumerade också mindre glukos, släppte ut mindre laktat och producerade mindre ATP, vilket visar att ZBTB7B bidrar till cancer cellernas sockerhungriga livsstil.
En speciell sockerenzym i fokus
För att förstå hur ZBTB7B ökar glykolysen kombinerade teamet genombindningsdata med kartor över genaktivitet och riktade in sig på ett relativt ovanligt enzym kallat ADPGK. Till skillnad från typiska hexokinaser, som använder ATP för att starta glykolysen, kan ADPGK använda ADP, vilket tillåter celler att fortsätta bearbeta glukos även när energin är låg. Författarna visade att ZBTB7B binder direkt till en kort region i ADPGK-genens kontrollsekvens och aktiverar den, vilket ökar både dess RNA- och proteinnivåer. När ADPGK tystades försvann till stor del den tillväxt, rörlighet och förhöjda glykolys som extra ZBTB7B orsakat, och när ADPGK återfördes återuppstod dessa tumörvänliga drag. Detta indikerar att ZBTB7B driver lungcancerceller mot ett högglykolytiskt, högväxande tillstånd huvudsakligen via ADPGK.
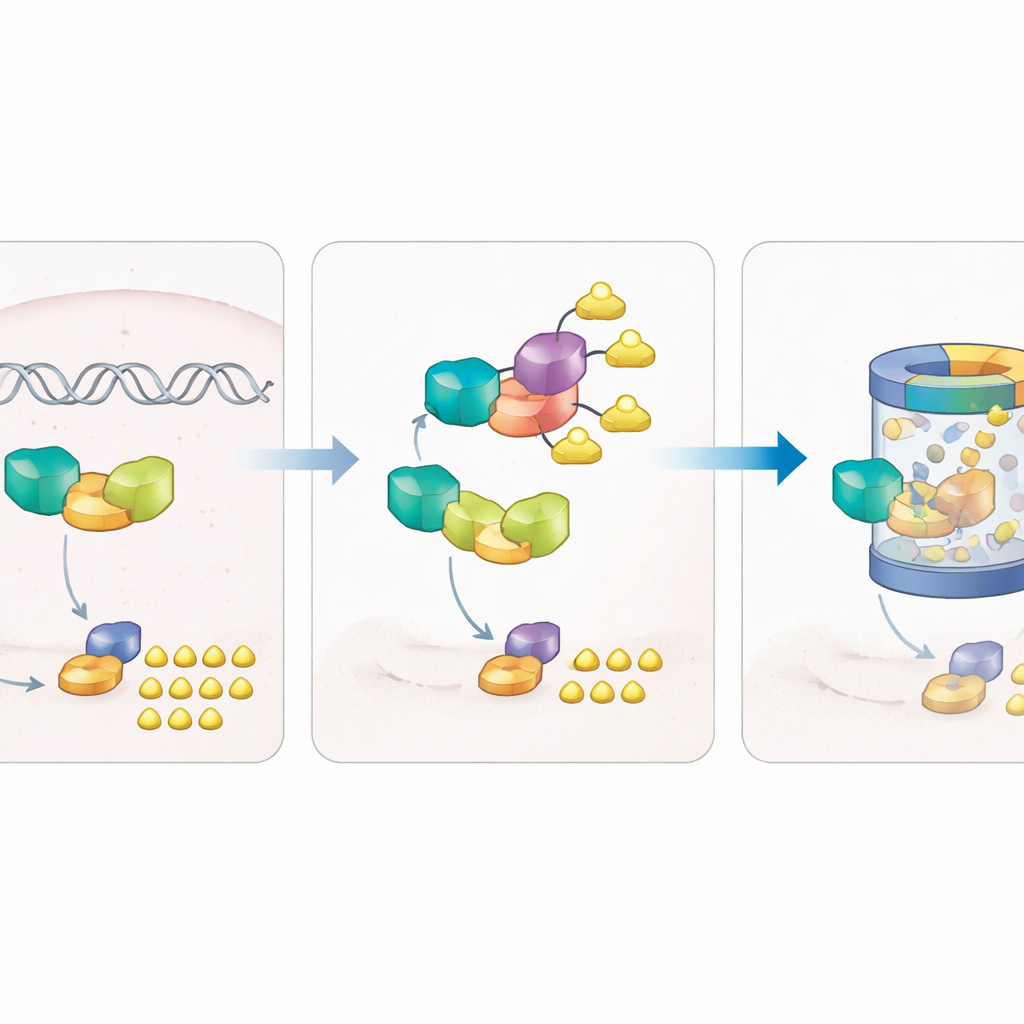
En inbyggd broms som riktar sig mot sockerbrytaren
Pusslet fördjupades när författarna noterade att ZBTB7B-RNA inte var förhöjt i tumörer, trots att dess protein var det. Detta pekade på reglering efter att RNA har skapats. De upptäckte att ett annat protein, E3-ligasen NEDD4, fysiskt binder till ZBTB7B och märker det med ubikvitintaggar vid en specifik plats, vilket markerar det för nedbrytning av cellens proteinåtervinningsmaskineri. När NEDD4 ökade blev ZBTB7B mindre stabilt, ADPGK-nivåerna sjönk och glykolysen avstannade; att minska NEDD4 gav motsatt effekt. En enda förändring på den taggade platsen på ZBTB7B skyddade det från NEDD4 och förhindrade dess nedbrytning. I musmodeller bildade lungcancerceller som konstruerats för att producera mer NEDD4 mindre, mindre glykolytiska tumörer och färre lungmetastaser, men att återintroducera ZBTB7B återvände denna fördel.
Vad detta betyder för framtida behandlingar
Tillsammans avslöjar dessa fynd en ny styrkrets i lungadenokarcinom: ZBTB7B slår på ADPGK för att driva glykolys och tumörprogression, medan NEDD4 fungerar som en naturlig broms genom att flagga ZBTB7B för destruktion. För icke-specialister kan detta ses som en gaspedal (ZBTB7B–ADPGK) och en fot på bromsen (NEDD4) som tillsammans avgör hur hårt tumörmotorn kör på socker. Genom att designa läkemedel som försvagar gaspedalen — genom att blockera ZBTB7B eller ADPGK — eller stärker bromsen genom att förstärka NEDD4:s verkan på ZBTB7B, kan man potentiellt skära av en viktig energikälla för lungadenokarcinomceller. Även om sådana terapier fortfarande befinner sig i ett konceptuellt skede, kartlägger detta arbete konkreta molekylära mål för framtida metabolisminriktade cancerbehandlingar.
Citering: Liu, FP., Huang, T., Yang, HY. et al. Inhibition of ZBTB7B-mediated ADPGK transcription by NEDD4 impedes glycolysis and progression of lung adenocarcinoma. Oncogenesis 15, 14 (2026). https://doi.org/10.1038/s41389-026-00605-5
Nyckelord: lungadenokarcinom, cancermetabolism, glykolys, ubikvitinligas NEDD4, transkriptionsfaktor ZBTB7B