Clear Sky Science · sv
Transkriptomprofilering av samexponerade tumör- och värdceller identifierar hypoxi som en drivkraft bakom skelettmuskels cellers antiproliferativa effekt på cancerceller
Varför vissa vävnader motstår cancerspridning
Cancer blir oftast dödlig när tumörceller lämnar sin ursprungliga plats och slår sig ner i avlägsna organ. Märkligt nog är vissa vävnader, som lungorna, frekventa mål medan andra, till exempel skelettmuskulatur, nästan aldrig koloniseras trots att de utgör en stor del av kroppsvikten. Denna studie ställer en enkel men viktig fråga för patienter och läkare: vad är det med muskeln som gör den till så dålig mark för cancerceller att växa i, och kan förståelsen av detta naturliga försvar ändra hur vi ser på behandling av metastaser?
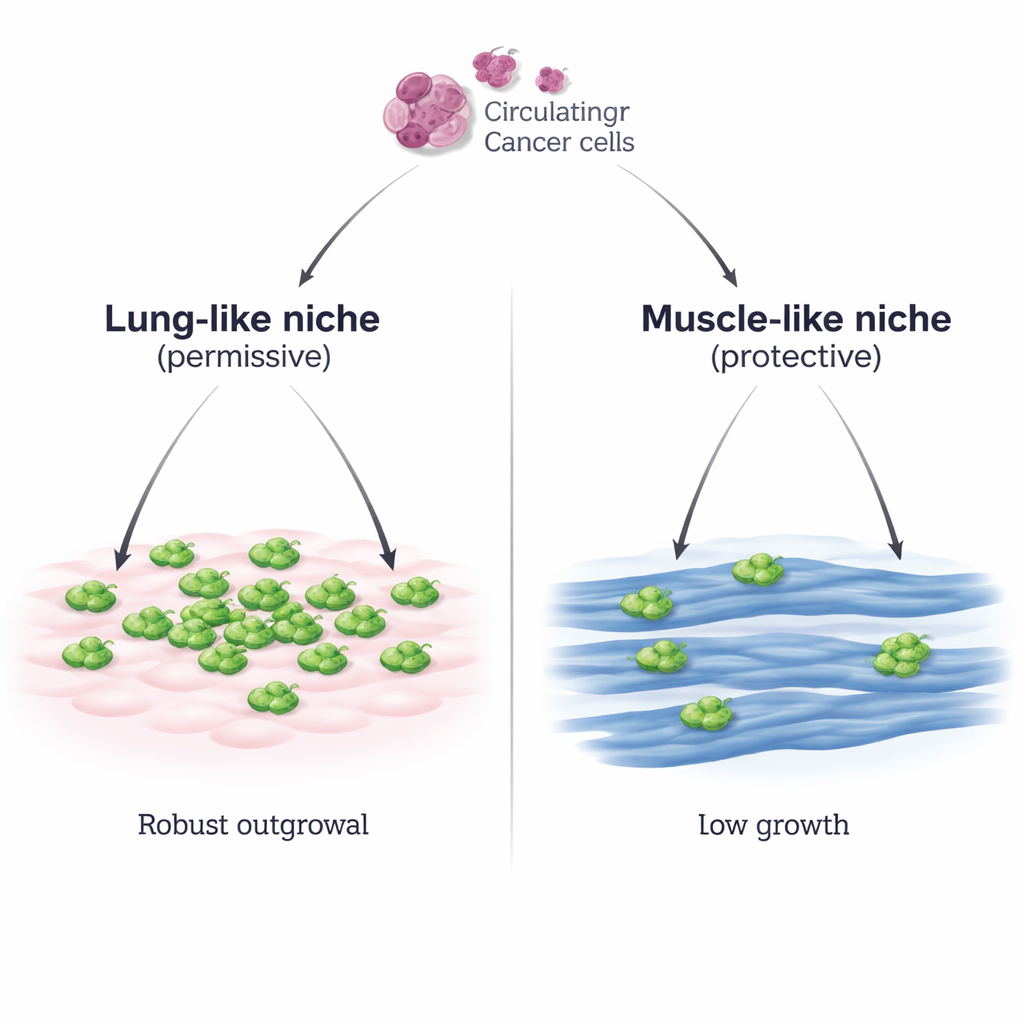
Två kvarter för resande tumörceller
Forskarna byggde ett kontrollerat labsystem som efterliknar två olika miljöer en bröstcancercell kan möta: en lungliknande miljö bestående av lungens bindvävsceller (MLg) och en muskelliknande miljö bestående av mogna skelettmuskelfibrer (C2C12 myotuber). De placerade mössbröstcancerceller ovanpå varje lager och observerade vad som hände. På de lungliknande cellerna fäste cancercellerna väl och började därefter dela sig snabbt och bilda täta kolonier. På muskelcellerna fäste de lika bra, men deras tillväxt förblev gles och långsam, även när startantalet cancerceller ökades kraftigt eller när en andra bröstcancercellinje användes. En separat skelettmuskellinje (Sol8) visade samma förmåga att hålla tillbaka cancerns tillväxt, vilket understryker att detta är en generell egenskap hos muskelceller snarare än en egenhet hos en enskild celltyp.
Hur cancer- och värdceller omprogrammerar sin aktivitet
För att förstå vad som skedde inne i cellerna isolerade teamet cancerceller och värdceller från de blandade kulturerna och sekvenserade deras RNA, en avläsning av vilka gener som är aktiva eller inaktiva. Cancerceller som satt på muskelfibrer genomgick mycket mer omfattande förändringar i genaktiviteten än de som växte på lungceller, vilket tyder på att muskelmiljön tvingar dem anpassa sig kraftigt. I muskelmiljön slog cancercellerna på program kopplade till muskel-liknande egenskaper, energihantering och, överraskande nog, lågt syre (hypoxi)-svar. Samtidigt dämpades de vanliga genprogrammen som driver snabb celluppdelning. Däremot behöll cancercellerna på lungceller en starkt tillväxtfokuserad profil och behövde mycket mindre omprogrammering, i linje med idén att den lungliknande nischen är permissiv och lätt för tumörceller att exploatera.
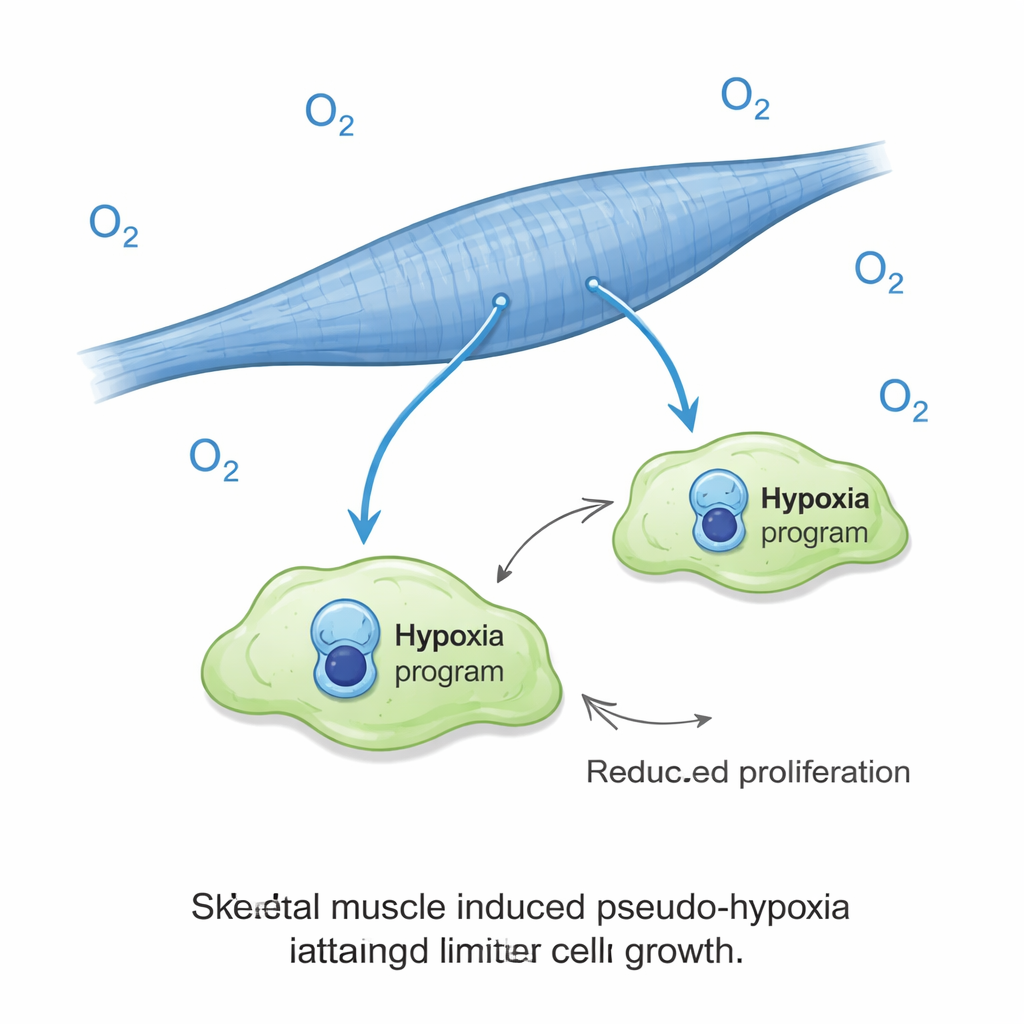
En överraskande roll för låga syresignaler
En av de mest påfallande upptäckterna var att cancerceller på muskelfibrer aktiverade en hypoxi-lik genprofil trots att de odlas under normala syreförhållanden. I de flesta tumörer är hypoxi ett dåligt tecken, ofta kopplat till aggressivt beteende och sämre prognos. Här var det kopplat till motsatsen: dålig tillväxt. Forskarna utsatte sedan kulturerna för verkligt lågt syre och fann att detta nästan utplånade cancercellsexpansionen på muskel, samtidigt som det faktiskt ökade cancerns tillväxt i de lungliknande kulturerna. Med andra ord blev samma signal som vanligtvis hjälper tumörer att frodas ett bromsmedel när cancerceller befann sig i en muskelmiljö. Denna syreffekt verkade inte kunna förklaras av enkla förändringar i laktat, surhetsgrad eller sockerhalt i odlingsmediet.
Mer än bara utsöndrade faktorer
Teamet testade också om enkla lösliga substanser som frigörs av muskelceller kunde förklara deras skyddande effekt. Att tillsätta extra laktat, ändra surhetsgraden, variera glukosnivåer eller odla cancerceller i medium som tidigare använts för muskelceller återgav inte den starka hämning som sågs i direkta kontakt-kokulturer. Detta tyder på att nära fysisk kontakt, eller mycket kortdistanssignaler vid cellytan, är avgörande för hur muskelceller tvingar cancerceller in i ett lågtillväxt-, möjligen dvalaliknande, tillstånd. Intressant nog förblev muskelcellerna själva relativt stabila i sin genaktivitet i mötet med cancer, medan lungceller lättare omprogrammerades, vilket framhäver muskeln som en robust "metastasresistent" vävnad.
Vad detta betyder för patienter och terapier
Sammantaget visar studien att skelettmuskulatur fungerar som en fientlig habitat som tvingar cancerceller in i ett hypoxi-likt, lågt proliferationsläge, även när syre finns i överflöd. Detta hjälper till att förklara varför muskeln är en så ovanlig plats för metastaser. Det ger också en varningsklocka för läkemedelsutveckling: terapier avsedda att blockera hypoxisignalisering i hela kroppen skulle oavsiktligt kunna försvaga detta naturliga muskelskydd, vilket gör det lättare för cancerceller att växa där de normalt inte gör det. Att förstå och bevara, eller till och med efterlikna, muskelskyddande egenskaper kan öppna nya vägar för att förebygga eller kontrollera metastatisk sjukdom.
Citering: Aunan, A., Claeyssen, C., Abdelhalim, M. et al. Transcriptomic profiling of co-cultured cancer-host cells identifies hypoxia as a driver of the skeletal muscle cell’s anti-proliferative effect on cancer cells. Oncogenesis 15, 7 (2026). https://doi.org/10.1038/s41389-026-00601-9
Nyckelord: cancermetastas, skelettmuskulatur, hypoxi, tumörmikromiljö, cancerdormans