Clear Sky Science · sv
Omstrukturering av cytoskelettet framkallad av en ny K6-K14-keratinfussion främjar cancerstamceller och cellulär plasticitet via cGAS-STING-selektion
Hur formskiftande cancerceller överlistar sin omgivning
Cancerceller växer inte bara okontrollerat; de lär sig också att böja och vrida sitt inre "skelett" för att överleva, gömma sig och sprida sig. Denna studie visar hur en specifik strukturell felaktighet i celler från huvud- och halscancer kan skada deras kärnor, utlösa ett inneboende larm för fara, pressa dem in i ett dvalt tillstånd och slutligen hjälpa dem att återkomma som mer aggressiva, invasiva och stamcellsliknande celler. Att förstå denna mekaniska väg till cancerutveckling kan öppna nya möjligheter att blockera återfall och metastaser.
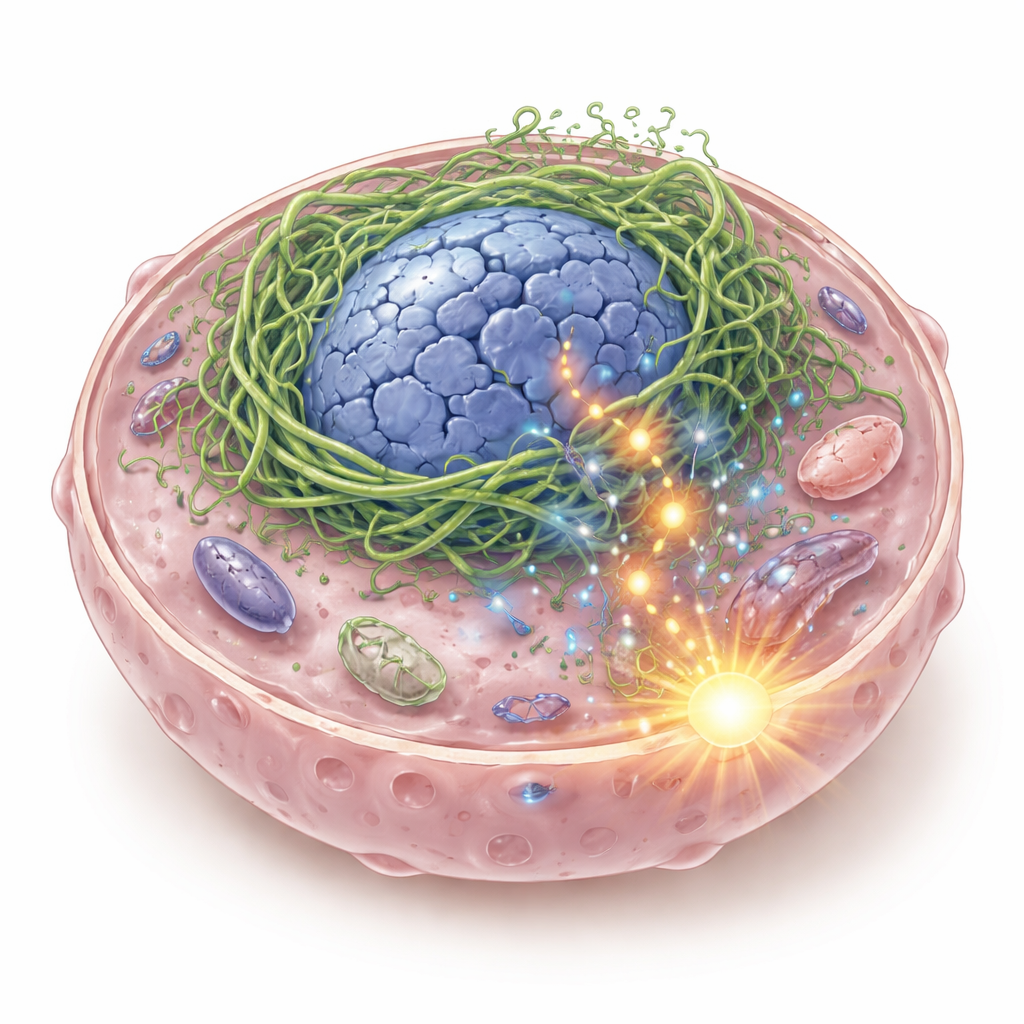
En trasig inre stomme med farliga följder
Inuti varje cell finns en flexibel stomme av proteintrådar som håller cellen och dess kärna i form och hjälper den att uppfatta fysiska krafter. Författarna fokuserade på keratiner, en familj stomproteiner vanliga i epitelvävnader, inklusive de som bekläder mun och svalg. I vissa skivepitelcancerformer i huvud och hals upptäckte de en hybridkeratin kallad K6-K14/V5, bildad när två keratingener smälter samman. När detta fusionsprotein aktiveras i cancerceller bildar det inte ett jämnt stödjande nätverk. Istället klumpar det ihop sig tätt runt kärnan, vrider den till ihåliga, missbildade strukturer och orsakar DNA-brott. DNA-bitar läcker ut i cellvätskan där de upptäcks av ett immunsensoriskt system kallat cGAS–STING, som normalt larmar när viralt DNA är närvarande.
Från dödspress till dold överlevnad
Den omedelbara effekten av denna kärnskada är skadlig för cancercellerna: deras tillväxt saktar ner och många dör. En andel klarar sig dock. Dessa överlevare påverkas starkt av sin fysiska omgivning. På vanliga platta plastskålar försvinner de gradvis, men när de odlas i ett mjukt kollagen-gel — närmare den verkliga vävnadens textur — kvarstår de och återuppträder som en ny population, kallad 3D-V5-celler. Genuttrycksanalyser visar att dessa celler svarar på det pågående DNA-larmet genom att slå på autophagi, ett självrensningsprogram som återvinner skadade delar, särskilt defekta mitokondrier. Detta svar hjälper dem att gå in i ett dvalt, lågaktivt tillstånd som låter dem uthärda stress istället för att elimineras.
Dvala celler kopplar om och förbereder sig för rörelse
Medan de är i dvala skriver dessa överlevande celler tyst om sina interna program. De ändrar blandningen av keratinproteiner och antar ett "partiellt" epitelialt–mesenkymalt övergångstillstånd (pEMT) — en mellantillvaro som behåller vissa epiteliala drag men får ökad flexibilitet och rörlighet. De blir mycket bättre på att bilda sfärer och anlägga nya cellkluster, ett kännetecken för cancerstamcellsegenskaper. Med tiden återfår deras mekaniska egenskaper: de förhärdar sina kärnor igen, bygger upp starka aktinfilament och utvecklar långa utskott som sonderar och greppar den omgivande matrisen. De ökar också produktionen av enzymer kallade matrixmetalloproteinaser (MMP), som bryter ned den extracellulära matrisen och öppnar vägar för invasion.
Kommunicerar med närliggande celler för att bygga en stödjande nisch
Dessa omprogrammerade cancerceller agerar inte ensamma. Forskarna observerade att 3D-V5-celler frisätter stora mängder små paket kallade extracellulära vesiklar till sin omgivning. När dessa vesiklar omger närliggande orala fibroblaster — bindvävsceller — ändrar fibroblasterna sitt eget genuttryck och blir mer lika cancerassocierade fibroblaster som stödjer tumörtillväxt. Många av signalerna som utbyts kretsar kring FGF–FGFR-axeln, en familj tillväxtfaktorer och deras receptorer som är kända för att driva cellexpansion, plasticitet och resistens. Både i cellodlingar och i musmodeller minskade blockering av FGFR-aktivitet denna tillväxtfördel. I djur var tumörer som bildades från 3D-V5-celler dåligt differentierade, mer invasiva, rika på stamcellsmarkörer och mer benägna att sprida sig bortom injektionsstället.
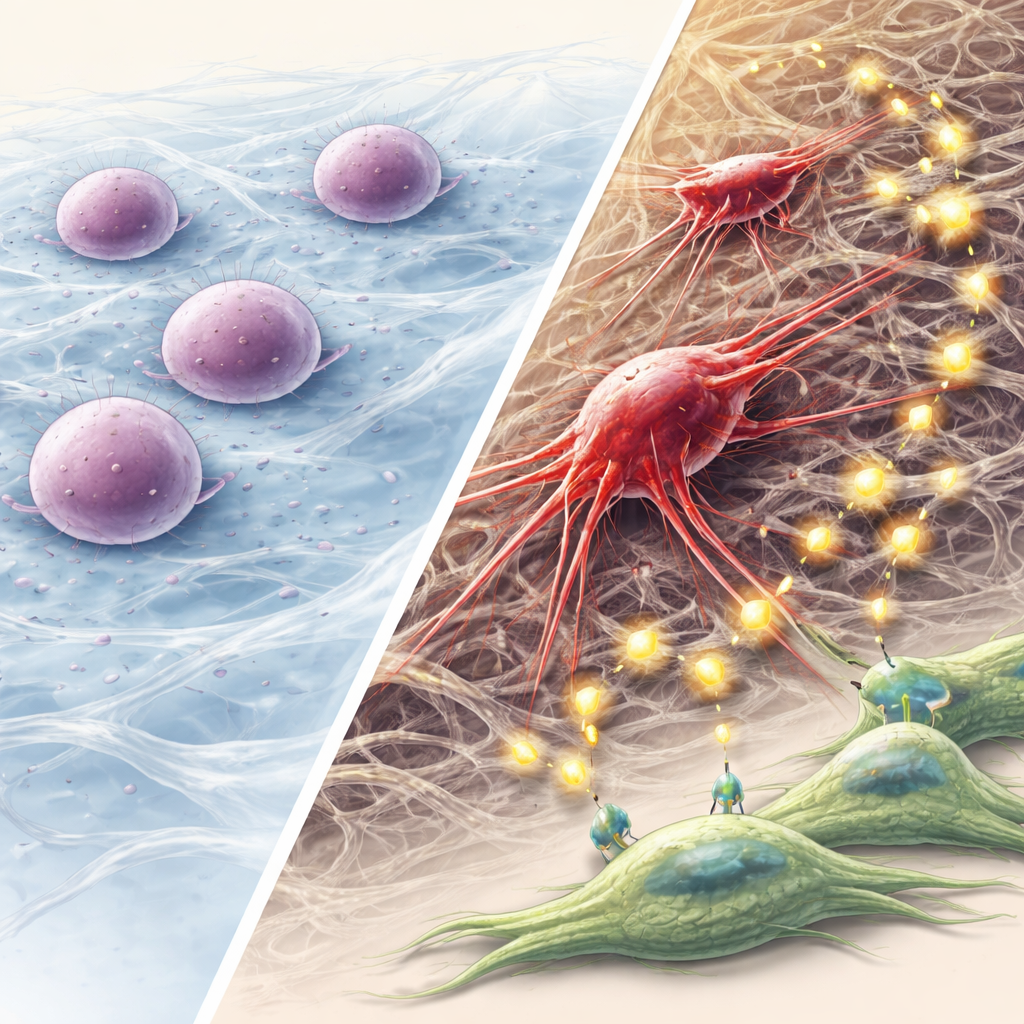
Varför denna mekaniska väg till aggressiv cancer är viktig
Detta arbete föreslår en stegvis modell: en keratinfusion stör cellens inre stomme, krossar kärnan och utlöser ett DNA-skadelarm; autophagi tillåter sedan några celler att gå i dvala istället för att dö; över tid omorganiserar dessa överlevare sitt skelett, förvärvar stamcellslika och invasiva egenskaper och omformar sin omgivning genom vesiklar och FGF-signalering. För icke-specialister är huvudbudskapet att fysiska krafter och strukturella proteiner inuti celler kan vara lika viktiga som gener och kemikalier i att driva cancerutveckling. Att rikta in sig på denna mekaniska stress–autophagi–FGF-väg, särskilt i huvud- och halscancer med keratinfusioner, kan erbjuda nya strategier för att förhindra att dvala tumörceller vaknar upp och sprider sig.
Citering: Chen, IH., Ravichandran, S., Lai, MT. et al. Cytoskeleton reorganization induced by a novel K6-K14 keratin fusion promotes cancer stemness and cellular plasticity via cGAS-STING selection. Oncogenesis 15, 5 (2026). https://doi.org/10.1038/s41389-026-00598-1
Nyckelord: cancerstamceller, cellens cytoskelett, tumördvala, huvud- och halscancer, mekanotransduktion