Clear Sky Science · sv
Histondemethylasetens PHF2 roll som tumörsuppressor i hepatocellulärt carcinom genom reglering av SRXN1
Varför denna studie om levercancer är viktig
Levercancer är en av de dödligaste cancerformerna globalt, och dagens läkemedel förlänger för många patienter livet endast måttligt. Denna studie ställer en annan fråga: i stället för att rikta in sig på de vanliga genfelen som driver cancer, kan vi utnyttja sättet DNA paketeras och kemiskt märks i leverceller för att hitta nya, mer precisa behandlingsalternativ? Forskarna fokuserar på ett lite känt protein kallat PHF2 och kartlägger hur det kan bidra till att hindra leverceller från att bli cancerösa.
Söker svagheter i cancers kontrollsystem
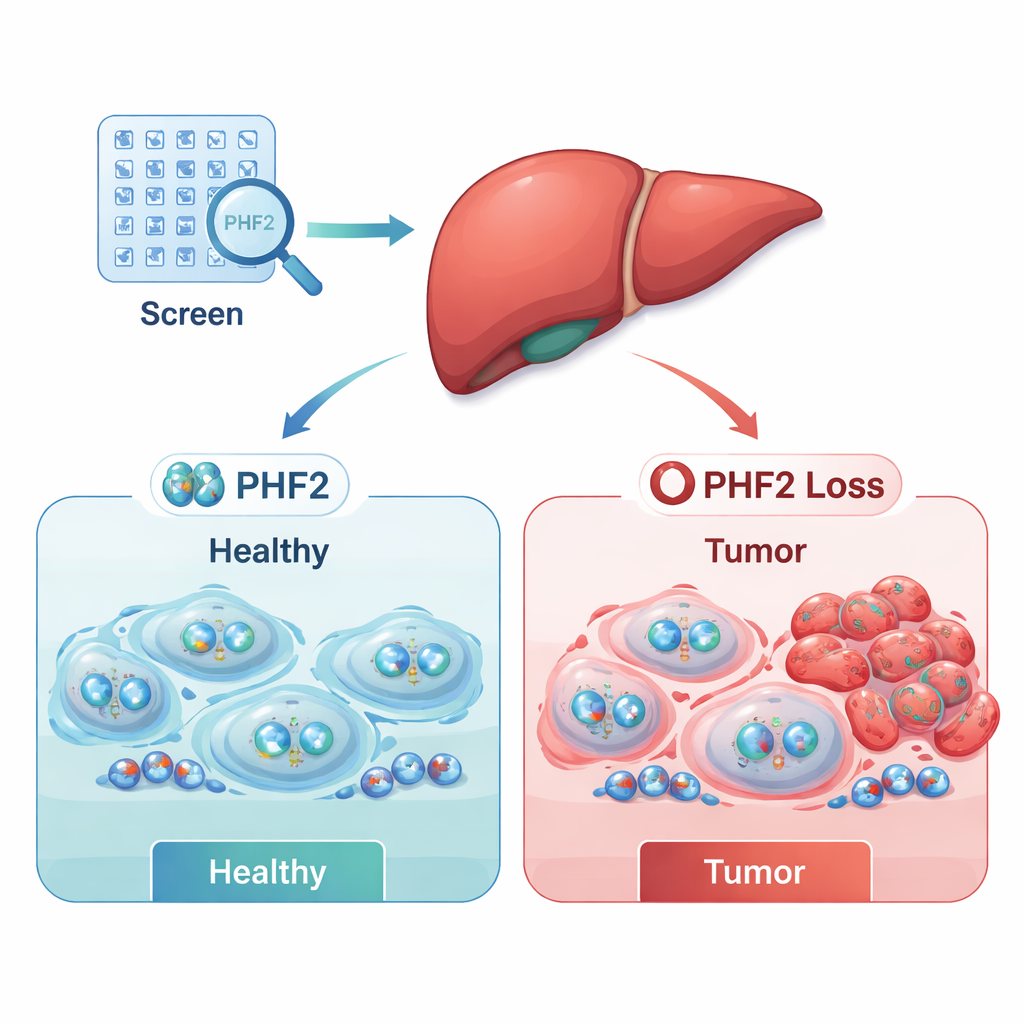
Cancer drivs inte bara av skadade gener; den underhålls också av brister i de epigenetiska kontrollmekanismerna—de kemiska taggar och proteinkomplex som bestämmer vilka gener som slås på eller av. I hepatocellulärt carcinom, den vanligaste formen av levercancer, är många sådana regulatorer rubbade. Forskargruppen testade systematiskt 497 epigenetiska regulatorer i sex levercancercellinjer, genom att använda RNA-verktyg för att tillfälligt minska varje regulator en efter en och sedan mäta hur väl cancercellerna överlevde. Denna stora screening var utformad för att avslöja vilka regulatorer cancer är beroende av för att växa, och vilka som normalt fungerar som bromsar för tumörbildning.
Upptäcker nya cancerhjälpare och skyddsproteiner
Screeningen avslöjade två breda grupper: potentiella cancer"acceleratorer" (onkogener) vars borttagning skadade cancercellernas överlevnad, och potentiella "bromsar" (tumörsuppressorer) vars förlust gjorde att cancerceller växte bättre. Genom att kombinera sina laboratoriedata med stora offentliga patientdatamängder begränsade forskarna listan till ett fåtal kliniskt relevanta kandidater. Två regulatorer, SUPT7L och SMARCC1, tenderade att vara mer aktiva i tumörer och kopplades till sämre överlevnad. I kontrast var en regulator—PHF2—ofta mindre aktiv i levertumörer, och patienter vars tumörer bibehöll högre nivåer av PHF2 levde i regel längre. Dessa mönster antydde att PHF2 kan fungera som en tumörsuppressor vid mänsklig levercancer.
Hur förlust av PHF2 förändrar levercancerceller
För att pröva PHF2 närmare konstruerade teamet levercancerceller som stabilt producerade mindre av detta protein och följde deras beteende över tid. Celler med reducerad PHF2 växte snabbare och visade högre nivåer av Ki-67, en markör för aktiv celldelning, vilket indikerar att PHF2 normalt hjälper till att begränsa proliferation. Effekterna var mest uttalade i redan aggressiva levercancercellinjer, vilket antyder att enbart förlust av PHF2 kanske inte startar cancer självständigt, men kan påskynda tillväxten av maligna celler när tumörer väl har bildats.
En överraskande koppling till cellens stressförsvar
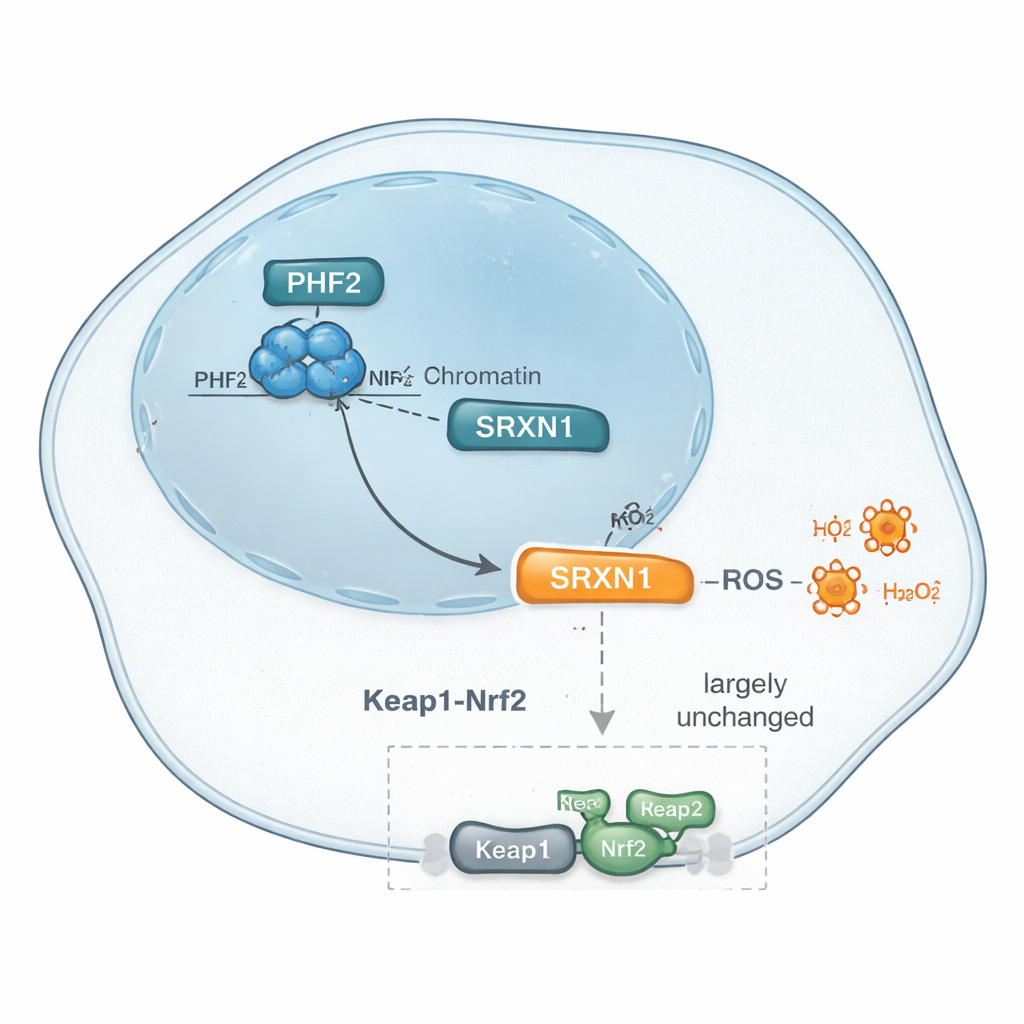
Därefter använde forskarna moderna proteomikmetoder för att katalogisera tusentals proteiner vars nivåer förändrades när PHF2 minskades. Bland många subtila förändringar framträdde ett mönster: nivåerna av ett stresskyddande protein kallat SRXN1 sjönk konsekvent när PHF2 förlorades. SRXN1 hjälper celler att hantera reaktiva syreföreningar—kemiskt reaktiva biprodukter som kan skada DNA och proteiner men som också kan pressa cancerceller att anpassa sig. Data föreslog att PHF2 hjälper till att upprätthålla SRXN1-nivåer, och att en förändring i denna balans kan påverka hur levercancerceller svarar på inre stress och i förlängningen hur snabbt de växer.
Verkar utanför en välkänd stressväg
SRXN1 regleras vanligtvis av en huvudfaktor för stressrespons kallad Nrf2, som aktiverar många antioxidantgener när celler utsätts för oxidativ stress. Eftersom SRXN1 sjönk när PHF2 undertrycktes, frågade sig teamet om PHF2 helt enkelt kunde verka via den välkända Nrf2-vägen. De undersökte nyckelgener och -proteiner relaterade till Nrf2, behandlade celler med läkemedel som aktiverar Nrf2 genom att blockera dess inhibitor Keap1, och använde genetiska verktyg för att direkt minska Keap1. I dessa tester liknade svaret hos PHF2‑defekta celler i hög grad svaret hos normala celler, och bredare väg- och transkriptionsfaktoranalyser pekade inte på Nrf2 som en huvudaktör. Istället framkom andra faktorer, inklusive ZNF384 och Nrf1—båda tidigare kopplade till levercancer—som kandidater. Tillsammans tyder bevisen på att PHF2:s kontroll över SRXN1 och antioxidantresponsen kan kringgå klassisk Nrf2‑signalering, vilket antyder en distinkt stressregleringsväg i dessa tumörer.
Vad detta kan innebära för framtida behandlingar
För en icke-specialist är huvudsaken att denna studie identifierar PHF2 som en lovande skyddsfaktor i levercancer: när PHF2 är närvarande och aktiv växer tumörceller långsammare; när den minskar får de en tillväxtfördel och ändrar hur de hanterar cellulär stress. Eftersom PHF2 i sig kan vara svår att hämma eller förstärka med konventionella småmolekylära läkemedel pekar författarna på framväxande strategier som RNA‑baserade terapier eller läkemedel som ökar PHF2:s aktivitet via uppströms signaleringspartner. De betonar också att PHF2:s effekter är kontextberoende—dess påverkan kan variera med andra mutationer som p53-status—så eventuell framtida behandling sannolikt skulle kräva noggrann patienturval. Sammanfattningsvis förfinar arbetet vår förståelse för hur epigenetiska regulatorer formar levercancerbeteende och öppnar nya vägar för att utveckla behandlingar som återställer eller imiterar PHF2:s tumörsuppressiva inverkan.
Citering: Thng, D.K.H., Hooi, L., Yong, W.K. et al. The role of histone demethylase PHF2 as a tumour suppressor in hepatocellular carcinoma by regulating SRXN1. Oncogenesis 15, 6 (2026). https://doi.org/10.1038/s41389-026-00597-2
Nyckelord: hepatocellulärt carcinom, epigenetisk reglering, PHF2, SRXN1, levercancerterapi