Clear Sky Science · sv
TRIM21-medierad nedbrytning av HILPDA övervinner anti-PD-1-immunterapiresistens i bröstcancer genom att begränsa PD-L1-palmitoylering
Varför vissa cancerimmunterapier slutar fungera
Läkemedel som släpper loss immunsystemet, som anti–PD‑1‑terapier, har förändrat behandlingen av flera cancerformer, inklusive aggressiva varianter av bröstcancer. Ändå svarar många tumörer aldrig eller hittar så småningom sätt att undkomma. Denna studie undersöker en sådan flyktrutt i trippelnegativ bröstcancer och visar hur omkoppling av tumörers fettmetabolism — och ett omfördelat läkemedel kallat fenretinid — kan öppna dörren igen för immunsystemet när standardimmunterapi misslyckas. 
En dold hjälpare som skyddar tumörer
Forskarna fokuserade på ett lite känt protein kallat HILPDA, tidigare kopplat till hur celler hanterar fett vid stress. Genom att jämföra mössens brösttumörer som förblev känsliga för anti‑PD‑1‑terapi med tumörer som blivit resistenta fann de att HILPDA-nivåerna var mycket högre i de resistenta cancrarna. Analys av stora patientdatabaser och tumörprover från kvinnor med bröstcancer bekräftade att HILPDA är mer rikligt förekommande i tumörer än i normalt bröstvävnad, särskilt vid trippelnegativ sjukdom, och att patienter vars tumörer uttrycker mer HILPDA tenderar att ha sämre utfall. Tumörer från personer som inte hade nytta av PD‑1‑blockerande läkemedel hade också mer HILPDA, vilket knyter detta protein direkt till behandlingssvikt.
Hur tumörer vänder immunsystemets landskap mot oss
För att se vad HILPDA faktiskt gör inne i tumörer, konstruerade teamet bröstcancerceller som antingen överproducerade eller saknade proteinet och odlade dem sedan tillsammans med mänskliga immunceller eller i möss. När HILPDA var högt drog tumörerna till sig fler regulatoriska T‑celler, myeloid‑deriverade suppressorceller och M2‑lika makrofager — immuncellstyper som dämpar anfall och hjälper tumörer att gömma sig. Samtidigt minskade antalet och vigör hos cytotoxiska CD8 T‑celler och natural killer‑celler, och deras förmåga att frisätta toxiska molekyler och inflammatoriska signaler försvagades. Att tysta HILPDA vände på detta: tumörer hade färre suppressiva celler, fler aktiva mördarceller, långsammare tillväxt och färre metastaser. Avgörande var att när djur med låg‑HILPDA‑tumörer fick anti‑PD‑1‑terapi krympte tumörerna mer och mössen levde längre, vilket visar att HILPDA kontrollerar hur väl immunterapin fungerar.
Fettproduktion, molekylärt pansar och immunflykt
Vidare grävande avslöjade hur HILPDA omformar tumörernas metabolism för att stärka immunförsvaret. Inne i cancerceller binder HILPDA till ett chaperonprotein kallat HSP90 för att stabilisera en transkriptionsfaktor, KLF5, som driver fettproduktion. Denna trio ökar syntesen av fettsyror, särskilt palmitat, och fyller tumörcellerna med lipid-droppar. En av dessa fetter fästs sedan på PD‑L1, kontrollproteinet som sitter på tumörytan och skickar en "attacka inte"‑signal till immunceller. Teamet visade att tillsats av palmitat till en specifik punkt på PD‑L1 fungerar som ett molekylärt lim: det hjälper PD‑L1 att sitta stabilt i cellmembranet och förhindrar att det bryts ner. Mutation av denna enda fästpunkt berövade PD‑L1 dess stabilitet och försvagade dess förmåga att skydda cancerceller, även när HILPDA var rikligt. Med andra ord matar HILPDA‑driven fettproduktion en kemisk modifiering av PD‑L1 som förvandlar tumörens immunskydd från skört till förstärkt stål.
Den inbyggda bromsen som kan aktiveras
Varje gas behöver en broms, och här är bromsen ett annat protein kallat TRIM21. Författarna upptäckte att TRIM21 känner igen HILPDA och märker det med molekylära "flaggor" som skickar det till cellens sophanteringsmaskineri. I brösttumörer från patienter tenderade TRIM21‑nivåerna att vara låga när HILPDA var högt, och låg TRIM21 var kopplat till sämre utfall, vilket antyder att detta naturliga bromssystem ofta försvagas i cancer. Teamet sökte därefter efter läkemedel som kunde stärka TRIM21 och identifierade fenretinid, en retinoid som redan testats på människor. I cell‑ och djurmodeller av trippelnegativ bröstcancer ökade fenretinid TRIM21‑aktiviteten, accelererade nedbrytningen av HILPDA, minskade fettsyntes och PD‑L1:s skyddande modifiering, och bromsade tumörtillväxt och spridning. Mest anmärkningsvärt var att kombinationen av fenretinid och anti‑PD‑1‑terapi gjorde tumörerna mer sårbara för immunsvar, ökade antal mördarceller och natural killer‑celler samtidigt som suppressiva celler i tumörmikromiljön minskade. 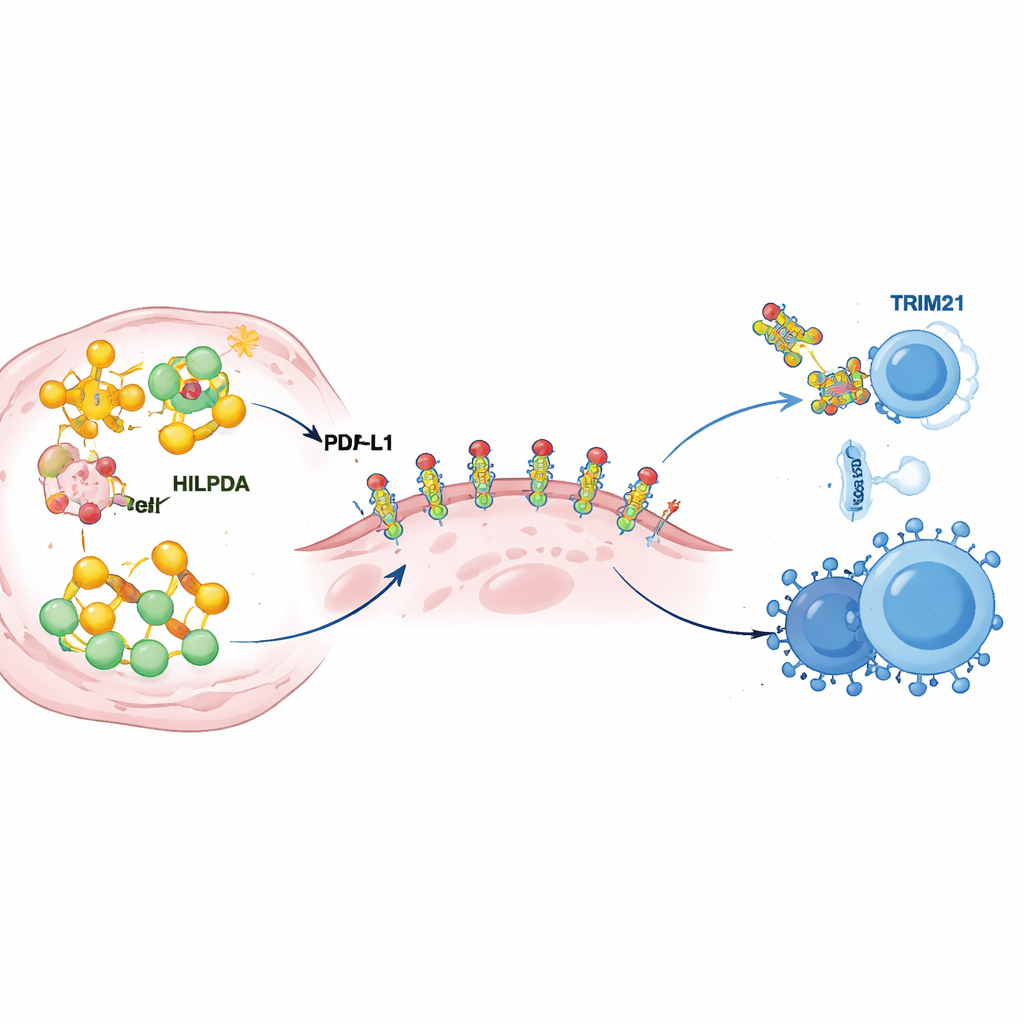
Vad detta innebär för framtida cancervård
Detta arbete avslöjar en kedja av händelser där stressade bröstcancerceller höjer HILPDA, skruvar upp fettproduktionen och kemiskt förstärker PD‑L1 på sin yta, vilket gör att de kan fortsätta undertrycka immunceller även inför PD‑1‑blockerande läkemedel. TRIM21 fungerar som en intern säkerhetsbroms som kan demontera HILPDA, men den är ofta för svag i tumörer. Genom att visa att fenretinid kan återaktivera denna broms pekar studien på ett praktiskt sätt att kombinera ett metabolt riktat läkemedel med befintlig immunterapi för att övervinna resistens. Om detta bekräftas i kliniska prövningar kan målning av TRIM21–HILPDA–PD‑L1‑axeln ge patienter med svårbehandlad trippelnegativ bröstcancer en andra chans att dra nytta av immunbaserade behandlingar.
Citering: Wang, X., Li, G., Wu, J. et al. TRIM21-mediated degradation of HILPDA overcomes anti-PD-1 immunotherapy resistance in breast cancer by limiting PD-L1 palmitoylation. Oncogene 45, 1338–1356 (2026). https://doi.org/10.1038/s41388-026-03728-6
Nyckelord: trippelnegativ bröstcancer, immunoterapiresistens, PD-L1-palmitoylering, tumörers lipidmetabolism, fenretinid