Clear Sky Science · sv
Cereblon (CRBN) hämmar prostatacancer‑metastasering genom negativ reglering av 6‑fosfoglukonatdehydrogenas (6PGD)
Varför denna forskning är viktig
När prostatacancer sprider sig från prostatan till andra organ blir den mycket svårare att behandla och ofta livshotande. Denna studie visar hur ett relativt okänt cellulärt ”kvalitetskontroll”‑protein, cereblon (CRBN), bidrar till att förhindra att prostatacancer sprider sig genom att avlägsna ett metabolt enzym som driver aggressivt beteende. Att förstå detta inbyggda bromssystem öppnar för nya sätt att sakta eller stoppa metastasering, särskilt i svårbehandlade former av sjukdomen.
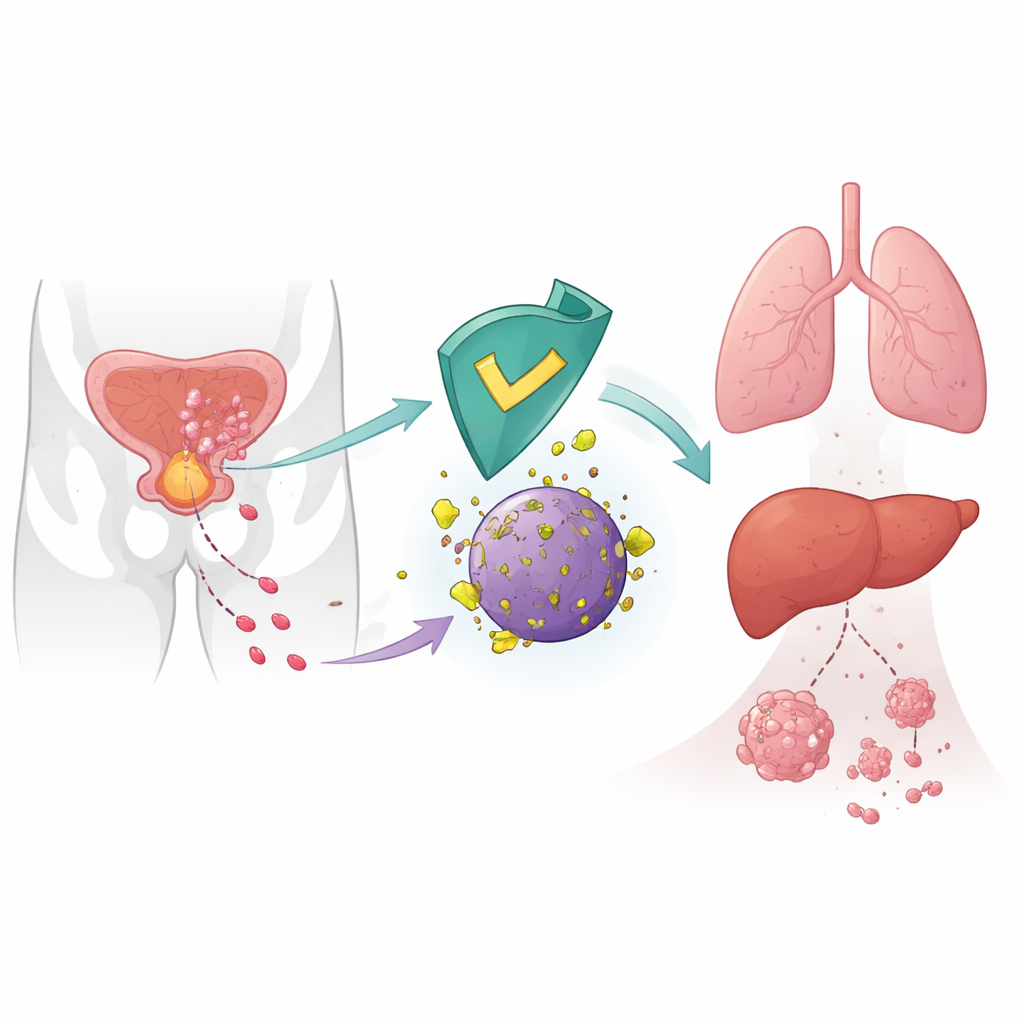
En intern broms mot cancerspridning
Cancerceller sprider sig inte slumpmässigt; de omprogrammerar sitt inre maskineri för att röra sig, invadera och kolonisera avlägsna organ. Forskarna inriktade sig på CRBN, ett protein mest känt som målet för läkemedel som talidomid som används vid blodcancer. I friska celler ingår CRBN i en molekylär avfallshanterare som märker vissa proteiner för nedbrytning. Tidigare arbete antydde att låga CRBN‑nivåer i tumörer var kopplade till sämre utfall, men dess direkta roll i metastasering var oklart. Här visar forskarna att CRBN fungerar som en naturlig suppressor av prostatacancer‑spridning genom att rikta ett metabolt enzym kallat 6‑fosfoglukonatdehydrogenas (6PGD) för nedbrytning.
En metabol motor som cancer kapar
6PGD verkar i en metabol väg känd som den oxiderande pentosfosfatvägen, som hjälper celler att producera NADPH, en molekyl som levererar både byggstenar och antioxidantkapacitet. Många tumörer skruvar upp denna väg för att växa snabbare och tåla stress. Gruppen fann att prostatacancerprover från patienter tenderar att ha mindre CRBN och mer 6PGD än normalt prostatavävnad, och att denna obalans är särskilt uttalad i aggressiv sjukdom. I prostatacancercellinjer ledde nedsättning av CRBN eller nedbrytning av det med en designad förening till ökade 6PGD‑proteinnivåer och enzymaktivitet, vilket ökade NADPH. Återställande av CRBN gav motsatt effekt — lägre 6PGD och NADPH utan förändring i 6PGD:s genbudskap — vilket pekar på en reglering på proteinnivå.
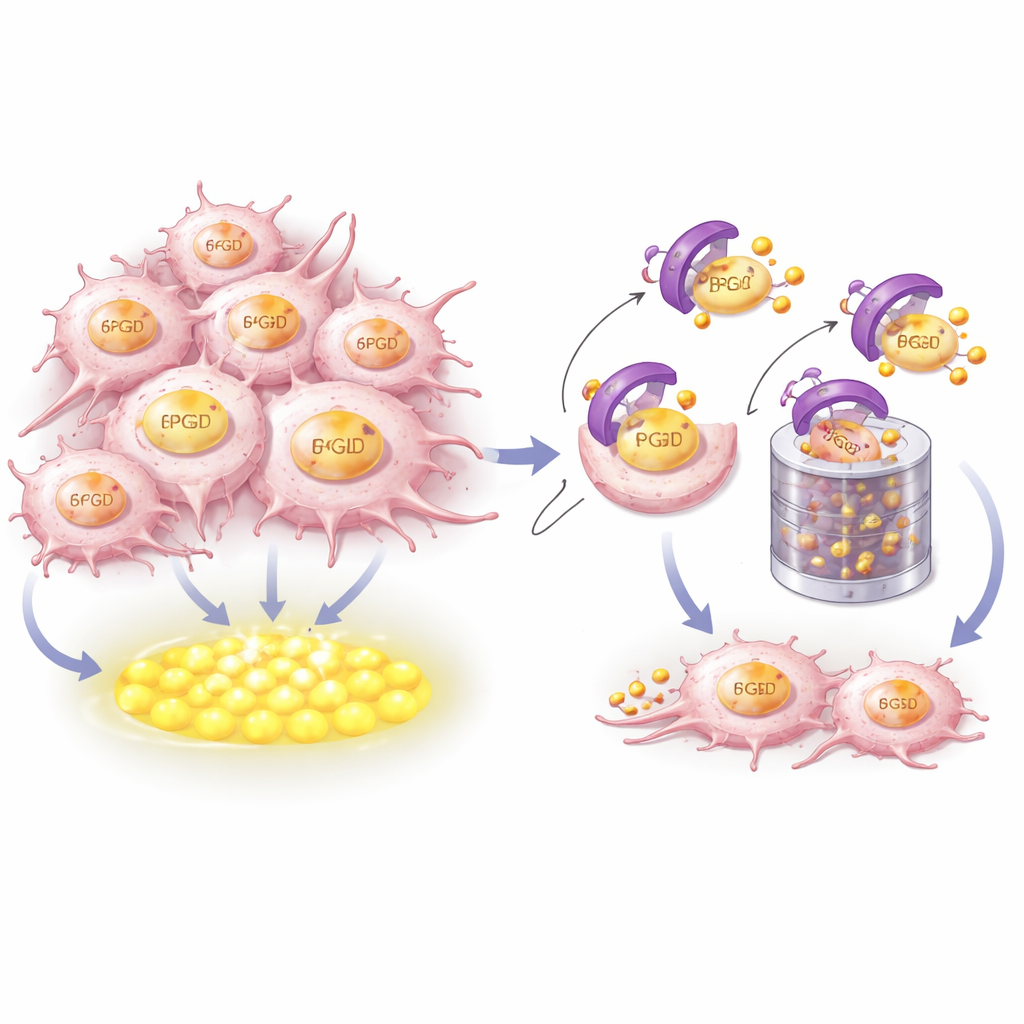
Hur CRBN känner igen och förstör bränslekällan
För att förstå hur CRBN kontrollerar 6PGD kombinerade forskarna strukturell modellering med biokemiska experiment. De visade att CRBN fysiskt greppar ett kort, högt bevarat helixsegment nära 6PGD:s C‑ände. Nyckelaminosyror i båda proteinerna bildar ett tätt dockningsgränssnitt. När dessa kontaktpunkter ändrades kunde CRBN inte längre binda 6PGD, fästa de små ubiquitin‑märken som markerar proteinet för nedbrytning, eller skicka det till cellens malningsmaskin, proteasomen. Noterbart är att denna igenkänningsyta är skild från fickan där immunmodulerande läkemedel binder CRBN, vilket betyder att CRBN:s kontroll över 6PGD är en del av dess naturrena hushållningsroll snarare än en läkemedelsinducerad effekt.
Från förändrad metabolism till vandrande celler
Konsekvenserna av detta molekylära handslag syns i cellbeteende. I prostatacancerceller utan CRBN gick förhöjda 6PGD‑ och NADPH‑nivåer hand i hand med ökad rörlighet och invasion genom artificiella barriärer — kännetecken för metastatisk potential. När CRBN överuttrycktes blev cellerna mindre rörliga och invasiva, trots oförändrad tillväxthastighet. Genuttrycksprofilering visade att CRBN ökade nivåerna av CDH1, förknippat med tätt packade epitelceller, och sänkte nivåerna av MMP1, kopplat till vävnadsnedbrytning och migration. Viktigt är att dessa förskjutningar krävde direkt CRBN–6PGD‑bindning och kunde återställas genom att blockera 6PGD:s enzymaktivitet, vilket knyter ihop förändrad metabolism med förändrat metastasbeteende.
Bevis från djurmodeller och andra cancerformer
Forskarna testade dessa idéer i möss genom att injicera prostatacancerceller i blodomloppet eller mjälten. Celler konstruerade för att producera extra CRBN bildade betydligt färre metastatiska noduler i levern och lungorna än kontrollceller, vilket bekräftar en anti‑metastatisk roll i levande djur. Möss saknade CRBN visade högre 6PGD‑proteinhalter i flera organ. Liknande mönster sågs i glioblastom‑, lunga‑ och njurceller: borttag av CRBN ökade 6PGD och främjade cellrörelse och invasion, medan genetisk eller läkemedelsmässig hämning av 6PGD dämpade detta aggressiva beteende. Dessa observationer tyder på att CRBN–6PGD‑bromsen mot metastasering inte är unik för prostatacancer.
Vad detta kan betyda för framtida behandlingar
Sammanfattningsvis föreslår studien att CRBN fungerar som en metabol grindvakt som begränsar energiförsörjningen som krävs för att cancerceller ska lösas upp, migrera och så frö till nya tumörer. När CRBN förloras eller är låg ackumuleras 6PGD, NADPH‑produktionen skjuter i höjden och cellerna är mer benägna att genomgå förändringar som gynnar metastasering. För patienter pekar detta på två möjligheter: att mäta CRBN‑ och 6PGD‑nivåer kan hjälpa till att identifiera tumörer med hög metastasrisk, och att terapier som förstärker CRBN‑funktionen — eller selektivt dämpar 6PGD i CRBN‑fattiga tumörer — kan erbjuda nya sätt att sakta eller förhindra spridning av prostata‑ och andra cancerformer.
Citering: Guchhait, K., Yoon, HS., An, HS. et al. Cereblon (CRBN) inhibits prostate cancer metastasis by negatively regulating 6-phosphogluconate dehydrogenase (6PGD). Oncogene 45, 1234–1246 (2026). https://doi.org/10.1038/s41388-026-03717-9
Nyckelord: prostatacancer‑metastasering, cancermetabolism, cereblon, 6PGD‑enzym, NADPH‑väg