Clear Sky Science · sv
L1TD1 främjar progression av kolorektal mukinös adenomkarsinom genom att öka stabiliteten hos ABCC3-mRNA
Varför denna slemfyllda cancer är viktig
Kolorektal cancer är en ledande orsak till cancerdöd i världen. Inom denna grupp finns en speciell undertyp som kallas mukinöst adenomkarsinom, som utmärker sig genom att tumörerna är fyllda med tjockt slem som utgör mer än hälften av tumörmassan. Denna slembarrär kan hjälpa cancerceller att gömma sig från cellgifter och kroppens försvar. Den här studien ställer en enkel men avgörande fråga: vad styr all den där slemproduktionen, och kan vi stänga av den för att bromsa cancer och få behandlingar att fungera bättre?
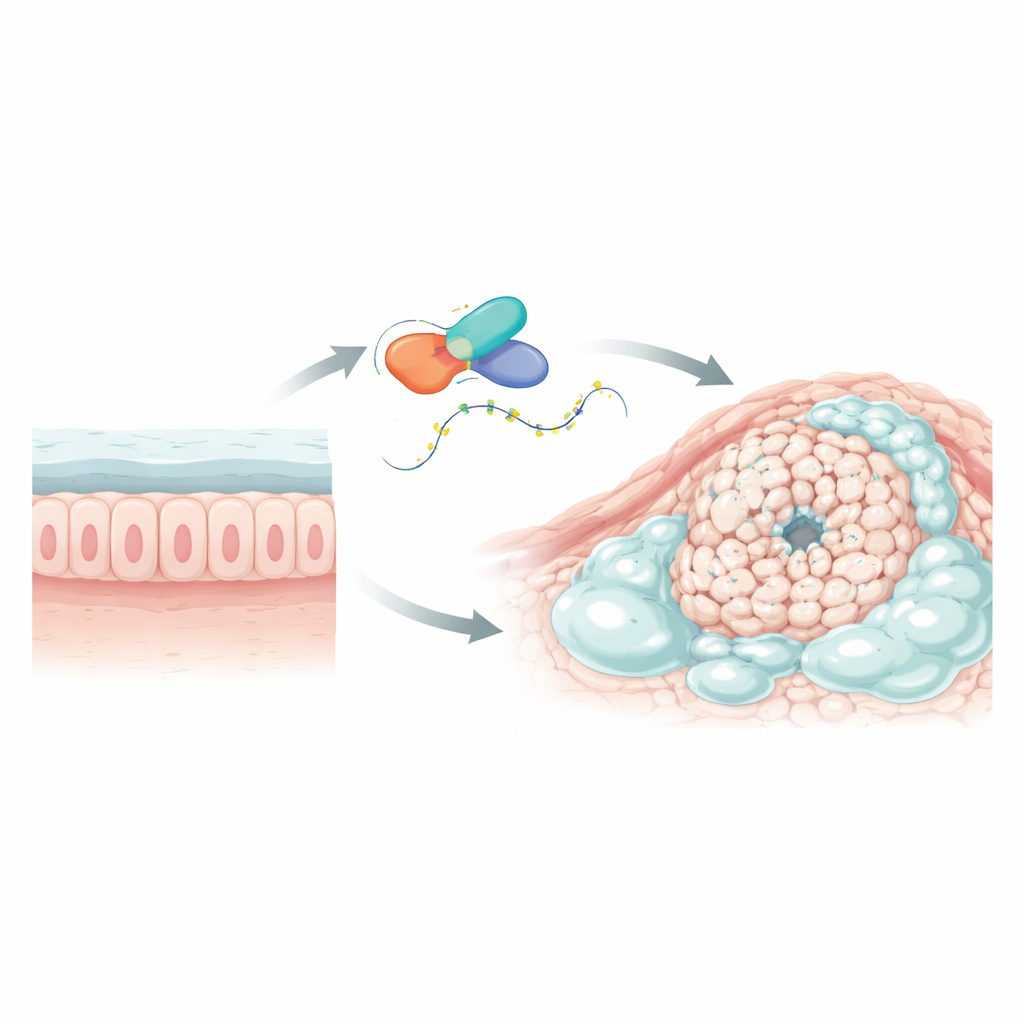
Att hitta en nyckelgen som ställer till problem
Forskarna sökte först i stora cancerregister och i enkelcellssekvenseringsdata för att identifiera gener som beter sig annorlunda i slemtäta kolorektala tumörer jämfört med vanliga kolorektala cancerformer och omgivande frisk vävnad. En gen, kallad L1TD1, framträdde tydligt. Den var kraftigt uppreglerad i mukinösa tumörer men inte i vanliga tumörer och var högre i tumörvävnad än i den omgivande normala tarmen. L1TD1 kodar för ett protein som binder RNA, molekylen som förmedlar genetiska budskap från DNA till cellens proteinsyntesmaskineri. Eftersom RNA-bindande proteiner kan finkalibrera hur länge budskapen kvarstår och hur effektivt de läses av, var L1TD1 en stark kandidat att fungera som en huvudregulator i dessa slemfyllda cancerformer.
Hur L1TD1 driver cancern att växa och sprida sig
För att testa vad L1TD1 faktiskt gör använde teamet koloncancercellinjer och musmodeller. När de ökade L1TD1-nivåerna i cancercellerna delade cellerna snabbare, rörde sig lättare och invaderade vävnadsliknande barriärer mer aggressivt. Att sänka L1TD1 gav motsatt effekt, med långsammare tillväxt och minskad invasion. I möss som injicerades med L1TD1-höga celler växte tumörerna större och spred sig oftare till levern och bukhålan. Tumörer med mer L1TD1 tenderade också att vara större, mindre differentierade och i mer avancerade stadier hos patienter, vilket kopplar denna gen till ett sämre sjukdomsbeteende kliniskt.
Aktivering av slem och läkemedelsresistens
Slemmet i sig visade sig vara centralt för L1TD1:s effekt. Celler med högre L1TD1 producerade större mängder nyckelproteiner för slemproduktion, särskilt MUC2 och MUC5AC, och uppvisade drag av bägarceller, de normala slemutsöndrande cellerna i tarmen. Tredimensionella odlingar och vävnadsfärgningar från både patienter och möss bekräftade att högre L1TD1 samvarierade med tjockare och mer rikligt slem. Viktigt är att detta slem inte bara var ett bihang. När forskarna selektivt minskade MUC2 försvann till stor del den extra tillväxt, invasion och cellgiftresistens som drivs av L1TD1. Celler rika på L1TD1 var svårare att döda med det vanliga läkemedlet oxaliplatin, och tumörer med dessa celler krympte mindre i behandlade möss, vilket understryker att slemmet fungerar som en sköld som L1TD1 hjälper till att bygga.
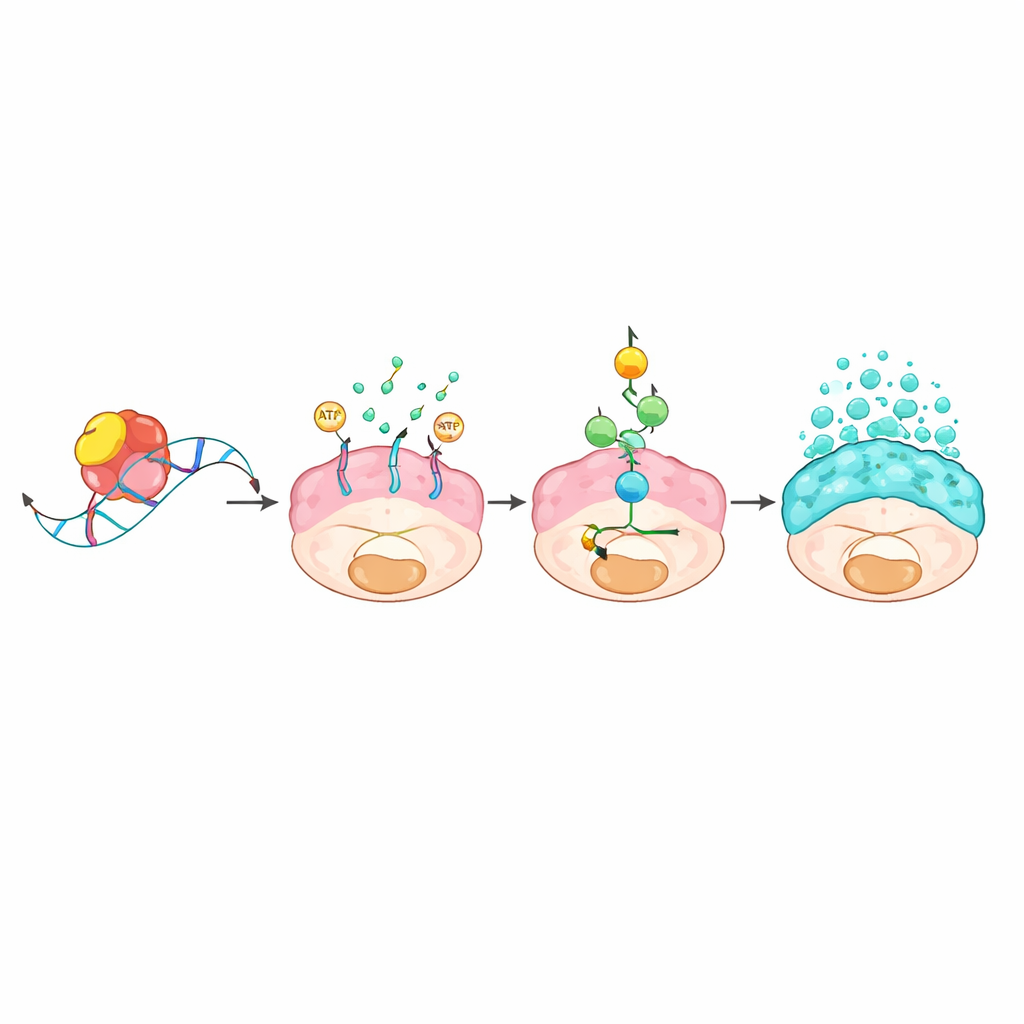
En molekylär kedja som länkar RNA-kontroll till slemöversvämningar
Teamet undersökte sedan hur ett RNA-bindande protein kan ge upphov till sådana dramatiska förändringar. Genom att fiska upp RNA-molekyler som fysiskt var bundna till L1TD1 och jämföra genaktivitet med och utan L1TD1 identifierade de en transportörgen kallad ABCC3 som ett huvudmål. L1TD1 fäste vid en kort ”GUGU”-motif i slutet av ABCC3:s RNA-meddelande och stabiliserade det så att cellen producerade mer av ABCC3-proteinet, känt som MRP3. Denna transportör sitter i cellmembranet och använder energi för att pumpa ut ämnen ur cellen. Den resulterande energiförbrukningen aktiverade ett metabolt larmsystem centrerat kring sensorn AMPK, som i sin tur slog på en klassisk tillväxt- och stressväg känd som MAPK. När denna kaskad aktiverades ökade produktionen och utsöndringen av slemproteiner och förstärkte cancercellernas förmåga att växa, migrera och motstå läkemedel. Att blockera ABCC3 genetiskt eller med en experimentell förening, eller att hämma MAPK-vägen, dämpade alla slemproduktionen och försvagade tumörerna.
Vad detta betyder för patienter
Sammantaget avslöjar arbetet ett stegvis kontrollsystem för slemtät kolorektal cancer: L1TD1 stabiliserar ABCC3:s RNA, ABCC3 tömmer cellulär energi, AMPK–MAPK-vägen aktiveras, och tumören svarar genom att överproducera slem och bli mer aggressiv och läkemedelsresistent. För patienter pekar detta på flera lovande angreppssätt. Nivåer av L1TD1 och ABCC3 skulle kunna hjälpa till att identifiera tumörer som sannolikt beter sig illa eller resistenta mot standardkemoterapi. Ännu viktigare är att läkemedel som stör L1TD1–ABCC3-interaktionen, blockerar MRP3:s pumppaktivitet eller riktar in sig på den nedströms signalvägen kan tunna ut slembarrären, bromsa tumörtillväxt och göra befintliga behandlingar mer effektiva för denna utmanande form av kolorektal cancer.
Citering: He, H., Yuan, J., Wang, H. et al. L1TD1 promotes colorectal mucinous adenocarcinoma progression by enhancing ABCC3 mRNA stability. Oncogene 45, 1071–1086 (2026). https://doi.org/10.1038/s41388-026-03716-w
Nyckelord: muköst kolorektalt cancer, L1TD1, ABCC3 MRP3, mukusproduktion, kemoresistens