Clear Sky Science · sv
Den multifunktionella RNA-helicasen DDX39A driver glioblastomprogression genom att modulera alternativ splitsning av WISP1 som inducerar en immunosuppressiv makrofagpolarisering
Varför denna hjärntumörstudie är viktig
Glioblastom är en av de dödligaste hjärntumörerna, känd för att återkomma efter behandling och motstå läkemedel. Denna studie avslöjar hur en enda molekylär ”omkopplare” i tumörceller inte bara hjälper cancern att växa utan också övertalar närliggande immunceller att sluta bekämpa och istället börja skydda tumören. Genom att spåra denna händelsekedja identifierar forskarna också ett befintligt antipsykotiskt läkemedel som skulle kunna återanvändas för att störta detta skadliga nätverk.
En nyckelhjälpare inne i hjärntumörceller
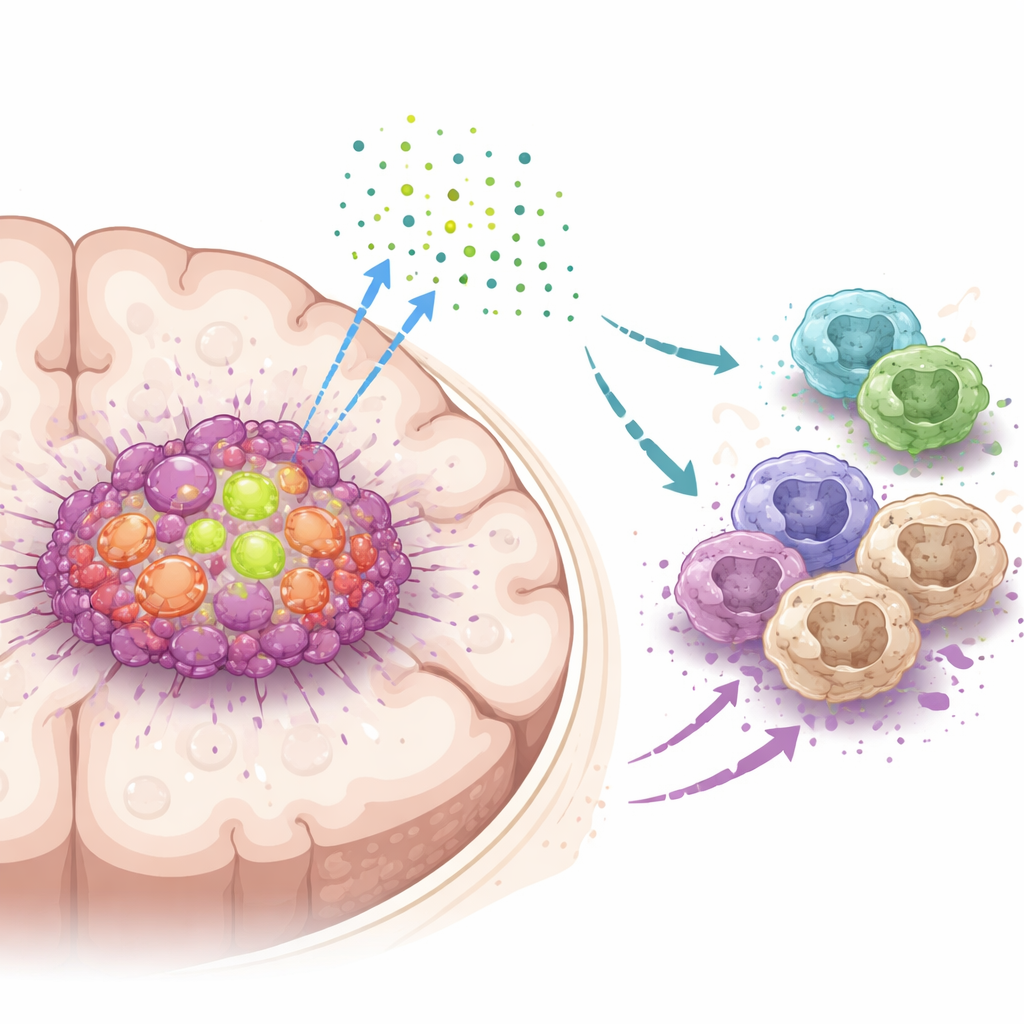
Teamet fokuserade på ett protein kallat DDX39A, en molekylär maskin som hjälper celler att bearbeta RNA, det fungerande kopian av genetisk information. Genom att analysera stora patientdatasatser och tumörprover fann de att DDX39A är mycket mer aktivt i glioblastom än i normalt hjärnvävnad, och dess nivåer ökar med tumörgrad. Encellsanalyser visade att DDX39A är särskilt rikligt i snabbt delande tumörceller och i vissa immunceller kallade makrofager inne i tumörmassan. Patienter vars tumörer hade högre DDX39A tenderade att få sämre utfall, vilket tyder på att detta protein är nära kopplat till aggressiv sjukdom.
Hur denna hjälpare driver tillväxt och spridning
För att testa vad DDX39A faktiskt gör använde forskarna genetiska verktyg för att sänka dess nivå i glioblastomstamliknande celler odlade i laboratoriet och i musemodeller av hjärntumörer. När DDX39A minskades växte tumörcellerna långsammare, invaderade omgivande vävnad mindre effektivt och var mer benägna att genomgå programmerad celldöd. De stamliknande cancercellerna förlorade också mycket av sin förmåga att bilda nya tumörsfärer, ett tecken på att deras självförnyelse kapacitet var försämrad. Hos möss var tumörer med sänkt DDX39A mindre och djuren levde längre, vilket bekräftar att detta protein aktivt driver tumörprogression och inte bara är en passiv markör.
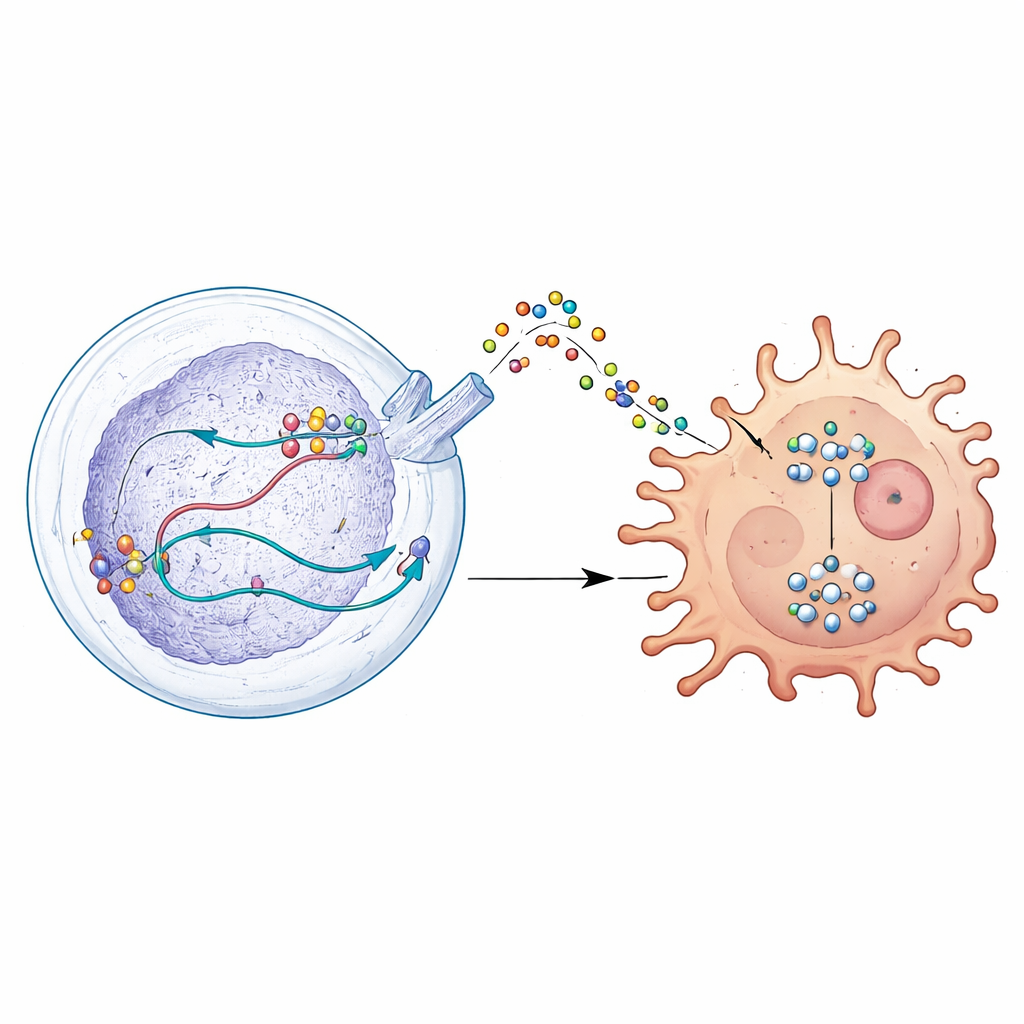
En hemlig signal som avväpnar immundefenderare
Genom fördjupade analyser upptäckte forskarna att DDX39A förändrar hur en gen kallad WISP1 bearbetas. Istället för att bara slå på eller av WISP1 hjälper DDX39A till att forma dess RNA på ett sätt som stabiliserar budskapet och ökar produktionen av WISP1-protein. Tumörcellerna frigör sedan WISP1 i sin omgivning, där det fungerar som en oroande vilseledande signal. Närliggande makrofager, som antingen kan attackera tumörer eller stödja dem, svarar på denna signal genom att skifta till ett immunosuppressivt, tumörhjälpande tillstånd. Detta skifte drivs genom aktivering av en tillväxtreglerande signalväg inuti celler känd som AKT. När DDX39A eller WISP1 minskades tystnade denna väg, tumörceller blev mindre aggressiva och makrofager rörde sig tillbaka mot en mer tumörbekämpande profil.
Att förvandla ett psykiatriskt läkemedel till ett cancerverktyg
Utrustade med denna vägkarta sökte forskarna i läkemedelsdatabaser efter molekyler som kan störa DDX39As aktivitet. De fastnade för fluphenazin, ett länge använt antipsykotiskt läkemedel som är känt för att nå hjärnan. Datorbaserade modeller och bindningstester visade att fluphenazin kan fästa direkt på DDX39A. I tumörceller försvagade läkemedlet DDX39As bindning till WISP1-RNA, sänkte WISP1-nivåerna och minskade AKT-signaleringen. Behandlade celler växte mindre, invaderade mindre, bildade färre tumörsfärer och hade högre dödlighet. I musemodeller bromsade fluphenazin hjärntumörtillväxt, minskade antalet tumörstödjande makrofager och förlängde överlevnaden, allt vid doser som liknade dem som redan används hos människor för andra tillstånd.
Vad detta betyder för framtida behandling
I enkla termer visar studien att glioblastomceller utnyttjar DDX39A för att finslipa ett budskap (WISP1) som både stärker deras egen uthållighet och omprogrammerar närliggande immunceller till kroppsvakter istället för soldater. Att blockera denna hjälpare, antingen genetiskt eller med ett läkemedel som fluphenazin, försvagar cancern på två fronter: tumörcellerna själva och den skyddande skölden av immunosuppressiva makrofager. Även om mycket mer testning krävs innan denna strategi kan nå patienter, öppnar arbetet en lovande väg för att återanvända ett välbekant läkemedel för att träffa en nyupptäckt svag punkt i en av de mest seglivade hjärntumörerna.
Citering: Zhang, Y., Xue, Z., Zhang, N. et al. The multifunctional RNA helicase DDX39A drives glioblastoma progression by modulating WISP1 alternative splicing that induces an immunosuppressive macrophage polarization. Oncogene 45, 1026–1041 (2026). https://doi.org/10.1038/s41388-026-03715-x
Nyckelord: glioblastom, RNA-splitsning, tumörmikromiljö, makrofagpolarisering, Läkemedelsåteranvändning