Clear Sky Science · sv
PMM2 interagerar med TRIM28 för att rekrytera E2F4 och främja KIFC3-medierad tumörglykolys och kolorektal cancerprogression
Varför denna cancerberättelse är viktig
Kolorektal cancer är en av världens dödligaste cancerformer, delvis därför att många tumörer lär sig kapa kroppens energisystem för att driva okontrollerad tillväxt. Denna studie avslöjar hur ett mindre känt enzym, PMM2, hjälper kolorektala tumörer att förbränna socker mer aggressivt och sprida sig, och varför det gör enzymet till ett lovande nytt mål för framtida läkemedel och diagnostiska tester.
En sockerhungrig tumörmotor
Cancerceller omkopplar ofta hur de använder glukos, till förmån för en snabb men ineffektiv form av sockerförbränning som kallas glykolys. Forskarna började med att jämföra tusentals gener i kolorektala tumörprov med närliggande frisk vävnad. PMM2, ett enzym som vanligtvis är involverat i att fästa sockerstrukturer på proteiner, framträdde som en av de mest uppreglerade generna i tumören. Tumörceller med ökat PMM2 växte snabbare, bildade fler kolonier och spred sig lättare i odlingsskålar, medan celler där PMM2 stängdes av saktade sin tillväxt, migrerade mindre och var mer benägna att dö.
Hur tumörceller överladdar sockeranvändningen
När teamet minskade PMM2-nivåerna i kolorektala cancerceller tog cellerna upp mindre glukos, producerade mindre ATP (deras huvudsakliga energivaluta) och frisatte mindre laktat, glykolysens avfallsprodukt. Känsliga metaboliska mätningar bekräftade att den övergripande försurningen av omgivande medium sjönk, medan syreförbrukningen ökade, vilket betyder att cellerna skiftade bort från turbocharged glykolys mot mer normal respiration. Nyckelproteiner som hjälper glykolysen, PKM2 och LDHA, minskade också. Överraskande nog kunde även en katalytiskt ”död” version av PMM2 fortfarande driva detta sockerhungriga beteende, vilket visar att enzymets roll i cancer inte beror på dess vanliga kemi utan på vilka proteiner det binder till inne i cellen.
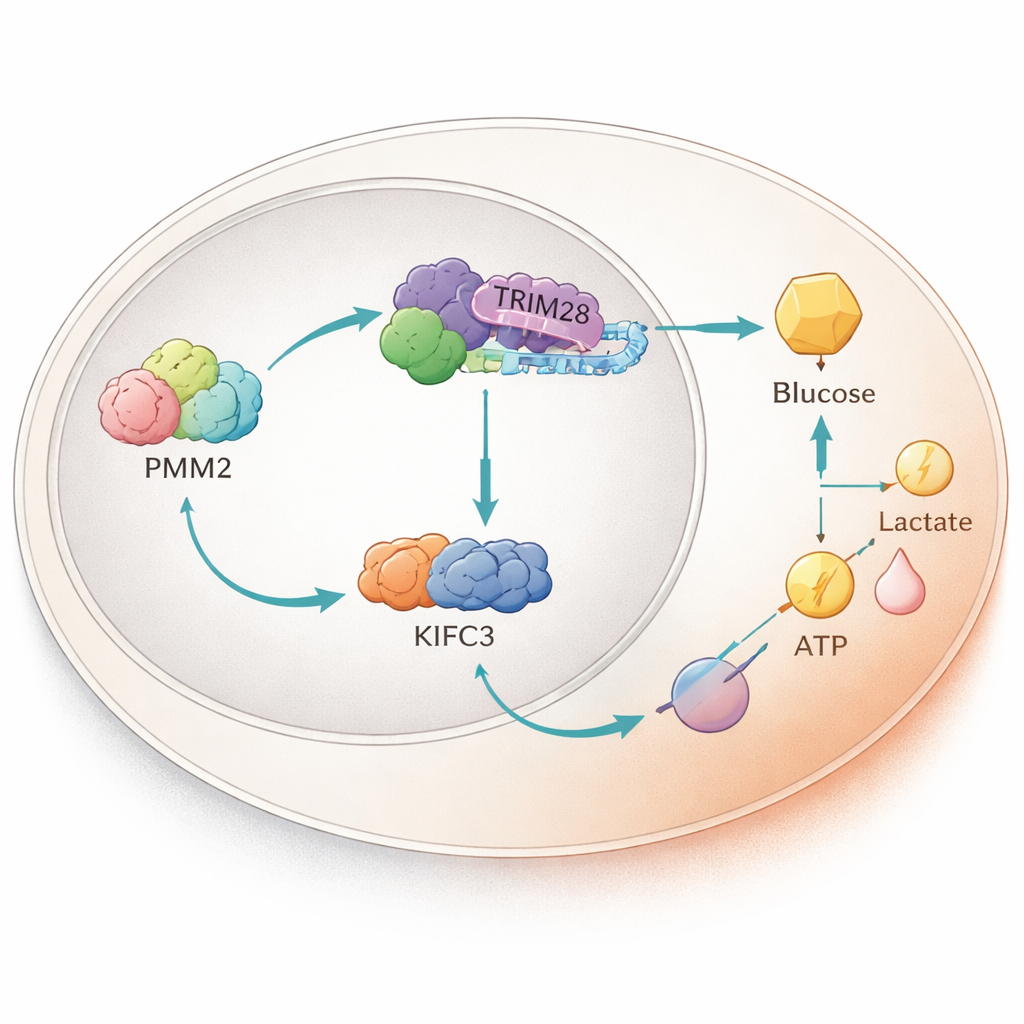
En proteinnedkoppling inne i kärnan
När forskarna grävde djupare fann de att PMM2 fysiskt hakar i ett annat protein som heter TRIM28, vilket kan röra sig in i cellkärnan och påverka genaktivitet. PMM2 hjälper TRIM28 att ackumuleras i kärnan, där TRIM28 samarbetar med en transkriptionsfaktor, E2F4. Tillsammans ökar denna trio produktionen av ett motorprotein kallat KIFC3 genom att binda till ett specifikt avsnitt i dess DNA-regionskontroll. Experiment som tog bort den del av PMM2 som krävs för TRIM28-bindning utslocknade PMM2:s förmåga att öka glykolys och celltillväxt, vilket understryker att det är detta proteinkomplex—inte PMM2:s klassiska enzymfunktion—som driver tumörfördelen.
Att vrida upp en viktig metabolisk strömbrytare
KIFC3, bättre känt för sin roll i att transportera last längs cellens interna skelett, visade sig vara en avgörande metabolisk strömbrytare. När forskarna sänkte KIFC3-nivåerna förbrukade kolorektala cancerceller mindre glukos, producerade mindre ATP och laktat och visade svagare glykolytisk aktivitet, medan deras syreförbrukning ökade. Viktigt är att tystande av KIFC3 delvis avbröt glykolysökningen och tillväxtfördelen som normalt orsakades av PMM2. I möss med implanterade humana kolorektala cancerceller växte tumörer med extra PMM2 större, men denna effekt minskade när KIFC3 slogs ned. Tumörprover från dessa djur visade högre nivåer av PMM2, KIFC3 och glykolysmarkörer, vilket binder ihop hela händelsekedjan i levande vävnad.
Från laboratoriemodeller till patientprov
För att föra arbetet närmare kliniken skapade teamet tredimensionella miniatyrtumörer, så kallade organoider, från patienters kolorektala cancer. Organoider med högre PMM2- och KIFC3-nivåer växte snabbare och producerade mer ATP och laktat än de med lägre nivåer. Att tvinga organoider att producera mer PMM2 ökade KIFC3 och glykolys, medan minskad PMM2 gav motsatta effekter. Analys av patienttumörmatriser visade dessutom att höga nivåer av PMM2 var kopplade till mer avancerad sjukdom, spridning till lymfkörtlar och kortare överlevnad, vilket pekar på PMM2 som en stark kandidat till biomarkör.
Vad detta betyder för framtida vård
Enkelt uttryckt visar denna studie att många kolorektala tumörer tycks koppla in PMM2 i en nukleär proteinnedkoppling—via TRIM28 och E2F4—för att skruva upp KIFC3 och därigenom sin sockerförbränningsmaskin. Denna metaboliska uppsving hjälper cancrar att växa och sprida sig. Eftersom denna väg bygger på proteininteraktioner snarare än PMM2:s vanliga enzymuppgift öppnar det nya vägar för terapi: små molekyler, peptider eller degraderande läkemedel som stör PMM2:s bindning till TRIM28, blockerar E2F4:s åtkomst till DNA eller dämpar KIFC3-aktivitet kan i princip svälta tumörer på deras föredragna bränsle. Även om sådana behandlingar ännu inte finns tillgängliga framstår nu PMM2–TRIM28–E2F4–KIFC3-kedjan som en lovande karta för mer precisa och metabolt inriktade strategier mot kolorektal cancer.
Citering: Peng, Z., Ma, B., Song, Z. et al. PMM2 interacts with TRIM28 to recruit E2F4 and promote KIFC3-mediated tumor glycolysis and colorectal cancer progression. Oncogene 45, 1145–1160 (2026). https://doi.org/10.1038/s41388-026-03707-x
Nyckelord: kolorektal cancer, tumörmetabolism, glykolys, onkogen signalering, biomarkör