Clear Sky Science · sv
ULK1 främjar metastatisk progression i experimentella modeller av epitelial äggstockscancer
Varför denna forskning är viktig
Epitelial äggstockscancer upptäcks ofta först efter att den tyst spridit sig i buken, vilket gör den till en av de dödligaste cancerformerna som drabbar kvinnor. Ett avgörande steg i denna spridning är bildandet av små kluster av tumörceller, så kallade sfäroider, som flyter i bukvätska, överlever kemoterapi och gror nya tumörer. Denna studie ställer en fokuserad fråga med stora följder: hjälper en cellulär "överlevnadsknapp" kallad ULK1 dessa kluster att uthärda och sprida sig, och kan avstängning av den öppna nya behandlingsvägar för avancerad äggstockscancer?
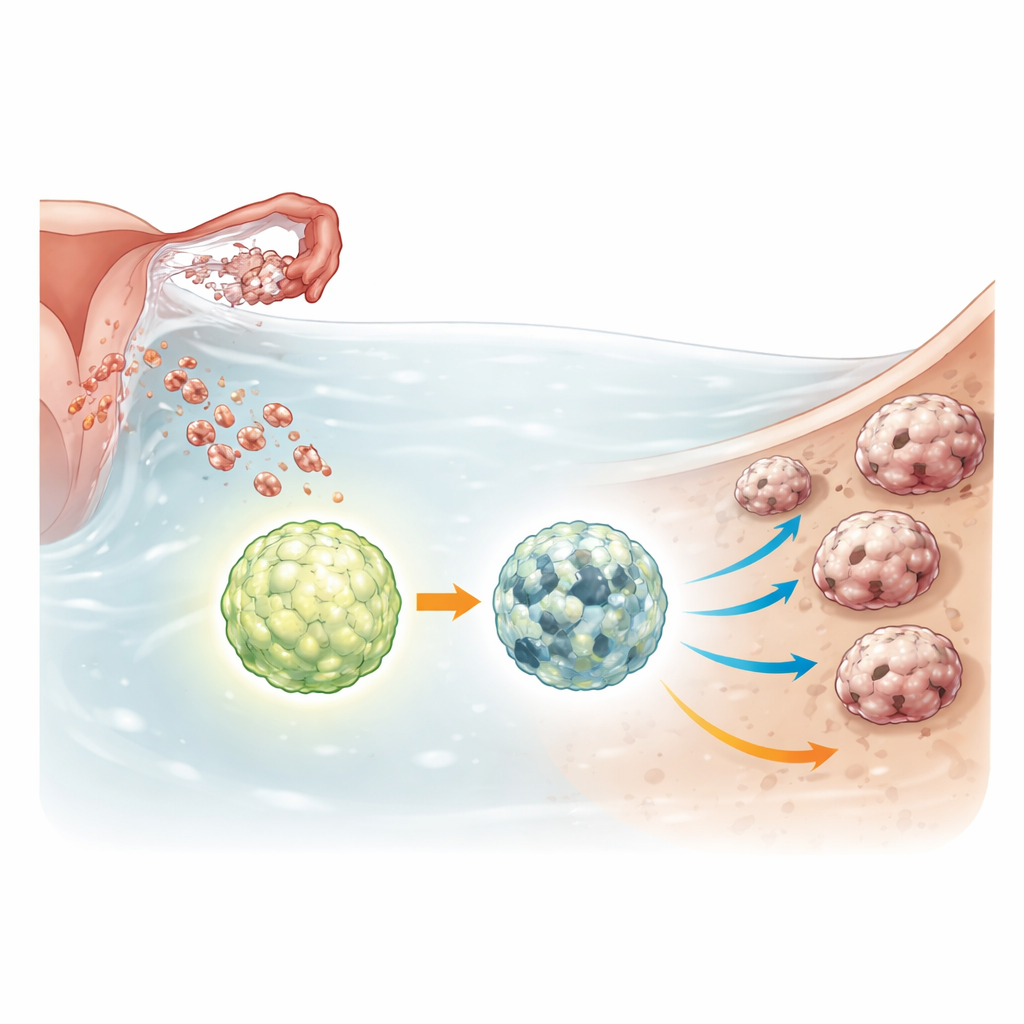
En överlevnadsknapp inne i cancercellskluster
Äggstockscancersfäroider klarar av hårda förhållanden: låg näring, bristande fäste och exponering för cytostatika. För att hantera detta ökar de en återvinningsprocess som kallas autofagi, som bryter ner och återanvänder interna komponenter för att hålla cellerna vid liv under stress. ULK1 är en huvudomkopplare som aktiverar detta återvinningssystem. Forskarna använde genredigering för att helt ta bort ULK1 i flera äggstockscancercellinjer och i en icke‑cancerogen cellinje från äggledaren som representerar tidiga, precancerösa stadier. De jämförde sedan hur normala och ULK1‑defekta celler betedde sig när de odlades som fritt flytande sfäroider eller som tredimensionella mini‑tumörer kallade organoider.
Vad som händer när knappen stängs av
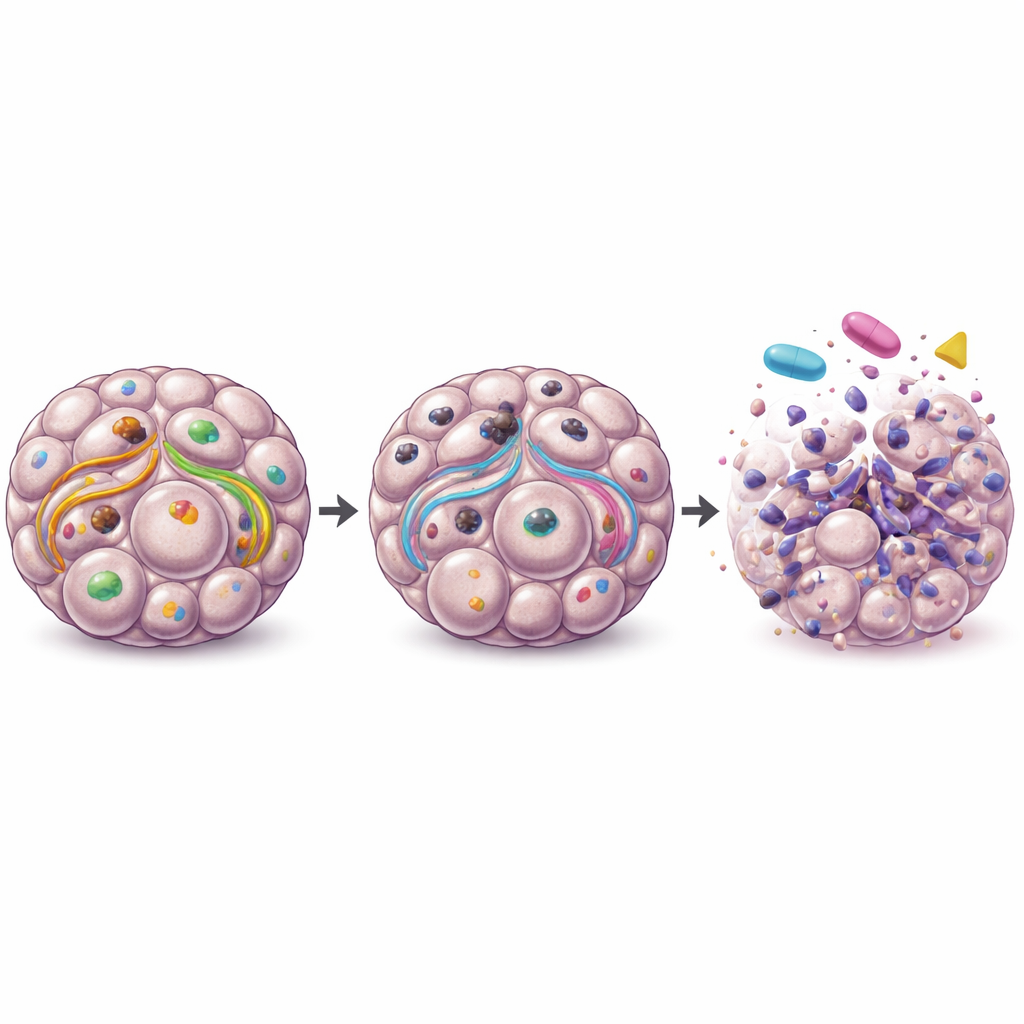
När ULK1 raderades i äggstockscancerceller försämrades deras förmåga att utföra autofagi i sfäroider kraftigt, vilket visades av förändringar i nyckelproteiner för återvinning. Dessa ULK1‑befriade sfäroider innehöll färre levande celler och visade ökade tecken på programmerad celldöd, vilket indikerar att cancercellsklusterna inte längre kunde stå emot stressiga förhållanden lika effektivt. Intressant nog stängde inte borttagandet av ULK1 ner återvinningssystemet i de icke‑cancerösa prekursorcellerna i samma grad, vilket tyder på att cancerceller är mer beroende av ULK1 än deras friska motsvarigheter. Detta cancerspecifika beroende gör ULK1 till ett attraktivt terapeutiskt mål.
Att sakta spridning och försvaga tumörutposter
Utöver överlevnad i suspension måste sfäroider fästa vid och invadera den släta beklädnaden i bukhålan för att bilda nya tumörer. Med hjälp av laboratoriemodeller som efterliknar detta tidiga metastassteg visade teamet att ULK1‑defekta sfäroider var avsevärt sämre på att tränga undan och invadera ett lager mesotelceller, som normalt täcker bukorganen. När de odlades som organoider inbäddade i en gel‑liknande matris bildade de cancerceller som saknade ULK1 också mindre och mindre robusta tumörstrukturer. I musmodeller där humana äggstockscancerceller injicerades i bukhålan ledde förlust av ULK1 till färre tumörinsättningar och mindre vätskeansamling, båda kännetecken för avancerad sjukdom, även om djurens övergripande överlevnad inte förbättrades.
Försvagning av nyckelsignaler och ökad effekt av riktade läkemedel
För att förstå hur ULK1 stödjer cancer utöver autofagi kartlade forskarna proteinförändringar i sfäroider utan ULK1. De fann att större tillväxt‑ och överlevnadsleder i cellen—särskilt MEK–MAPK‑ och PI3K–AKT–mTOR‑vägarna—påverkades. Dessa vägar hjälper normalt cancerceller att motstå död och fortsätta dela sig. När teamet behandlade ULK1‑defekta sfäroider med läkemedel som blockerar MEK eller mTOR blev cancercellsklusterna mycket mer sårbara, med kraftigt minskad livsduglighet och förmåga att återfästa. Däremot gjorde inte borttagandet av ULK1 standardkemoterapier som karboplatin, paklitaxel eller PARP‑inhibitorn olaparib mer effektiva, och under vissa förhållanden tycktes det dämpa deras nytta.
Ledtrådar från patienttumörer och mini‑patientmodeller
Vid granskning av stora publika dataset över äggstockstumörer fann författarna att högre ULK1‑genaktivitet var kopplad till sämre långsiktig överlevnad och var särskilt förhöjd i metastatiska prover jämfört med primära tumörer och normal vävnad. För att komma närmare klinisk tillämpning testade de en klinisk ULK1‑hämmare i tablettform, DCC‑3116, på patient‑härledda organoider odlade från metastatiska tumörprover. I en delmängd av dessa patientmodeller minskade blockering av ULK1 ensam, eller användning av MEK‑ eller mTOR‑läkemedel ensamt, organoidernas överlevnad, även om kombinationer av dessa ämnen inte konsekvent gav ytterligare nytta. Andra patientorganoider var resistenta mot alla behandlingar, vilket understryker hur varierande äggstockscancer kan vara och behovet av biomarkörer för att identifiera vilka som kan dra nytta.
Vad detta innebär för framtida vård
Tillsammans målar fynden upp ULK1 som en central medhjälpare i äggstockscancerns spridning: den driver den interna återvinningen som håller sfäroidkluster vid liv, stödjer deras förmåga att invadera nya platser och hjälper till att bibehålla starka tillväxtsignaler. Att stänga av ULK1 försvagar dessa processer, krymper experimentella tumörer och gör cancercellskluster mer känsliga för vissa riktade läkemedel, men inte för standardkemoterapi. För patienter antyder detta att ULK1 skulle kunna bli en del av en precisionsmedicinsk strategi—särskilt för dem med ULK1‑hög, metastatisk sjukdom—där målinriktade ULK1‑hämmare kombineras med MEK‑ eller mTOR‑blockerare för att begränsa tumörtillväxt och spridning, förutsatt att noggranna tester kan identifiera vilka tumörer som sannolikt svarar.
Citering: Webb, J.D., Buensuceso, A., Tomas, E.J. et al. ULK1 promotes metastatic progression in experimental models of epithelial ovarian cancer. Oncogene 45, 1111–1127 (2026). https://doi.org/10.1038/s41388-026-03702-2
Nyckelord: äggstockscancer, metastas, autofagi, ULK1, målstyrd terapi