Clear Sky Science · sv
Modellering av korssnack mellan fettvävnad och cancer: ett tredimensionellt perspektiv
Varför fett och cancer är närmare varandra än du tror
De flesta av oss ser kroppsfett som extra vaddering eller lagrad energi, men forskningen visar nu att det är ett aktivt, kommunikativt organ som kan påverka vår hälsa på oväntade sätt. Denna översiktsartikel undersöker hur fettvävnad och cancerceller kommunicerar, och hur nya tredimensionella (3D) laboratoriemodeller hjälper forskare att efterlikna den dialogen mer realistiskt än någonsin. Att förstå denna dolda konversation kan förbättra cancerförebyggande åtgärder, läkemedelstestning och behandlingar, särskilt i en värld där övervikt blir allt vanligare. 
Fett som ett levande, talande organ
Adipös vävnad—vårt kroppsfett—är inte bara en passiv lagringsplats. Det är ett komplext organ bestående av fettceller, immunceller, blodkärl och stödjeceller, alla inbäddade i ett strukturellt nätverk kallat extracellulär matrix. Olika typer av fett finns på olika platser: subkutant fett under huden, visceralt fett runt inre organ och vita, bruna och beige fettceller som varierar i hur de lagrar energi eller förbränner den som värme. Dessa celler avger ständigt en blandning av hormoner, fettsyror och signalproteiner som påverkar metabolism, inflammation och, som vi nu vet, cancerrisk och tumörernas beteende.
Fetma, inflammation och cancerrisk
När vi går upp för mycket i vikt växer vita fettceller i storlek och antal och vävnaden blir stressad och inflammerad. Detta ”ohälsosamma” fett frigör fler inflammatoriska molekyler och fettsyror till blodomloppet, samtidigt som hanteringen av socker och fett blir mindre effektiv. Stora epidemiologiska studier har kopplat fetma till ökad risk och sämre utfall för många cancerformer, inklusive bröst-, tjocktarms-, pankreas- och livmodercancer. Översikten förklarar hur dysfunktionellt fett kan mata tumörer med extra bränsle, göra den omgivande vävnaden styvare och rekrytera andra celltyper som tillsammans skapar en mer cancervänlig miljö.
En tvåvägskommunikation mellan fett och tumörer
Cancer ses numera som en sjukdom i ett helt ekosystem, inte bara som avvikande celler. Tumörceller utnyttjar närliggande fett för stöd och omprogrammerar fettceller, immunceller och fibroblaster för att hjälpa dem att växa och sprida sig. Som motreaktion bryter fettceller ner lagrade lipider och frigör fettsyror och hormoner som cancerceller lätt kan använda. Denna korssignalering kan ske via cirkulerande signaler på avstånd eller lokalt där tumörer växer intill fett, som i bröst eller buk. Tumörceller kan till och med få fettceller att förlora sin ursprungliga identitet och bli mer likt ärrbildande eller immuncellslika celler som omformar vävnaden och främjar invasion. 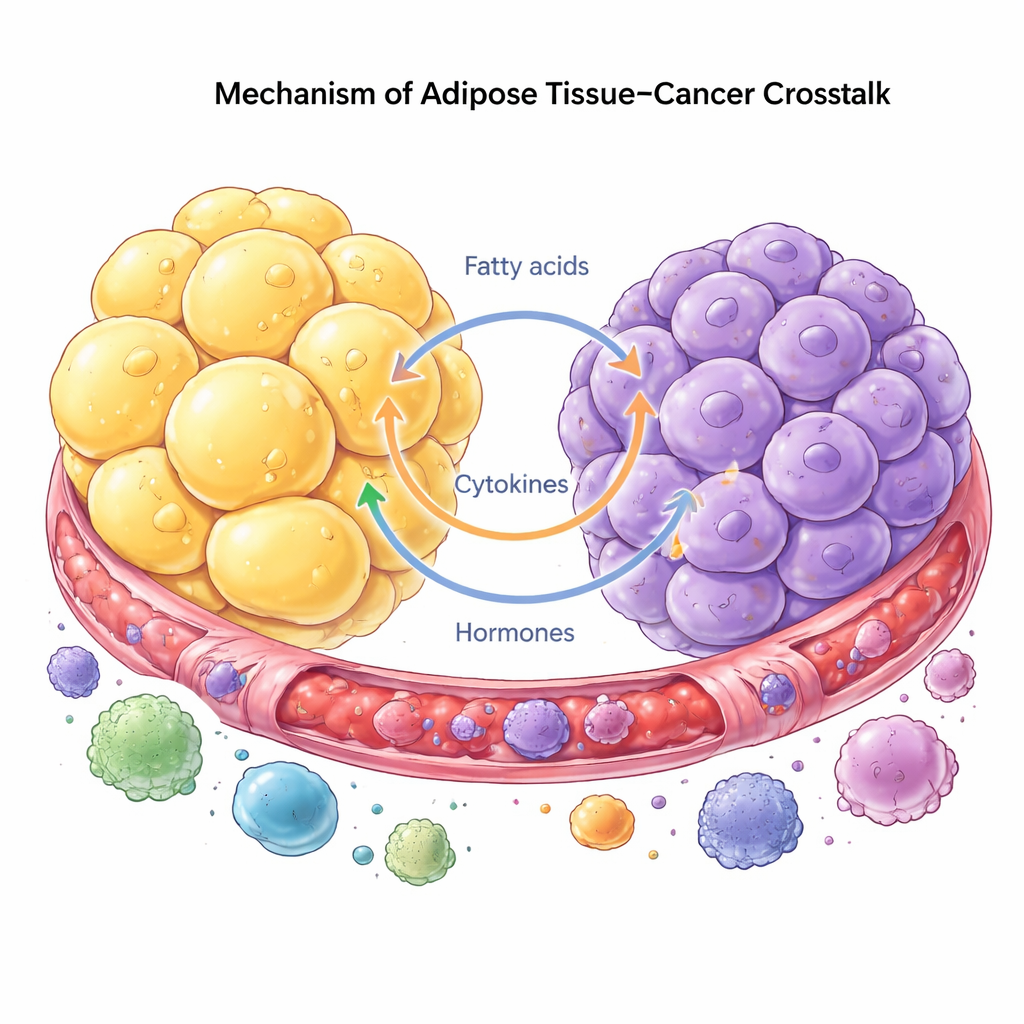
Bygga mini-vävnader i 3D
Traditionella platta (2D) cellkulturer och djurmodeller fångar ofta inte dessa komplexa interaktioner. Författarna beskriver en ny generation 3D-system som bättre liknar verklig vävnad. Spheroider är enkla cellkluster som självorganiserar till små sfärer; ställningar (scaffolds) är konstruerade material som ger ett 3D-stöd för celler att växa på; organoider är miniatyrer av vävnader som självorganiserar; och assembloider kombinerar flera organoider eller spheroider till sammansatta ”mini-organ”. Forskare använder nu dessa 3D-ansatser för att samekultivera fettceller och cancerceller, studera hur fetmaliknande förhållanden förändrar deras beteende och testa hur läkemedel kan bryta den skadliga dialogen mellan dem.
Löften och nuvarande brister
Varje modell har avvägningar. Spheroider är billiga och lämpade för hög genomströmning men relativt enkla. Ställningar tillåter noggrann kontroll av fysiska egenskaper såsom styvhet, vilket kan påverka cancerspridning, men är mer tekniskt krävande. Organoider och assembloider fångar den högsta nivån av realism med flera interagerande celltyper, men de är kostsamma, svåra att standardisera och saknar ofta fullständiga nätverk av blodkärl eller immunkomponenter. Översikten betonar att dagens system fortfarande inte fullt ut reproducerar mänsklig fett- och tumörvävnad, särskilt när det gäller att återskapa hela extracellulära matrixen, mogna fettceller och immuncellernas deltagande.
Vart forskningen är på väg
Författarna konkluderar att förbättrade 3D-modeller av fett–cancer-interaktioner är avgörande för mer träffsäker läkemedelstestning och för att förstå hur fetma främjar cancer. Allt eftersom dessa ”mini-vävnader” blir mer livlika—med realistiskt fett, tumörceller, blodkärl och immunceller—kan de hjälpa forskare att förutsäga vilka behandlingar som fungerar för specifika patienter, utforma bättre strategier för att hindra att cancer använder kroppsfett som bränsle och i slutändan vägleda terapier som riktar sig inte bara mot tumörer utan också mot de ohälsosamma miljöer som hjälper dem att frodas.
Citering: Strusi, G., Suelzu, C.M. & Stebbing, J. Modelling adipose tissue-cancer crosstalk: a three-dimensional perspective. Oncogene 45, 905–913 (2026). https://doi.org/10.1038/s41388-026-03697-w
Nyckelord: fettvävnad, fetma, cancermiljö, 3D-cellodling, tumörmetabolism