Clear Sky Science · sv
POM121 O-GlcNAcylation underlättar skelettmetastasering vid icke-småcellig lungcancer genom ökad c-MYC-nukleär import och ECM-omprogrammering
Varför denna forskning är viktig
När lungcancer sprider sig till skelettet orsakar det svåra smärtor, frakturer och en markant försämrad överlevnad, men läkare har fortfarande få verktyg för att stoppa detta dödliga steg. Denna studie undersöker det inre maskineriet i lungcancerceller för att ta reda på hur vissa av dem får en särskild fördel som gör att de kan färdas från lungan till ben och trivas där. Genom att följa processen ända ner till små förändringar på ett enda grindvaktsprotein i kanten av cellkärnan identifierar författarna en ny händelsekedja som kan vara en måltavla för att bättre förutsäga, förebygga eller behandla skelettmetastaser hos patienter med icke-småcellig lungcancer.
En sockermärkning som förändrar cancerbeteendet
Forskningen fokuserade på posttranslationella modifieringar, små kemiska förändringar som proteiner får efter att de syntetiserats. En sådan förändring, kallad O-GlcNAcylation, innebär att en liten sockerenhet fästs vid specifika ställen på proteiner. Med hjälp av lungcancercellinjer och musmodeller jämförde teamet vanliga tumörceller med underpopulationer som upprepade gånger selekterats för sin förmåga att kolonisera ben. De fann att dessa ben-sökande celler hade mycket högre nivåer av O-GlcNAcylation, drivet av ökad aktivitet hos enzymet OGT, som fäster sockret. Bland hundratals modifierade proteiner utmärkte sig ett: POM121, en kärnkomponent i kärnporkan, strukturen som styr trafiken in och ut ur cellkärnan.
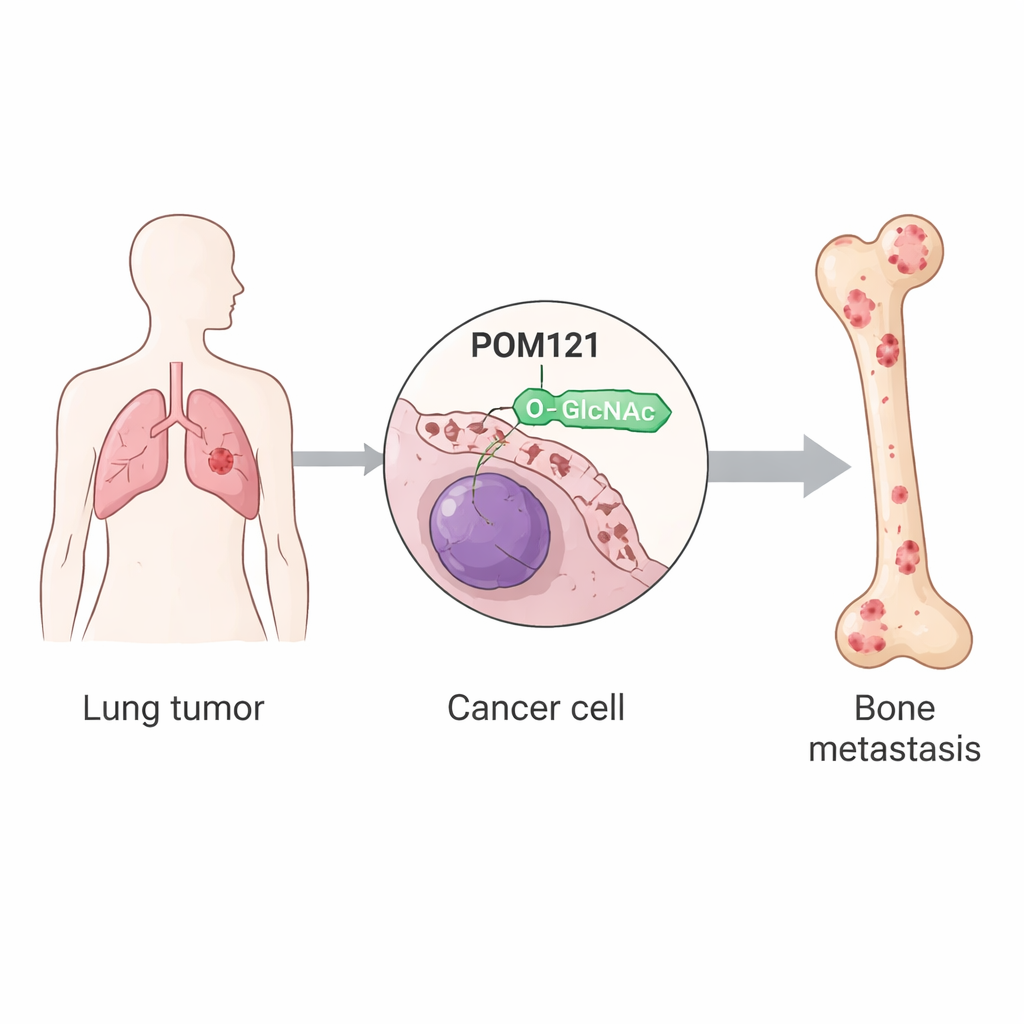
Den nukleära grindvakten POM121 stabiliseras
POM121 sitter i membranet runt kärnan och utgör en del av kanalen som många signalproteiner måste passera. I benmetastaserande lungcancerceller bar POM121 en tung last av O-GlcNAc vid en enda aminosyras position kallad serin 199. När denna plats förändrades så att den inte längre kunde modifieras blev proteinet instabilt och bröts snabbt ner av cellens avfallshanteringssystem. Studien visar att sockret skyddar POM121 från att märkas för nedbrytning av ett enzym kallat TRIM21, som normalt fäster ubiquitin—”bortforslings”-etiketter. Med O-GlcNAc på plats kan TRIM21 inte binda väl, ubiquitinering minskar och POM121 ackumuleras vid kärnporkan utan att ändra sin lokalisering.
Öppnar dörren för en kraftfull cancerdrivare
Vilken skillnad gör ett extra stabilt POM121? Nyckeln ligger i ett välkänt cancerfrämjande protein, transkriptionsfaktorn c-MYC. c-MYC måste ta sig in i kärnan för att slå på gener, men dess passage beror på kärnporkomponenter som POM121. Författarna visade att när POM121 var rikligt förekommande och O-GlcNAcylaterat fanns mer c-MYC inne i kärnan; när POM121-nivåerna minskades eller dess sockermärkning togs bort sjönk c-MYC:s nukleära import kraftigt. I möss bildade lungcancerceller som bar den icke-modifierbara POM121-mutanten långt färre och mindre skelettmetastaser, medan återställande av c-MYC i POM121-deficienta celler återupplivade mycket av deras förmåga att kolonisera ben. Detta placerar POM121 uppströms om c-MYC i en kritisk metastatisk bana.
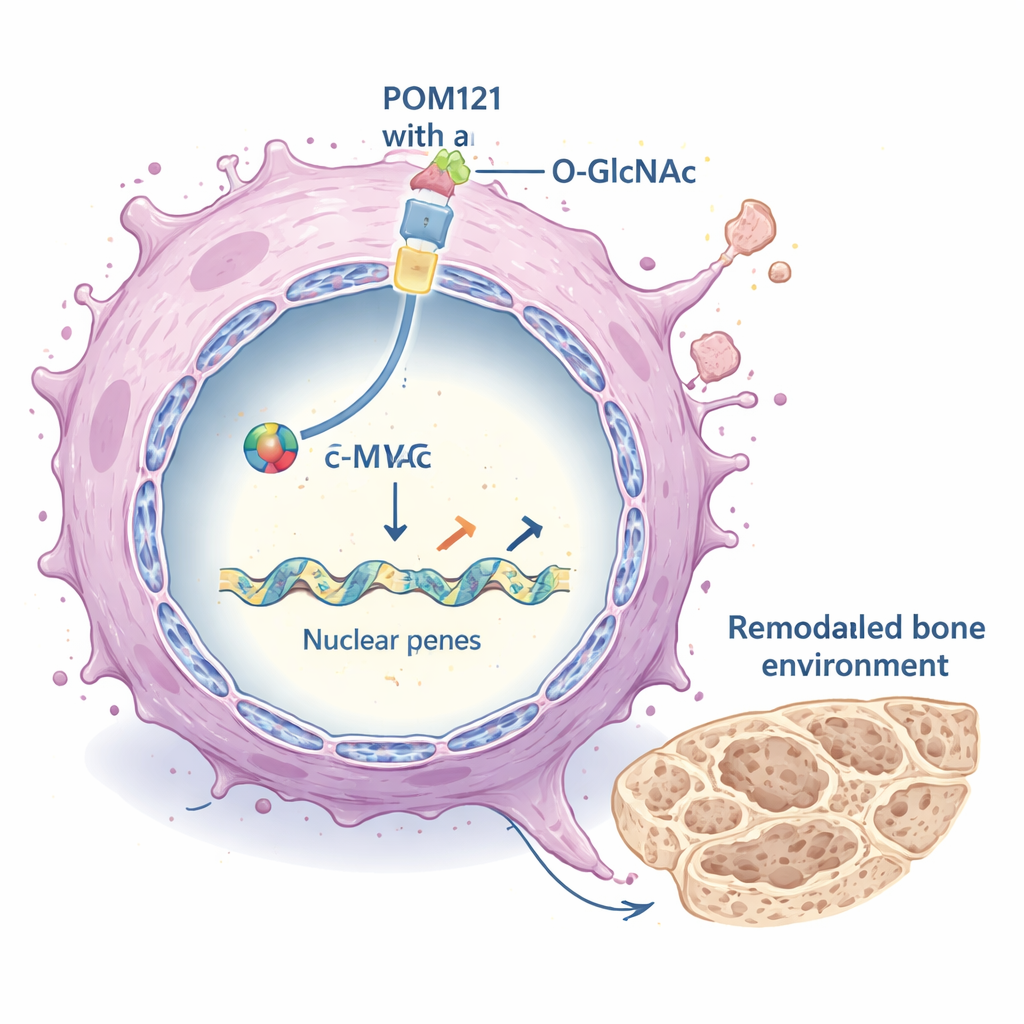
Omkoppling av tumörens omgivning
När c-MYC väl är inne i kärnan fungerar det som en huvudströmbrytare för många gener. Här visade det sig kraftigt aktivera en uppsättning gener som formar den extracellulära matrisen (ECM) – skelettet av proteiner runt cellerna. Dessa ECM-gener, som inkluderar olika kollagener och enzymer som omstrukturerar vävnad, nedreglerades när POM121 eller c-MYC blockerades och uppreglerades när O-GlcNAcylation och POM121 var höga. Den ändrade ECM förstärkte i sin tur stora tillväxtvägar inne i cancercellerna, särskilt PI3K–AKT–mTOR-signaleringen, som stödjer överlevnad, tillväxt och spridning. Liknande mönster observerades i flera olika lungcancermodeller, vilket tyder på att denna mekanism inte är begränsad till en enskild cellinje.
Från laboratoriefynd till patientpåverkan
I patientdata fann forskarna att höga nivåer av OGT, POM121 och c-MYC, samt de ECM-gener de reglerar, var kopplade till sämre utfall och till lungtumörer som redan spridit sig till ben. Tillsammans skisserar arbetet en OGT–POM121–c-MYC–ECM-axel: ökad O-GlcNAcylation stabiliserar den nukleära grindvakten POM121, som för in mer c-MYC i kärnan, vilket i sin tur omprogrammerar vävnadens stomme och tillväxtsignaler för att gynna skelettmetastasering. För patienter antyder detta nya typer av biomarkörer för att identifiera dem i riskzonen för bennyckelspridning, och nya terapeutiska angreppssätt — från att blockera OGT eller POM121-funktion till att dämpa c-MYC eller ECM-ombyggnad — som en dag skulle kunna hjälpa till att hålla lungcancer borta från skelettet.
Citering: Ren, YZ., Zhao, MN., Du, FL. et al. POM121 O-GlcNAcylation facilitates bone metastasis in non-small cell lung cancer through enhanced c-MYC nuclear import and ECM reprogramming. Oncogene 45, 728–743 (2026). https://doi.org/10.1038/s41388-026-03687-y
Nyckelord: lungcancer skelettmetastaser, POM121, O-GlcNAcylation, c-MYC, extracellulär matrix