Clear Sky Science · sv
Sortilin uppvisar tumörsuppressorliknande aktivitet genom att begränsa EGFR:s transduktionsfunktion
Varför detta är viktigt för cancerbehandling
Lungcancer är den vanligaste orsaken till cancerrelaterade dödsfall i världen, och många moderna läkemedel riktar sig mot ett molekylärt måltavla som kallas EGFR som driver tumörtillväxt. Dessa läkemedel fungerar ofta bra inledningsvis, men tumörer blir ofta snabbt resistenta. Denna studie avslöjar en naturlig ”broms” inne i lungcancerceller — en oväntad roll för ett protein kallat sortilin — som kan dämpa EGFR:s cancerfrämjande signaler. Att förstå denna relation kan hjälpa till att förklara varför vissa patienter svarar bättre på EGFR‑inriktade behandlingar och föreslå nya sätt att få dessa behandlingar att fungera längre. 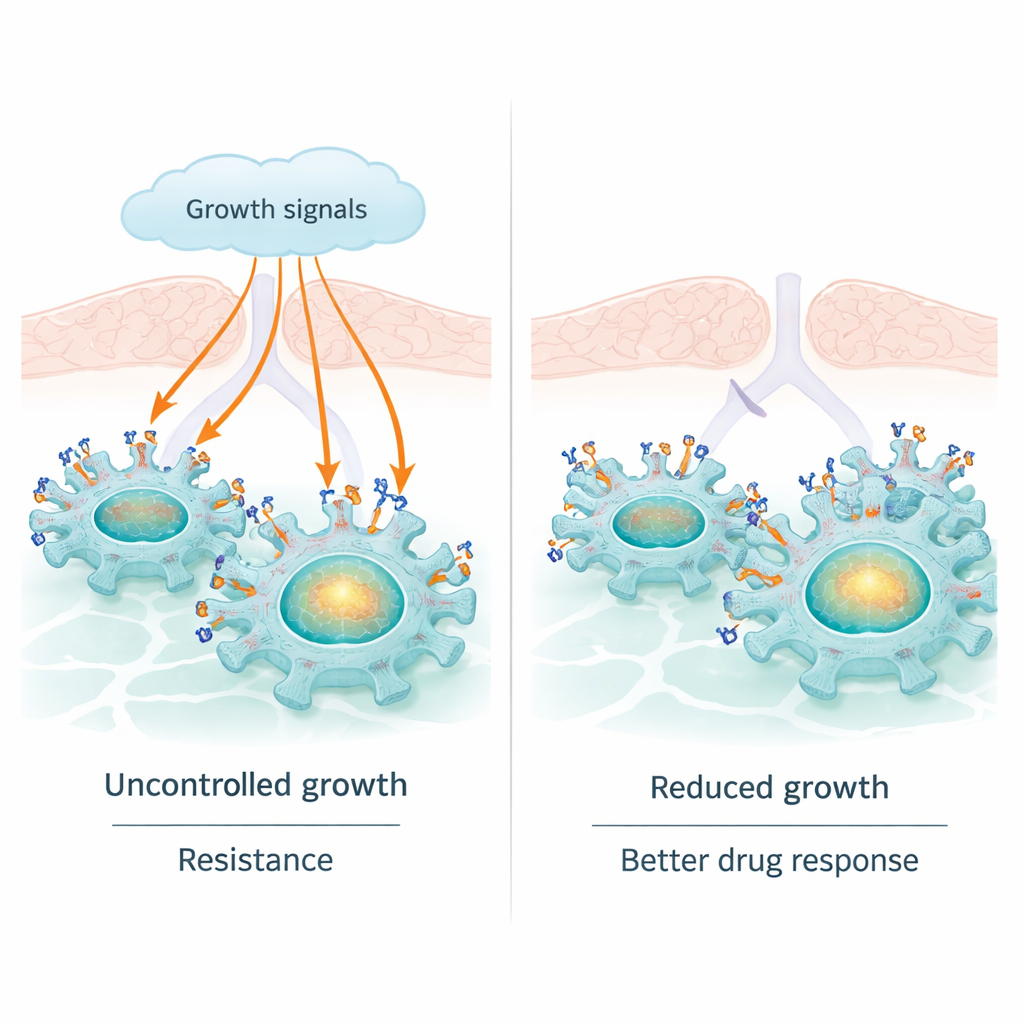
En tillväxtomkopplare ur kontroll
EGFR är en receptor på ytan av många celler som känner av tillväxtsignaler från omgivningen. I en stor andel av lungadenocarcinom är EGFR förändrat så att det är permanent aktiverat. Det driver ständig tillväxt och delning, och det är därför EGFR‑blockerande tabletter, så kallade tyrosinkinashämmare, kan krympa tumörer. Men EGFR har också en mindre uppskattad funktion: det kan vandra in i cellkärnan och verka direkt på DNA, och slå på gener som cMYC och CCND1 som ytterligare ökar tillväxt, överlevnad och behandlingsresistens. Denna nukleära roll för EGFR kan hjälpa tumörer att undkomma även när dess ytfunktion kemiskt blockeras.
Sortilin följer med in i kärnan
Sortilin var tidigare främst känd som ett sorteringsprotein som hjälper till att ta in EGFR från cellmembranet och leda det mot nedbrytning, vilket försvagar dess tillväxtsignaler. I detta arbete visar författarna att sortilin också följer EGFR in i kärnan när lungcancerceller stimuleras. Med hjälp av högupplöst mikroskopi och biokemisk fraktionering observerade de komplex av EGFR och sortilin som bildas inne i kärnorna strax efter aktivering. Viktigt är att när EGFR inte kunde gå in i kärnan, höll sig sortilin också utanför, vilket indikerar att EGFR fungerar som sortilins ”biljett” in i detta kompartment. Väl där hittades EGFR–sortilin‑komplex bundna till DNA‑sträckor nära startpunkterna för viktiga tillväxtreglerande gener, inklusive cMYC och CCND1.
En inbyggd broms på cancergener
För att förstå vad dessa komplex gör kartlade forskarna deras bindning över genomet och mätte förändringar i genaktivitet. De fann att EGFR ensam tenderar att främja aktivering av tillväxtrelaterade gener, medan närvaro av sortilin vid samma DNA‑regioner dämpar denna effekt. När sortilinnivåerna artificiellt sänktes ökade EGFR‑bindningen vid target‑gener, och cancergener som cMYC och CCND1 blev mer aktiva. I kontrast gav en ökning av sortilin motsatt effekt: EGFR:s grepp om DNA försvagades, rekryteringen av transkriptionsmaskineriet minskade och uttrycket av dessa onkogena gener föll. I musmodeller växte lungtumörer som konstruerats för att överproducera sortilin långsammare och visade minskade nivåer av cMYC och CCND1. 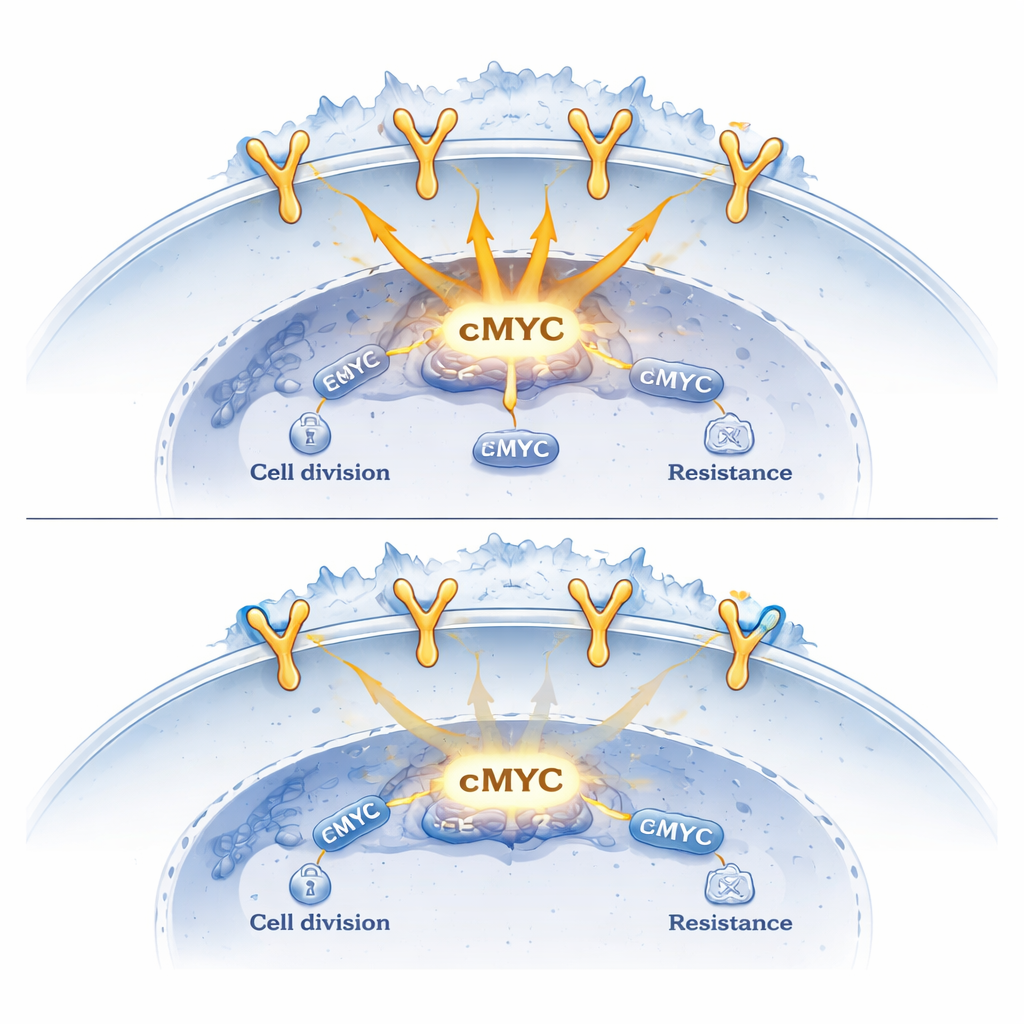
Samverkan med EGFR‑läkemedel
Studien undersökte också hur denna mekanism interagerar med osimertinib, ett mycket använt EGFR‑inriktat läkemedel utformat för att blockera problematiska EGFR‑mutationer. Överraskande nog, även när osimertinib stängde ner EGFR:s enzymatiska aktivitet, fortsatte receptorn att förflytta sig in i kärnan. Där fortsatte den att binda DNA, särskilt i närheten av cMYC‑genen. Sortilin ackumulerades dock också i kärnan under dessa förhållanden. När sortilin var rikligt minskade cMYC‑nivåerna kraftigare som svar på osimertinib, och cancercellerna blev mindre livskraftiga. Analys av patienttumörer och stora offentliga cancer‑databaser visade att sortilinnivåer ofta är lägre i lungadenocarcinom än i normalt lungvävnad, och att högre sortilinuttryck konsekvent är kopplat till lägre cMYC‑uttryck.
Vad detta betyder för patienter
Sammantaget målar fynden upp sortilin som en slags tumörsuppressorliknande partner som åker med EGFR in i kärnan och sedan begränsar dess aktivitet. Genom att begränsa EGFR:s förmåga att slå på kraftfulla tillväxtgener som cMYC kan sortilin bromsa tumörprogression och öka effekten av EGFR‑blockerande läkemedel. Eftersom många lungtumörer har reducerad sortilin kan de sakna denna interna broms, vilket kan förklara varför vissa cancerformer är särskilt aggressiva eller snabbt blir läkemedelsresistenta. Att mäta sortilinnivåer i tumörer kan hjälpa till att förutsäga hur väl en patient kommer att svara på EGFR‑inriktade behandlingar, och strategier som ökar sortilinaktivitet kan erbjuda ett nytt sätt att hålla EGFR‑drivna cancerformer bättre under långsiktig kontroll.
Citering: Lapeyronnie, E., Granet, C., Tricard, J. et al. Sortilin exhibits tumor suppressor-like activity by limiting EGFR transduction function. Oncogene 45, 875–888 (2026). https://doi.org/10.1038/s41388-026-03680-5
Nyckelord: lungcancer, EGFR, sortilin, cMYC, resistens mot målinriktad behandling