Clear Sky Science · sv
Kaskadisk inertial mikrofluidik för höggenomströmning och flerskalig berikning av tumörceller och intakta kluster för förbättrad malignitetsdiagnostik
Varför det spelar roll att sortera cancerceller i vätska
När cancer sprider sig kan tumörceller ofta lämna tumören och hamna i de vätskor som omger våra organ. Hos personer med lungcancer kan detta omfatta vätska som samlas runt lungorna, kallad pleuravätska. Dold i denna vätska finns sällsynta enskilda tumörceller och täta cellkluster. Dessa kluster anses särskilt farliga eftersom de är starkt kopplade till aggressiv sjukdom och sämre utfall. Nuvarande laboratoriemetoder har dock svårt att skonsamt och effektivt plocka ut både enskilda celler och kluster ur stora volymer patientvätska. I denna studie presenteras en ny chipbaserad teknik som snabbt och varsamt kan sortera dessa celler från pleuravätska, vilket öppnar för mer tillförlitlig cancerdiagnostik och bättre insikt i hur tumörer sprider sig.
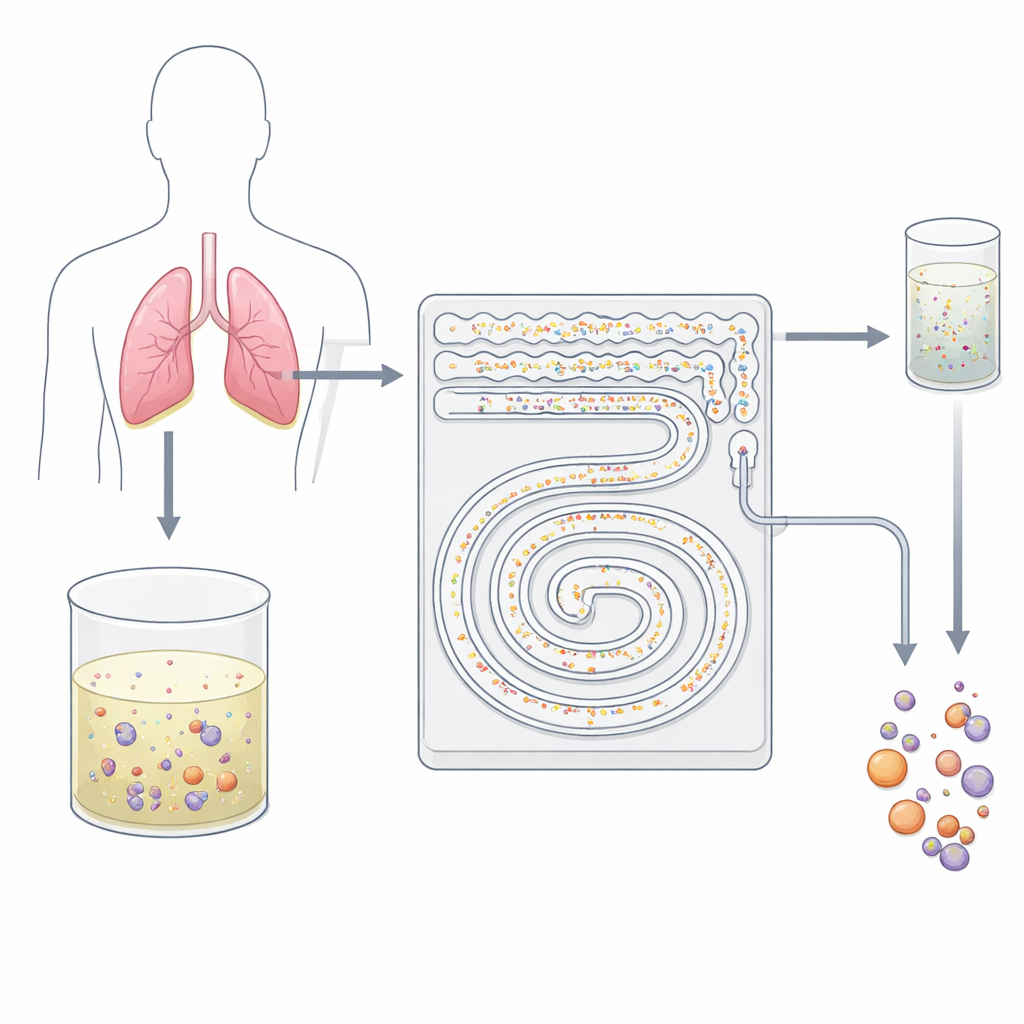
En skonsam cellsil på en chip
Forskarna utvecklade en handflatesstor plastanordning med inristade mikroskopiska kanaler som fungerar som ett smart, tvåstegsfilter. Istället för att använda klibbiga antikroppar eller hårdhänt sållning förlitar sig chippet på hur celler beter sig i snabbflytande vätska. När vätska rusar genom kurvade mikrokanaler pressar osynliga krafter partiklar av olika storlek in i olika strömlinjer. Gruppen utnyttjar denna effekt, allmänt kallad inertial mikrofluidik, för att skilja små bakgrundsblodceller från större tumörceller och deras kluster utan att röra vid eller markera dem. Eftersom allt sker i ett kontinuerligt, slutet flöde kan enheten hantera tiotals milliliter vätska på bara några minuter—något traditionell cytologi på preparatglas inte lätt klarar av.
Första steget: rensa bort mängden
I enhetens första stadium pumpas pleuravätskan—efter att överflödig vätska avlägsnats och cellerna suspenderats igen—genom ett fält av parallella serpentinkanaler. Här skjuter det virvlande, kurvade flödet de små vita blodkropparna mot kanalväggarna, medan större tumörceller och kluster håller sig nära mittstrålen. De små cellerna leds till avfallsluckor och tunnar därmed dramatiskt ut bakgrunden. Detta steg med hög genomströmning kan köras vid ungefär 8 milliliter per minut, vilket innebär att ett typiskt kliniskt prov på 50 milliliter kan bearbetas på cirka sex och en halv minut utan igensättning. Det som kommer ut från detta första steg är en mycket renare blandning, berikad på potentiellt maligna celler och redo för finare separation.
Andra steget: skilja enskilda celler från kluster
Det delvis berikade provet förs sedan in i en snedställd spiralformad kanal som innehåller ett upprepat mönster av smala och breda sektioner. I detta stadium balanserar flera flödeskrafter olika för objekt av olika storlek, vilket styr dem in i skilda banor nära den inre eller yttre väggen av spiralen. Enkelcells-lika tumörceller, som är mindre, radar upp sig på en lateral position, medan större kluster migrerar till en annan position närmare innerkanten. Genom att placera utlopp på rätt ställen delar chippet fysiskt upp dessa strömmar: ett utlopp samlar huvudsakligen enskilda tumörceller, ett annat samlar intakta kluster, och övriga utlopp tar bort kvarvarande småceller. Viktigt är att klustren förblir hela, vilket undviker den skada och sönderfall som ofta ses vid traditionell filtrering.
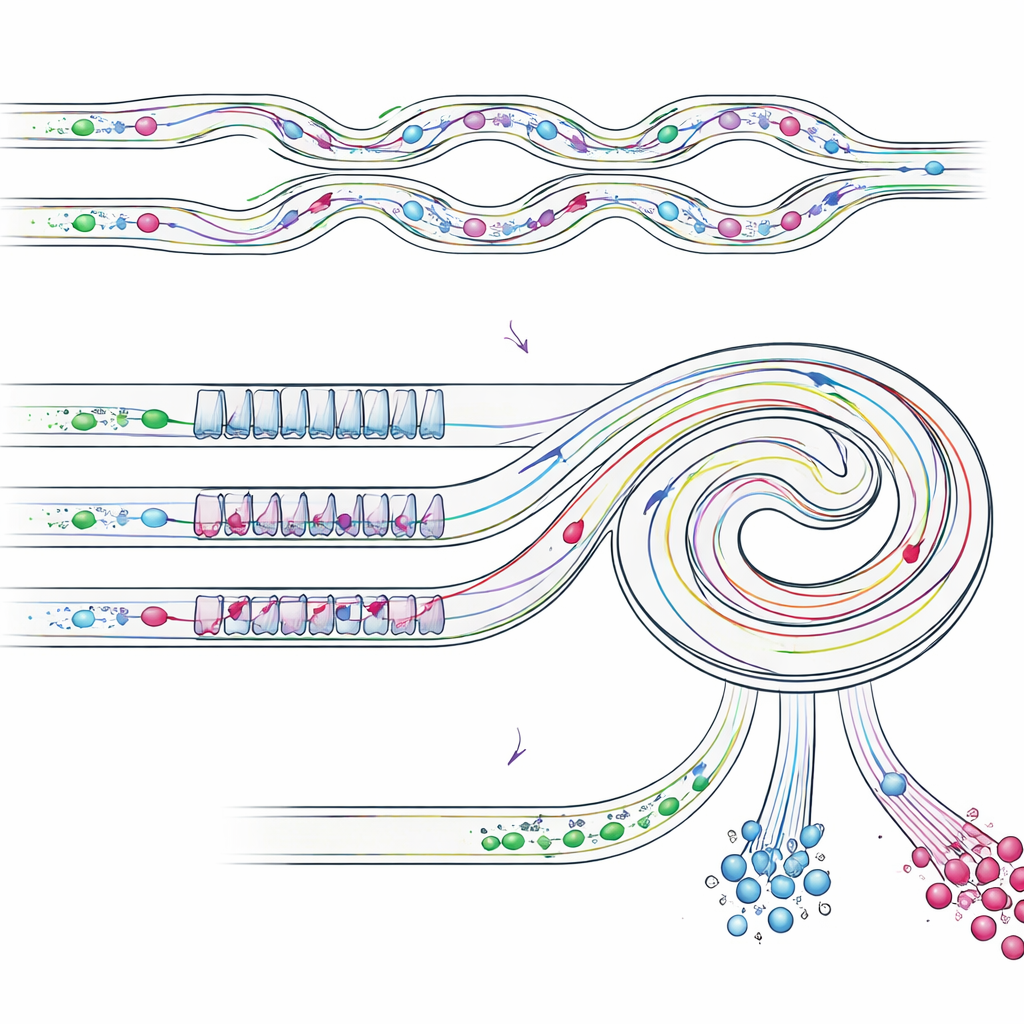
Sätta enheten på prov
För att kontrollera hur väl designen fungerade använde teamet först plastkulor med kända storlekar för att efterlikna blodceller, enskilda tumörceller och kluster. De visade att den kaskaderade chipen återvann mer än 87 % av “enskild-cell”-kulorna och cirka 92 % av “kluster”-kulorna, samtidigt som de avlägsnade de flesta mindre ”blodcell”-kulorna. De gick sedan vidare till riktiga lungcancerceller (A549-celler) blandade med vita blodkroppar. I dessa tester återvann enheten omkring 82 % av cancercellerna totalt, med ungefär 76 % renhet i den berikade fraktionen och nästan 80 % renhet för cellkluster. Slutligen bearbetade de faktiska pleuravätskeprover från tre lungcancerpatienter. Från vätska där tumörceller och kluster utgjorde mindre än 1 % av alla celler producerade chippet fraktioner där enskilda maligna celler uppgick till omkring 68 % av alla celler och där kluster utgjorde cirka 35 % av cellerna i en dedikerad utloppsström.
Vad detta kan betyda för patienter
Genom att endast använda vätskeflöde och kanalgeometri kan denna anordning snabbt och skonsamt plocka ut både enskilda tumörceller och intakta kluster ur stora volymer patientvätska utan kemiska markörer eller komplexa instrument. De berikade cellerna förblir lämpliga för standardtester som immunofluorescensfärgning och mikroskopi, vilket gör att tekniken smidigt kan integreras i befintliga sjukhusarbetsflöden. Även om den aktuella studien omfattade ett litet antal patienter och större prövningar behövs för att bevisa effekten på diagnos och prognos, visar arbetet ett kraftfullt koncept: en snabb, märk-fri “cellkoncentrator” som avslöjar både antalet och det klustrade tillståndet hos tumörceller i pleuravätskor. På längre sikt skulle sådana verktyg kunna skärpa bedömningen av malignitet, vägleda personliga behandlingsval och ge en klarare inblick i hur cancer metastaserar.
Citering: Zhu, Z., Ren, H., Zhang, Z. et al. Cascading inertial microfluidics for high-throughput, multi-scale enrichment of tumor cells and intact clusters towards enhanced malignancy diagnosis. Microsyst Nanoeng 12, 101 (2026). https://doi.org/10.1038/s41378-026-01235-y
Nyckelord: flytande biopsi, mikrofluidisk cellsortering, tumörcellskluster, pleuravätska, cancerdiagnostik