Clear Sky Science · sv
Design av ett automatiserat mikoinjektionssystem för cellpartier baserat på magnetiska pincetter för zebrafiskembryon
Varför små fiskägg är viktiga
Innan nya läkemedel eller genterapier når människor testar forskare dem ofta i små, snabbväxande djur. Zebrafiskembryon är populära eftersom de är genomskinliga och utvecklas snabbt, vilket gör att forskare kan följa organbildning i realtid. Men för att ändra deras gener eller leverera läkemedel måste varje ömtåligt ägg injiceras med en mikroskopisk nål, en uppgift som vanligtvis är långsam, utmattande och starkt beroende av mänsklig skicklighet. Denna artikel presenterar ett nytt robotsystem som automatiskt kan injicera partier av zebrafiskembryon snabbare, varsammare och mer pålitligt än en människa, vilket öppnar för större och mer konsekventa experiment.
Ett nytt sätt att hantera sköra celler
Traditionell mikroinjektion kräver en tränad operatör som styr en glasnål under ett mikroskop, hittar varje embryo, vrider det till rätt orientering och skär igenom utan att skada viktiga strukturer. Det är särskilt svårt eftersom embryon är mjuka sfärer med känsliga regioner som måste undvikas för att de ska överleva. Befintliga robotsystem har hjälpt till att automatisera transport och penetrering, men de kan vanligtvis inte kontrollera hur varje embryo roteras i tre dimensioner. Som ett resultat kan nålen komma in i en riskfylld vinkel, vilket minskar överlevnadsgraden och begränsar hur många embryon som pålitligt kan bearbetas. Teamet bakom denna studie satte målet att bygga en fullt integrerad plattform som kan transportera, rotera, injicera och släppa embryon i en smidig sekvens, utan ständiga objektivbyten eller manuella justeringar.
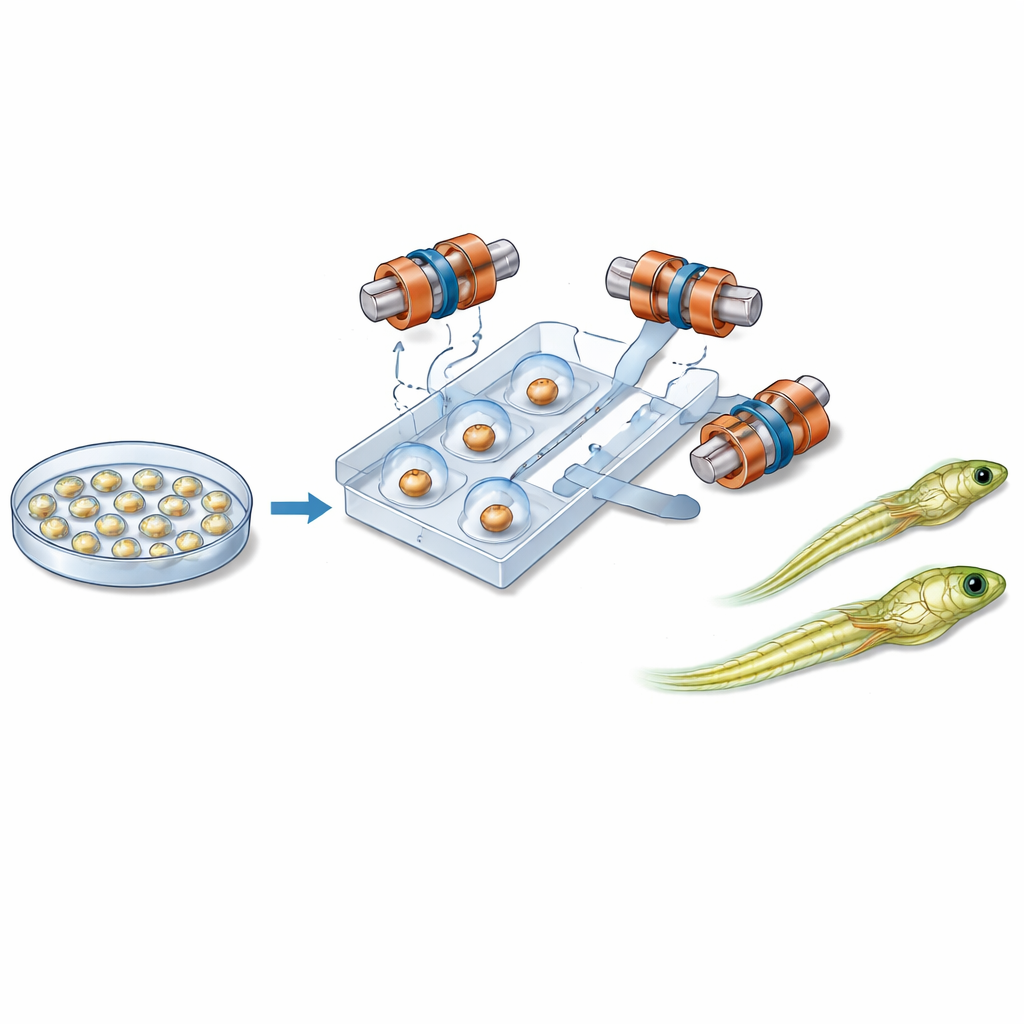
Magneter, mikrokanaler och varsam kontroll
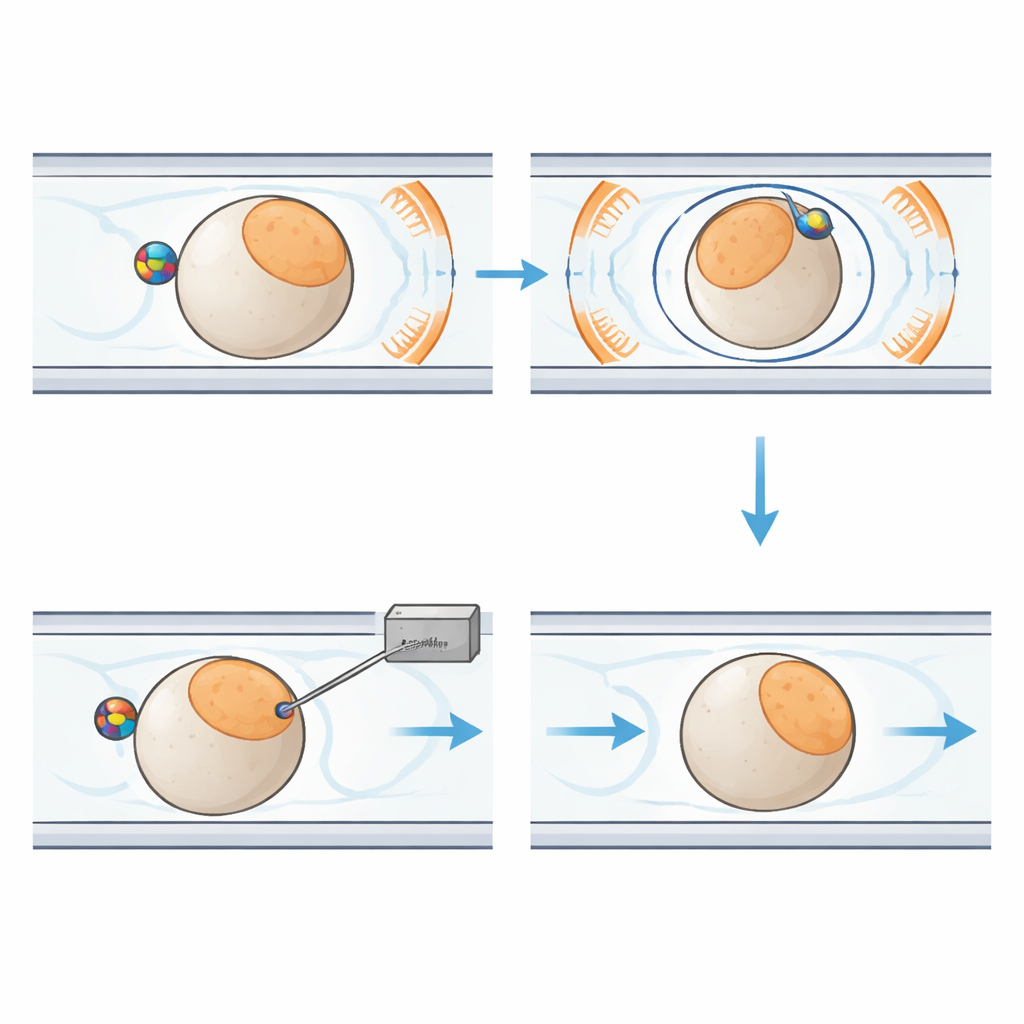
I kärnan av det nya systemet finns ett handflatesstort plastchip som innehåller smala kanaler som styr enskilda embryon längs en fast bana. Nära varje embryo sitter en liten magnetisk kula. Runt chippet genererar sex noggrant placerade spolar ett enhetligt magnetfält i tre dimensioner. Genom att ändra riktningen på detta fält över tiden får systemet kulan att rotera. Tack vare friktionen mellan kulan och embryots yta följer hela cellen med, som två ihopkopplade kugghjul. Detta gör det möjligt för roboten att vinkla embryot ut ur avbildningsplanet eller snurra det inom planet tills den känsliga regionen ligger tryggt bort från den inkommande nålen. Vätska och varsamt lufttryck förflyttar och håller embryon på plats, medan en separat modul kontrollerar injektionsnålen och den mycket små mängden genetiskt material.
Skarp sikt i ett litet synfält
För att möjliggöra denna precisa koreografi designade forskarna också ett avancerat datorvisionssystem, kallat microscopic manipulation perception network. Det analyserar bilder från ett mikroskopkamera i realtid för att hitta varje embryo, detektera den fina nålspetsen och skilja de två motsatta "polerna" på ägget där viktiga utvecklingsstrukturer ligger. Nätverket använder moderna djupinlärningstekniker—såsom dubbla funktionsutvinningsvägar, attention-moduler som framhäver viktiga detaljer och flerskalig fusion av bildinformation—för att hantera den röriga, svagt belysta världen inuti ett mikrofluidiskt chip. I tester på tusentals bilder upptäckte det objekt och segmenterade embryoområden med cirka 98–99% noggrannhet, vilket gav den pålitliga feedback som krävs för att styra både magnetisk rotation och nålpositionering.
Bevisa att det fungerar i levande zebrafisk
Teamet jämförde sitt automatiserade system med erfarna mänskliga operatörer och använde 100 zebrafiskembryon vardera. Roboten genomförde sina injektioner på cirka 33,8 sekunder per embryo, mer än dubbelt så snabbt som manuellt arbete, och punkterade framgångsrikt varje cell. Den orienterade även varje embryo med ett genomsnittligt vinkelavvikelse på endast 2,1 grader, ungefär hälften av människornas felmarginal. Viktigast var att 88% av de robotinjekterade embryona överlevde till utskolning som larver, jämfört med 66% efter manuell injektion. Under ett fluorescensmikroskop lyste larverna från det automatiserade systemet grönt, vilket visade att det införda genetiska materialet tagits upp och uttryckts som planerat. Genom att rotera embryon magnetiskt istället för att klämma dem med mekaniska verktyg minimerade systemet deformation och skada samtidigt som hög genomströmning bibehölls.
Vad detta betyder för framtida studier
Kort sagt visar detta arbete att en noggrant konstruerad kombination av mikrokanaler, magnetisk kontroll och smart bildanalys kan injicera sköra fiskembryon snabbare och med bättre överlevnad än en skicklig person med traditionella verktyg. Eftersom zebrafisk är en viktig modell för att studera utveckling, sjukdom och läkemedelseffekter kan en pålitlig injektor med hög genomströmning snabba upp stora genetiska screeningar och långsiktiga biologiska studier som tidigare hindrats av manuellt arbete. Med lämpliga designändringar av chippet och styrinställningar skulle samma strategi kunna anpassas till andra celltyper och små organismer, och hjälpa till att förvandla känslig cellulär kirurgi från en konst som utövas av några specialister till en automatiserad, standardiserad process.
Citering: Guo, X., Wang, F., Zhao, A. et al. Design of an automated cell batch microinjection system based on magnetic tweezers for zebrafish embryos. Microsyst Nanoeng 12, 113 (2026). https://doi.org/10.1038/s41378-026-01230-3
Nyckelord: zebrafiskembryon, mikroinjektion, magnetiska pincetter, mikrofluidik, robotisk cellmanipulation