Clear Sky Science · sv
Snabbtillverkad och kostnadseffektiv enskikts mikrofluidisk enhet för höggenomströmning tredimensionell hydrodynamisk fokusering
Varför det spelar roll att krympa små strömmar
Modern medicin förlitar sig i allt högre grad på att undersöka mycket stora mängder enskilda celler, till exempel för att upptäcka cancerceller i urin eller blod. För att göra detta snabbt och billigt skickas celler ofta genom hårtunna kanaler på mikrochip där laser eller kameror inspekterar dem. Men för att få skarpa, pålitliga bilder vid extrema hastigheter måste varje cell passera i nästan exakt samma lilla punkt. Denna artikel presenterar ett nytt sätt att bygga sådana chip så att de kan samla celler i en smal tredimensionell ström, även vid mycket höga hastigheter, med en enhet som är snabbare och billigare att tillverka än dagens standardlösningar.
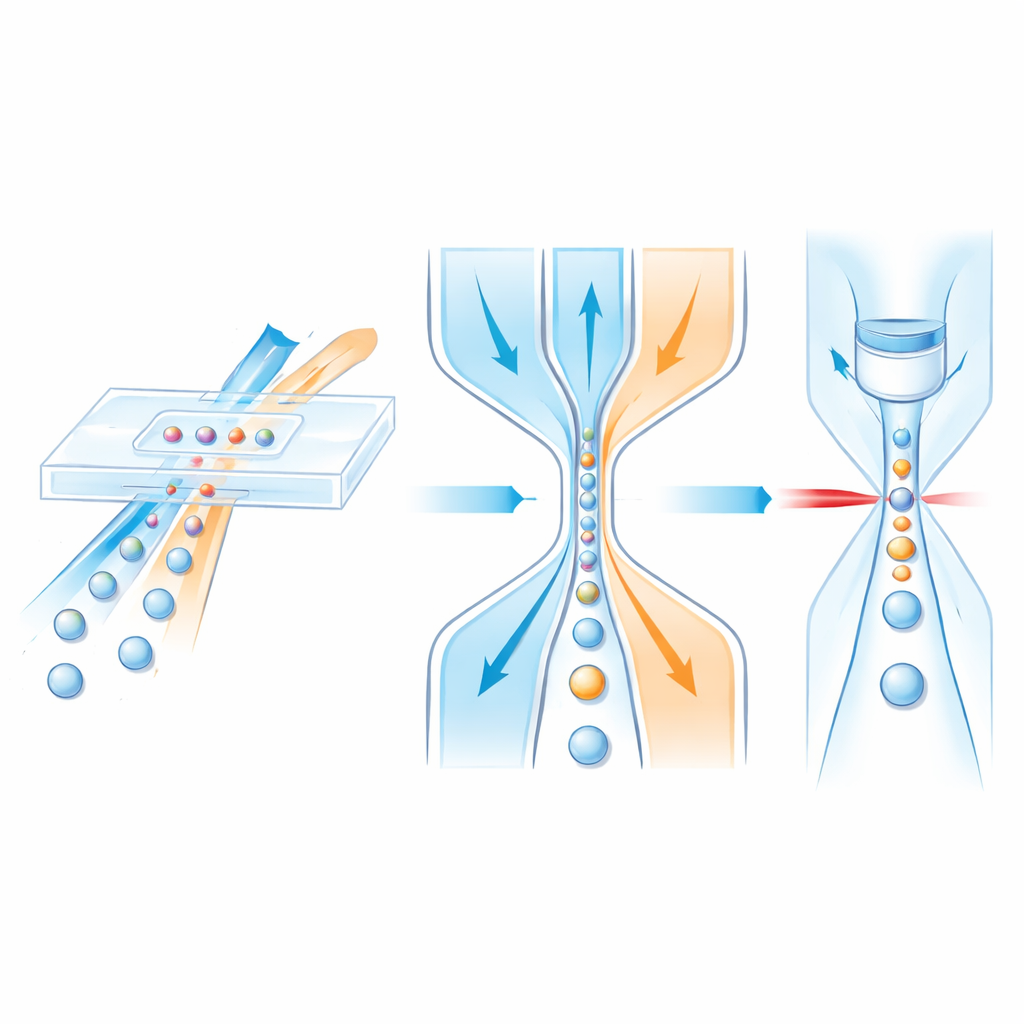
Vägleda celler med flytande "filbanor"
Inuti ett mikrofluidiskt chip färdas cellerna i en central vätskeström medan omgivande "skydds"-flöden fungerar som osynliga ledstänger och försiktigt pressar provet mot mitten. Tidigare konstruktioner kunde ofta bara fokusera celler sidledes, inte upp-och-ned, eller förlitade sig på komplexa flerskiktsstrukturer som är långsamma och dyra att tillverka. Författarna konstruerar istället en enskiktskanal som ändå uppnår full tredimensionell kontroll. Först ansluter provet till ett vertikalt skyddsflöde vid en vinklad T-formad förgrening som smalnar av längs sin längd. På grund av kanalens form och vätskornas tröghet vid högre hastigheter trycks provströmmen mot kanalens övre halva. Därefter klämmer två matchande sidokåpor längre nedströms från vänster och höger och pressar det redan upplyfta provet till en tunn central filament som löper genom ett detektionsfönster.
Bygga bättre chip på minuter, inte timmar
De flesta forskningsmikrofluidiska chip idag tillverkas av mjuk silikon (PDMS) med hjälp av soft litografi, en process som kräver flera uppvärmnings- och härdningssteg och kan ta en timme eller mer per enhet. PDMS är lätt att forma men böjer sig vid högt tryck, vilket får kanalerna att svälla utåt och den fokuserade strålen att sprida sig. Den nya enheten använder en hård plast kallad polyuretanakrylat (PUA), mönstrad genom en "dubbelöverförings"-process. Först gjuts en återanvändbar PDMS-form med upphöjda kanalstrukturer från en kiselmaster. Flytande PUA hälls sedan i denna form, härdas under ultraviolett ljus och skalas av för att bilda kanallagret. En separat glasplatta belagd med PUA fungerar som bas. De två PUA-ytskikten riktas in, pressas ihop och binds med ytterligare en kort UV-exponering. Eftersom varje härdningssteg tar bara sekunder och ingen lång bakning krävs kan ett komplett chip produceras på ungefär fem minuter, ungefär tio gånger snabbare än traditionella metoder.
Testa flödet och tygla deformation
För att förstå hur väl konstruktionen fungerar kombinerar teamet datorbaserade simuleringar med experiment. Först simulerar de hur förändringar av flödeshastigheterna för prov- och skyddsströmmarna påverkar formen på den fokuserade kärnan. Resultaten visar att ökade vertikala och sidokåpsflöden båda hjälper till att minska provets höjd och bredd, och att högre totala hastigheter (högre Reynolds-tal) ytterligare förbättrar fokuseringen. De simulerar sedan hur kanalsidorna deformeras när de är gjorda av mjuk PDMS jämfört med styv PUA. Under realistiska högfartsförhållanden buktar PDMS-väggar ut med över hundra mikrometer, tillräckligt för att förvränga flödet så kraftigt att provet splittras och driver mot hörnen. I kontrast deformerar PUA med mindre än hundra nanometer—i praktiken styvt i denna skala—så den fokuserade strömmen förblir centrerad och tät även vid högt tryck.
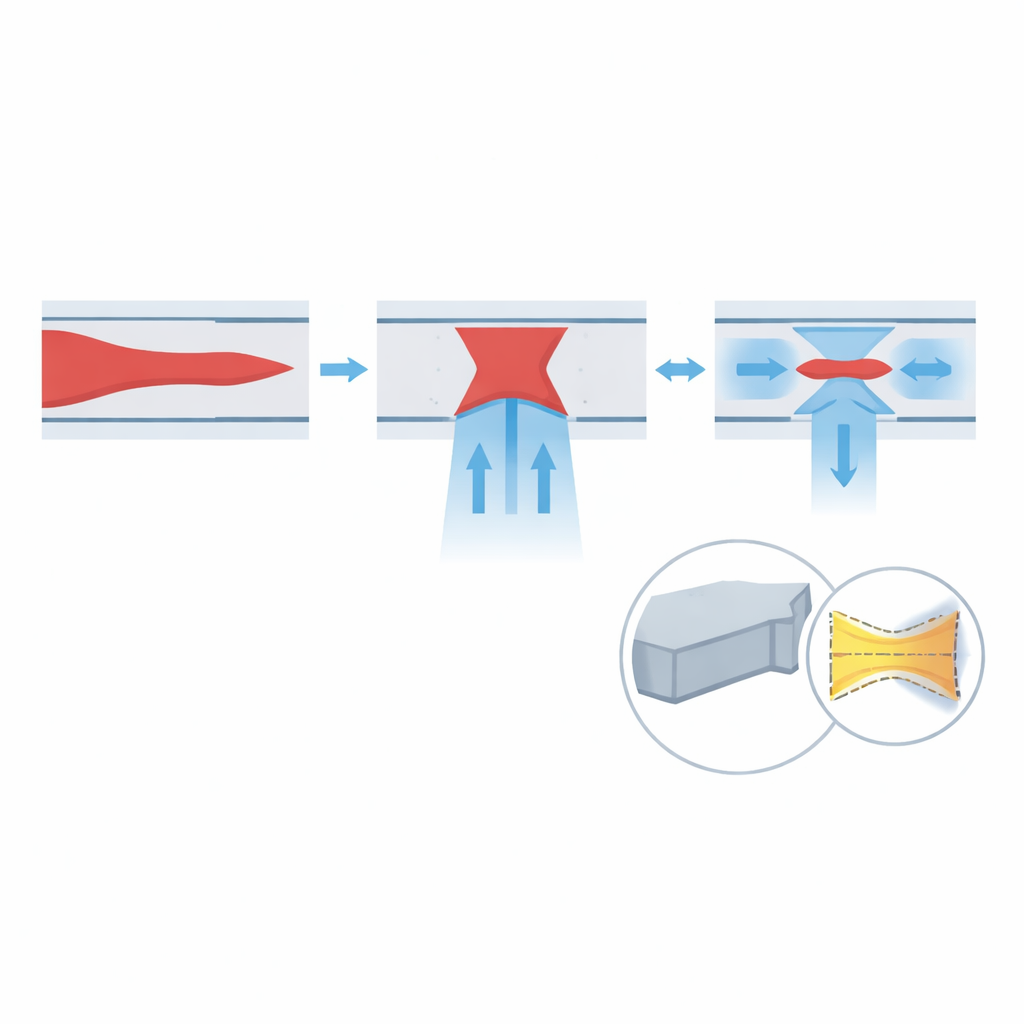
Se verkliga celler i extrema hastigheter
Utöver färgämnestester utvärderar författarna enheten med optisk tidssträckningsmikroskopi (OTS), en teknik som omvandlar ultrafasta laserpulser till snabba linjeskanningar och möjliggör miljontals linjebilder per sekund. De skickar behandlade urinprover från blåscancerpatienter genom chippet vid ökande flödeshastigheter, medan OTS spelar in tvådimensionella bilder av varje passerande cell. Eftersom det optiska systemet har en mycket tunn fokalregion blir varje cell som avviker upp- eller nedåt suddig, vilket ger en direkt mätning av vertikal fokusering. Över hastigheter från 3,3 till 16,7 meter per sekund ökar andelen skarpt fokuserade bilder och når 98,4 % vid den högsta testade hastigheten. Lateral fokusering bedöms genom att mäta hur långt cellcentren avviker från kanalens mittpunkt; denna förskjutning minskar med hastigheten, vilket motsvarar ungefär 95,0 % lateral fokuseringseffektivitet vid 16,7 meter per sekund.
Vad detta innebär för framtida cellanalys
Enkelt uttryckt visar forskarna att ett okomplicerat, enskikts plastchip pålitligt kan samla celler i en tät, välkontrollerad ström i alla riktningar, även under de krävande förhållanden som krävs för ultrahöghastighetsavbildning. Genom att kombinera ett deformationståligt material med en smart arrangemang av skyddsflöden undviker de de mekaniska begränsningarna hos mjuka silikonanordningar samtidigt som tillverkningstiden minskar dramatiskt. Detta gör det enklare att producera många identiska chip för klinisk och industriell användning och att köra storskaliga höggenomströmningsanalyser på verkliga patientprover. Som ett resultat erbjuder tekniken en praktisk väg mot snabbare, mer precisa verktyg för cellscreening som kan gynna diagnostik, cancerövervakning och andra tillämpningar som är beroende av att noggrant undersöka stora mängder enskilda celler.
Citering: Yan, R., Wei, S., Weng, Y. et al. Rapid-manufacturing and cost-effective single-layer microfluidic device for high-throughput three-dimensional hydrodynamic focusing. Microsyst Nanoeng 12, 87 (2026). https://doi.org/10.1038/s41378-026-01212-5
Nyckelord: mikrofluidisk flödescytometri, 3D hydrodynamisk fokusering, höggenomströmning enkelcellanalys, polyuretanakrylat mikrofluidiska chip, optisk tidssträckningsmikroskopi