Clear Sky Science · sv
Robotiserat transportsystem för celler baserat på modellering av mikropipettmotstånd
Flytta små celler utan mikroskop
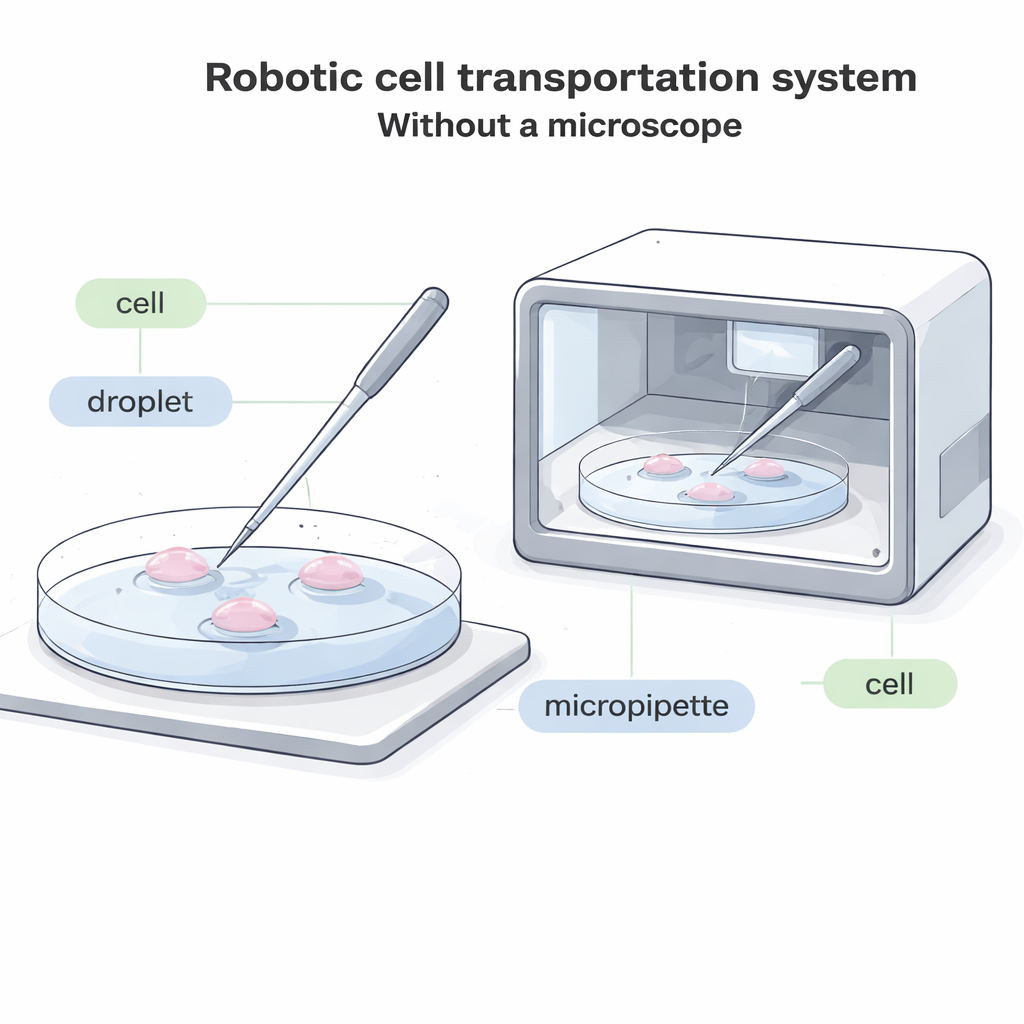
Modern biologi bygger ofta på en överraskande enkel uppgift: att plocka upp en enskild cell med ett glasrör och placera den någon annanstans. Det är avgörande för fertilitetsbehandlingar, nedfrysning av embryon, cellbaserade terapier och grundforskning. Idag kräver det nästan alltid ett skrymmande mikroskop och en högt utbildad operatör som övervakar varje rörelse. Denna artikel beskriver ett nytt robotsystem som kan flytta enskilda celler mellan vätskedroppar utan någon mikroskopisk vy alls, vilket öppnar för helt slutna, automatiserade "cellfabriker" som kan arbeta snabbare, billigare och med mindre skada på känsliga celler.
Varför cellförflyttning behöver förnyas
I dagens laboratorier tittar en operatör genom ett mikroskop och använder ett tunt glasrör, en så kallad mikropipett, för att nå botten av en petriskål, försiktigt suga in en cell, flytta den till en ny vätskedroppe och sedan trycka ut den. Processen är långsam, visuellt krävande och svår att automatisera. I många framtida system — till exempel kompakta, förseglade enheter som odlar embryon eller andra celler inuti en låda — finns helt enkelt inte plats för ett traditionellt mikroskop. I andra fall är celler märkta med fluorescerande färgämnen som kan blekna eller skadas av ljus, så det är viktigt att minimera intensiv mikroskopisk observation. Befintliga "blinda" system som inte förlitar sig på bilder fungerar bara för ovanligt stora celler, vilket lämnar de flesta vanliga celltyper utan bra automatiserade lösningar.
Ett särskilt sugrör med inbyggd stoppfunktion
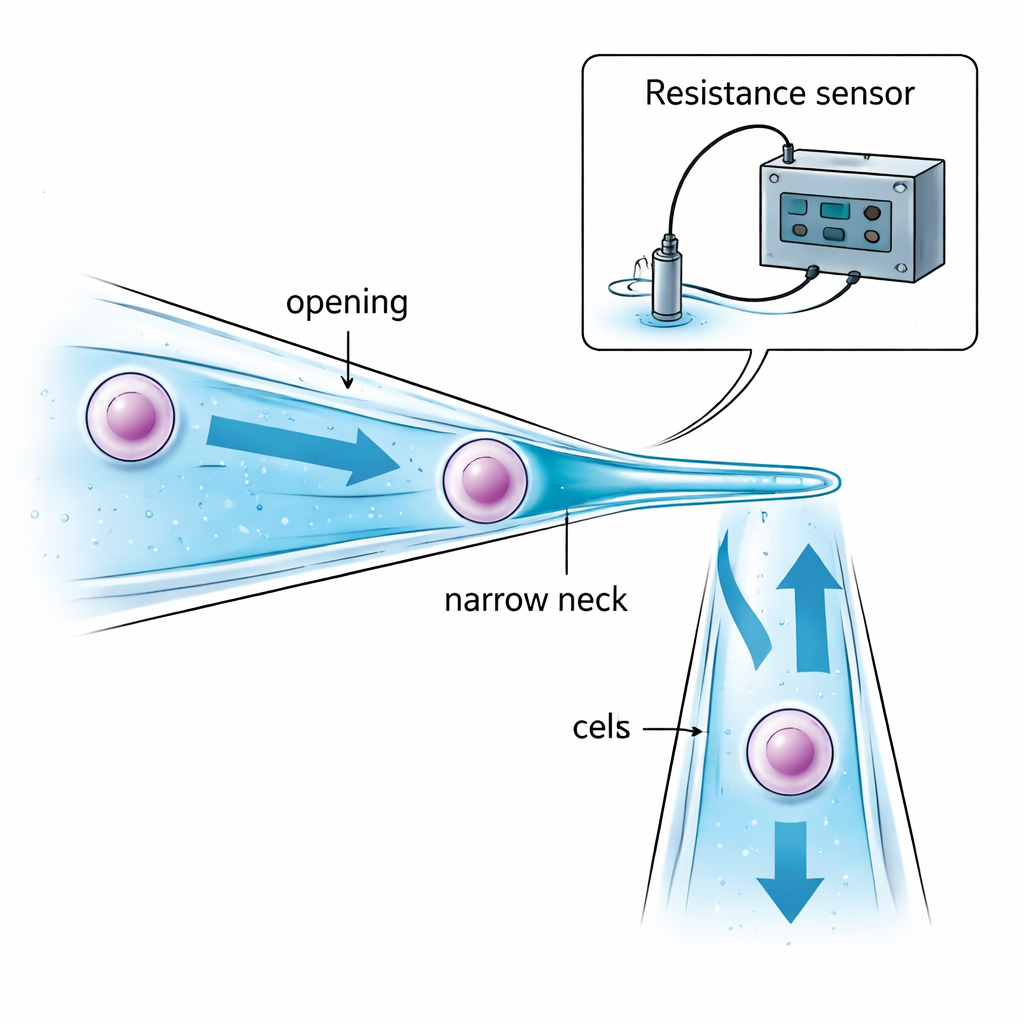
Författarna angriper problemet genom att omforma själva mikropipetten. Istället för ett rakt glasrör med samma diameter genom hela, skapar de en mikropipett med smal nacke. Öppningen är något större än målcellens diameter så att cellen kan dras in. Längre in smalnar röret försiktigt till en "nacke" som är mindre än cellen. När sug kraftar cellen mot denna förträngning stoppas den och hålls på plats inuti röret — istället för att dingla i spetsen och exponeras för olja eller luft mellan dropparna. Genom noggrant val av öppningsstorlek, nackstorlek och avståndet mellan dem säkerställs att cellen kan fångas säkert utan att klämmas för hårt, och att endast en liten mängd vätska förs med från en droppe till en annan, vilket minskar kontaminationsrisken.
Lyssna på elektriska signaler i stället för att titta
Utan mikroskop måste roboten ändå veta tre saker: när glaspipettens spets är tillräckligt nära skålens botten, när cellen framgångsrikt har fångats vid nacken, och när den har släppts helt i den nya droppen. Teamet löser detta genom att övervaka små förändringar i elektriskt motstånd i vätskan inuti och runt mikropipetten. När den lutande pipetten närmar sig skålens botten krymper vätskeavståndet mellan dem och det elektriska motståndet stiger på ett förutsägbart sätt, vilket signalerar en säker landning precis före kontakt. När en cell blockerar den smala nacken begränsas den elektriska vägen genom vätskan och motståndet ökar plötsligt; när cellen trycks ut sjunker motståndet lika snabbt. Matematiska modeller av dessa "gap", "aspiration" och "injektions"-motstånd tillåter en dator att tolka signalerna i realtid och avgöra när sug eller tryck ska stoppas, allt utan visuell återkoppling.
Sätta roboten på prov
För att se om tillvägagångssättet fungerar i praktiken byggde forskarna ett komplett robotsystem som kombinerar rörelsekontroll, tryckstyrning, motståndssensorik och en värddator. De testade det på små cancerceller kända som HeLa-celler (cirka 10 mikrometer i diameter) och mycket större grisäggceller (ungefär 150 mikrometer). Systemet kunde pålitligt upptäcka landning, fångst och frigöring enbart från motståndssignaler över ett brett utbud av pipettstorlekar. I direkt jämförelse flyttade roboten HeLa-celler med 90 procents framgång — bättre än en tidigare bildbaserad automatisk metod — och transporterade grisägg med 95 procents framgång, högre än en standard mikroskopisk metod. Tiden per cell var liknande eller snabbare än mänskligt styrda metoder, främst eftersom den smala nacken eliminerar behovet av upprepad finjustering av sugstyrkan för att positionera cellen.
Bevara cellernas livskraft och skala upp
En robotassistent i biologilabb måste undvika att skada de celler den hanterar. Efter transport med det nya systemet odlas både HeLa-celler och grisäggceller i ett dygn och färgades med en fläck som endast lyser upp i levande celler. Överlevnadsgraden för den nya metoden matchade eller närmade sig de som erhölls vid traditionell mikroskopledd överföring och hos opåverkade kontrollceller, vilket tyder på att den milda mekaniska klämningen vid den smala nacken inte märkbart minskar cellernas livskraft när tröskelvärden ställs in korrekt. Framöver föreslår författarna att samma motståndsbaserade sensning och tryckkontroll kan byggas in i kompakta mikrofluidiska chip. Det skulle möjliggöra många parallella kanaler, vilket möjliggör hög genomströmning i helt slutna cellhanteringssystem lämpade för automatiserad reproduktionsmedicin, cellterapier och långsiktiga odlingsenheter där mikroskop svårt kan användas.
Vad detta innebär för framtida cellarbete
För icke-specialister är huvudbudskapet att förflyttning av enskilda celler inte längre behöver bero på en person som tittar genom ett mikroskop. Genom att noggrant forma ett glasrör och "lyssna" på hur elektricitet flyter genom den omgivande vätskan kan en robot känna när den har landat, fångat en cell och släppt den — allt i mörker och i trånga utrymmen. Detta gör det mycket mer praktiskt att designa slutna, självgående cellodlingssystem som skyddar känsliga prover, förenklar kliniska arbetsflöden och för oss närmare laboratoriekvalitativ cellmanipulation i en automatiserad, fabriksliknande drift.
Citering: Zhao, Q., Liu, M., Zhu, R. et al. Robotic cell transportation system based on micropipette resistance modeling. Microsyst Nanoeng 12, 65 (2026). https://doi.org/10.1038/s41378-026-01193-5
Nyckelord: cellmanipulation, mikropipett, robotik, mikrofluidik, automatisering