Clear Sky Science · sv
Strategier för att kontrollera cellers rumsliga organisation i mikrofysiologiska system
Att bygga små vävnader i laboratoriet
Våra organ fungerar så bra eftersom deras celler inte ligger utspridda slumpmässigt—de är noggrant arrangerade i rummet. Denna artikel undersöker hur forskare lär sig återskapa denna intrikata ordning inne i ”organ-on-chip” och andra miniatyriserade laboratorieodlade vävnader. Genom att styra var olika celler placeras och hur de interagerar kan forskare bygga mer realistiska modeller av hjärta, hjärna, tarm, blodkärl och till och med människa–mikrob-ekosystem. Dessa avancerade system lovar säkrare läkemedelstestning, färre djurförsök och bättre verktyg för att studera sjukdomar och utveckla personanpassade behandlingar.
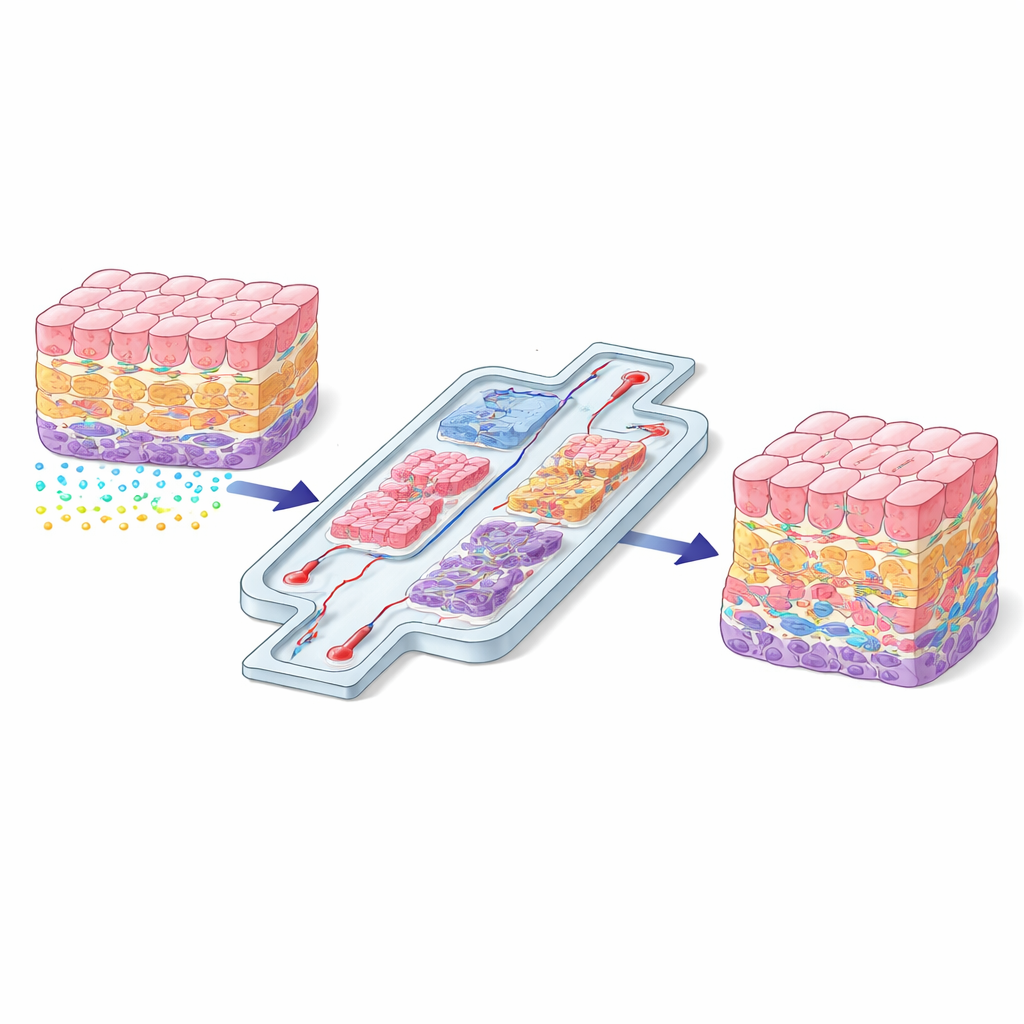
Varför cellens position spelar roll
Inne i kroppen lever varje cell i ett specifikt kvarter med sin egen blandning av stödjande strukturer, kemiska signaler och fysiska krafter. En levercell nära ett blodkärl möter helt andra signaler än en cell begravd djupt i organet. Dessa skillnader i läge hjälper till att bestämma hur celler växer, vad de differentierar till och hur de svarar på skada eller medicin. När forskare odlar celler på platta plastskålar går den rumsliga ”konversationen” förlorad och cellerna beter sig ofta onaturligt. Artikeln hävdar att att återskapa realistisk rumslig organisation inte är en valfri förbättring utan ett grundläggande krav om laboratorieodlade vävnader ska efterlikna riktiga organ.
Två huvudvägar för att arrangera celler
Författarna grupperar nuvarande strategier i två breda familjer: direkt och indirekt kontroll. Direkta metoder placerar fysiskt celler eller fack exakt där de behövs. Exempel är 3D-bioprinting, som lägger ner lager av celler och mjuka geler som en biologisk 3D-skrivare; mikrofluidiska chip som skär ut vävnader i sammankopplade kammare och kanaler; och fysiska fångstmetoder som knuffar celler på plats med ljus, ljud, magneter eller elektriska fält. Dessa tillvägagångssätt visar sin styrka när precis geometri är avgörande—som att återskapa blod–hjärnbarriären, en lagerindelad blodkärlsvägg eller flödesvägen från tarm till lever.
Låta cellerna läsa sin omgivning
Indirekta metoder omformar istället miljön och låter cellerna sköta resten. Här justerar forskare det ”landskap” som cellerna känner av: sammansättningen i den omgivande gelen, ytornas styvhet och textur, samt gradienter av lösta ämnen som tillväxtfaktorer eller läkemedel. Noggrant ordnade stödjande molekyler kan få vissa celltyper att bosätta sig i specifika regioner. Smarta hydrogel som mjuknar eller frisätter signaler när celler omstrukturerar dem uppmuntrar självorganiserade strukturer såsom blodkärnsnätverk eller tarmliknande kryptor och villi. Mikrofluidiska enheter kan generera stabila kemiska gradienter som får stamceller att anta olika identiteter längs en kanal, eller får cancerceller och immunceller att migrera till skilda zoner och därigenom avslöja hur sjukdomar sprider sig.
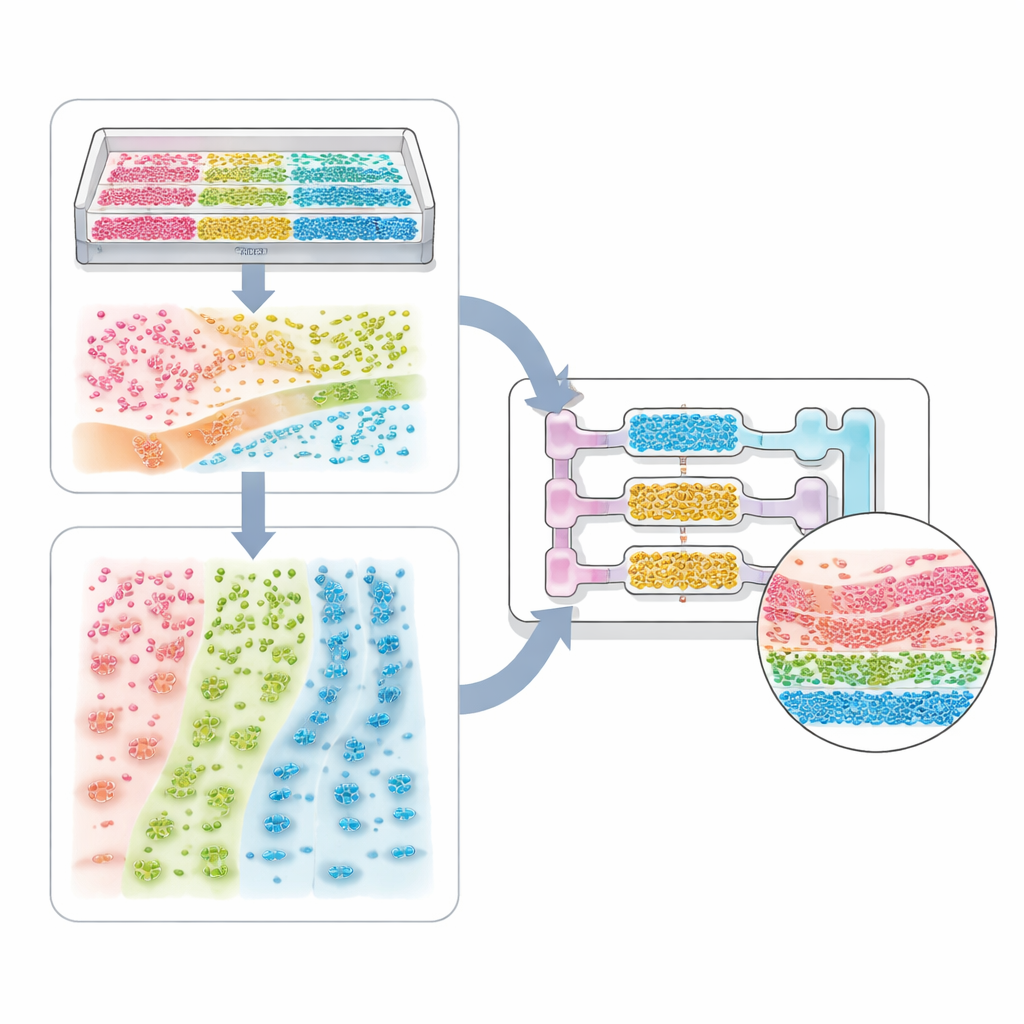
Från enskilda cellsystem till helkroppsmodeller
Översikten går igenom ett spektrum av tillämpningar. I den enklaste änden finns encelliga system, där mönstrade fåror eller styvhetsgradienter kan få hjärtceller att slå i takt eller nervceller att förlänga ordnade fibrer. Mer komplexa vävnadsmodeller blandar flera celltyper—såsom tumörceller, stödjeceller och blodkärlsceller—för att bilda sferoider och organoider med interna kärnor och skikt. Mikrokanalchip och bioprinting lägger sedan till gränser och flöde, vilket möjliggör återskapande av lungblåsor, njurfilter, leverzoner och multi-organ-kretsar som följer hur ett läkemedel tas upp, omvandlas och utsöndras. Samma idéer gäller värd–mikrob-system, där den rumsliga ordningen av bakterier längs tarmväggen eller över ett slemskikt kan avgöra om de skyddar oss eller orsakar sjukdom.
Kontrollera att mönstren är verkliga
Eftersom dessa system blir mer intrikata behöver forskare tillförlitliga sätt att bekräfta att cellerna hamnar där de ska och beter sig som avsett. Artikeln framhäver avbildningsmetoder som kan följa levande celler när de rör sig och förändras över tid, liksom avancerade färgnings- och sekvenseringstekniker som kartlägger vilka gener, proteiner och metaboliter som förekommer på varje plats. Sensorer inbyggda i chip kan mäta syre, näringsämnen, syror och mekaniska krafter och knyta lokala förhållanden till cellresponser. Tillsammans hjälper dessa verktyg forskare att verifiera att en design inte bara är visuellt övertygande utan också funktionellt trogen verklig vävnad.
Vart detta arbete är på väg
Författarna drar slutsatsen att de mest kraftfulla systemen kommer att kombinera direkta och indirekta strategier: använda chip och bioprinter för att fastställa den övergripande layouten och sedan lägga in ställbara geler, texturer och gradienter som låter vävnader mogna och omforma sig över tid. De noterar också praktiska hinder—såsom att skala upp tillverkningen, minska variation mellan laboratorier och hantera etiska frågor kring komplexa mänskliga vävnadsmodeller. Trots detta är budskapet tydligt: att bemästra rumslig organisation är nyckeln för att förvandla mikrofysiologiska system till trovärdiga ersättare för mänskliga organ, vilket öppnar nya möjligheter för att studera utveckling, testa terapier och skräddarsy medicin till enskilda patienter.
Citering: Truong, H.D., Ge, Z., Chng, E. et al. Strategies to control cellular spatial organization in microphysiological systems. Microsyst Nanoeng 12, 85 (2026). https://doi.org/10.1038/s41378-025-01141-9
Nyckelord: organ-on-a-chip, cellers rumsliga organisation, 3D-bioprinting, mikrofluidiska vävnadsmodeller, mikrofysiologiska system