Clear Sky Science · sv
En enflaskig CRISPR-baserad punktvårdsplattform för snabb, specifik och känslig detektion av HPV 16 utan förförstärkning
Varför det spelar roll att upptäcka just en virustyp
Cervixcancer är ofta kopplat till infektion med humant papillomvirus (HPV), men alla HPV-typer har inte samma riskprofil. Kliniker behöver därför tester som tillförlitligt kan skilja dessa mycket lika virus åt, särskilt den högrisktyp som kallas HPV16. Utmaningen är att dagens genetiska tester ibland kan förväxla nära släktingar, vilket leder till falska larm eller missade fall. Den här studien introducerar en ny testmetod som kraftigt förbättrar både noggrannhet och användbarhet, med målet att föra precis HPV-subtypning till kliniker och punktvårdsinställningar.
Låset och nyckeln i molekylär form
Forskarna byggde ett enrörstest som de kallar CASTSA och som kombinerar två effektiva idéer: precisionen hos CRISPR, ett genriktat system anpassat från bakterier, och signalförstärkningen hos PCR, den vanliga metoden för att kopiera DNA. I CASTSA leds ett CRISPR-protein kallat Cas12a till HPV16:s genetiska sekvens av ett kort RNA-”nyckel”. När det hittar en exakt match plus ett närliggande kort mönster som krävs (PAM), klipper Cas12a virus-DNA vid en förutsägbar plats. Detta snitt skapar en karakteristisk lös ände på ena DNA-strängen som fungerar som en unik startpunkt för amplifikation. Andra HPV-typer, även med mycket liknande sekvenser, klipps antingen inte eller genererar inte rätt startpunkt och amplifieras därför inte.
Att göra ett litet snitt till en stark signal
För att omvandla det CRISPR-inducerade snittet till en detekterbar signal designade teamet en särskild DNA-primer kallad terminalspecifik primer. Denna primer fäster endast korrekt på den sträng som produceras av Cas12a:s snitt, viker sig sedan tillbaka som en hårnål och hjälper till att bygga ett stabilt mall-DNA för PCR. Ytterligare ”universella” primersekvenser fäster därefter och driver en konventionell realtids-PCR-reaktion. Avgörande är att amplifikation endast sker om Cas12a först gjort sitt jobb och om primern vikts korrekt, vilket skapar två kontrollnivåer. Denna arkitektur minskar kraftigt risken att delvis matchande, icke-målorienterat DNA oavsiktligt amplifieras, och undanröjer en vanlig svaghet hos tidigare CRISPR-baserade tester som förlitade sig på en separat förförstärkningssteg.
Allt i ett rör, med färre fel
En viktig praktisk förbättring är att CRISPR-klippning och PCR-amplifikation sker tillsammans i samma förseglade rör, vilket undviker att öppna rör mellan steg — en stor källa till kontaminering i många laboratoriearbetsflöden. Författarna finjusterade reaktionsförhållandena, särskilt magnesiumkoncentrationen, så att både Cas12a och DNA-kopierande enzym fungerar väl utan att främja oönskade reaktioner. De visade att deras enflaskiga setup tillförlitligt kan skilja HPV16 från flera andra högrisktyper, inklusive HPV18, 33, 45 och 52, trots att dessa virus delar starkt bevarade genetiska regioner. Jämfört med standard realtids-PCR ensam, eller CRISPR-tester som först amplifierar DNA och sedan genomför CRISPR-detektion, gav CASTSA långt färre vilseledande signaler från icke-specifika HPV-typer.
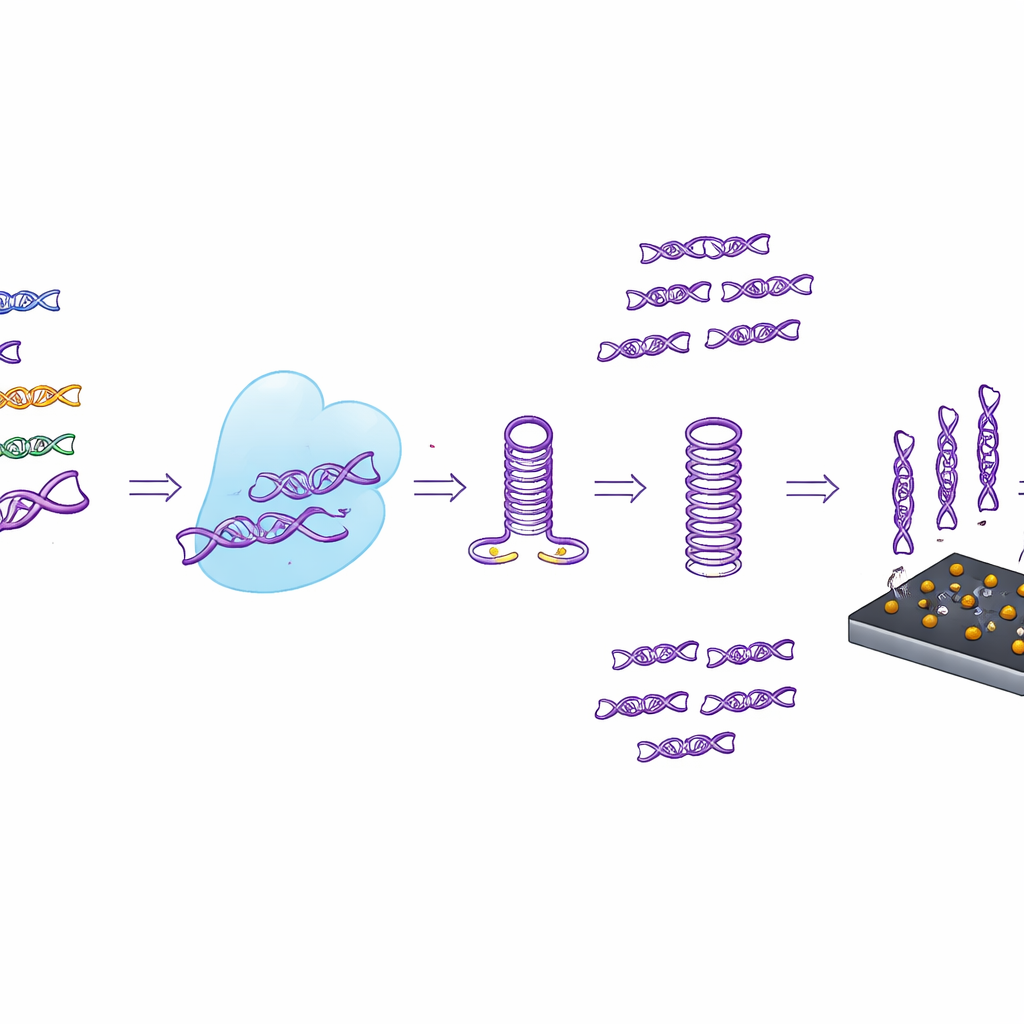
Från provrör till handhållen sensor
I stället för att enbart förlita sig på fluorescensläsning kopplade forskarna även CASTSA till en kompakt elektrokemisk sensor tillverkad av laserinducerat grafen. Denna porösa, mycket ledande kolyta dekoreras med guldbärande nanopartiklar som bär fångststrängar utformade för att binda endast CASTSA-amplifikationsprodukter från HPV16. När dessa produkter fäster ändras den elektriska strömmen genom sensorn på ett mätbart sätt. Genom att använda en fyraelektrodsarray — tre mätpunkter och en inbyggd bakgrundskontroll — kan enheten subtrahera brus från icke-specifik bindning. I försök detekterade detta integrerade system så få som 18 kopior av HPV16-målet per reaktion, vilket överträffade känsligheten hos enbart fluorescens och bibehöll utmärkt repeterbarhet.
Hur detta kan förändra HPV-testning
För att utvärdera metoden i verkliga förhållanden testade teamet 20 kliniska prover kända för att innehålla HPV16 och 10 prover från friska donatorer. CASTSA, både i sin fluorescerande form och när den parades med grafenbaserade sensorn, överensstämde helt med standardiserade sjukhus-PCR-tester. Samtidigt visade den en överlägsen förmåga att ignorera andra högrisk-HPV-typer som ofta orsakar förvirring. För patienter kan detta innebära färre otydliga resultat och tryggare beslut om uppföljning och behandling. Mer generellt erbjuder CASTSA-strategin — först CRISPR-igenkänning, sedan amplifikation, allt i ett förseglat rör — en modell för mycket specifika, lågkontaminations genetiska tester som kan anpassas till många patogener och mutationer, särskilt i miljöer som kräver snabba och tillförlitliga svar.
Citering: Chen, Y., Chen, Y., Zhang, C. et al. One-pot CRISPR-based point of care platform for rapid, specific and sensitive detection of HPV 16 without pre-amplification. Microsyst Nanoeng 12, 81 (2026). https://doi.org/10.1038/s41378-025-01130-y
Nyckelord: Detektion av HPV16, CRISPR-diagnostik, PCR-baserad testning, elektrokemisk biosensor, punktvårdsanalys