Clear Sky Science · sv
Interferometrisk bildskanningsmikroskopi för färgfria bilder med 120 nm lateral upplösning inuti levande celler
Att se levande celler utan tillsatta färgämnen
Modern biologi förlitar sig ofta på lysande fluorescerande märken för att avslöja den dolda arkitekturen inne i våra celler. Men dessa markörer kan stressa celler, förändra deras beteende och ibland inte alls fungera i ömtåliga eller svårmodifierade prover. Denna artikel introducerar ett nytt sätt att följa livets processer inne i levande celler med hög detaljrikedom—utan att tillsätta färger eller genetiska taggar—vilket lovar skonsammare, längre och mer naturliga observationer av hur celler verkligen fungerar.
Att se celler genom hur de sprider ljus
Metoden bygger på en familj tekniker som inte förlitar sig på fluorescens, utan istället mäter hur små strukturer sprider ljus. En sådan metod, interferometrisk spridningsmikroskopi (iSCAT), blandar ljus som sprids av ett nanoskaligt objekt med en referensreflektion från en glasyta. Det resulterande interferensmönstret är extremt känsligt för mycket små partiklar som proteiner, virus eller vesikler. iSCAT har tidigare fungerat bäst på enkla, rena prover som isolerade partiklar på glas. Att tillämpa den djupt inne i levande celler har dock varit svårt eftersom celler är trånga och röriga: många överlappande spridningshändelser skapar en kornig bakgrund som döljer fina detaljer.
Kombination av två idéer för skarpare, skonsammare avbildning
För att övervinna dessa begränsningar kombinerade författarna iSCAT med en kraftfull avbildningsstrategi kallad image scanning microscopy (ISM). I ISM skannas provet punkt för punkt med en fokuserad stråle, och istället för en enda detektor registrerar en matris av detektorpixlar många lätt förskjutna vyer av varje punkt. Genom att klurigt omjustera och kombinera dessa vyer kan man skärpa slutbilden utan att förlora värdefotoner. Den nya tekniken—interferometrisk image scanning microscopy, eller iISM—anpassar denna idé till de mer komplexa, fasesensitiva signalerna från interferometrisk spridning. Mikroskopet använder en blå laser, specialoptik för att göra ljusets polarisation symmetrisk, och en känslig kamera för att spela in det spridda och reflekterade ljuset för varje skanningsposition. Ett skräddarsytt beräkningsflöde omplacerar sedan pixelinformationen på ett sätt som respekterar signalens vågkaraktär, vilket ger bilder med cirka 120 nanometers lateral upplösning, ungefär två gånger finare än standard diffraktionsbegränsade optiker.
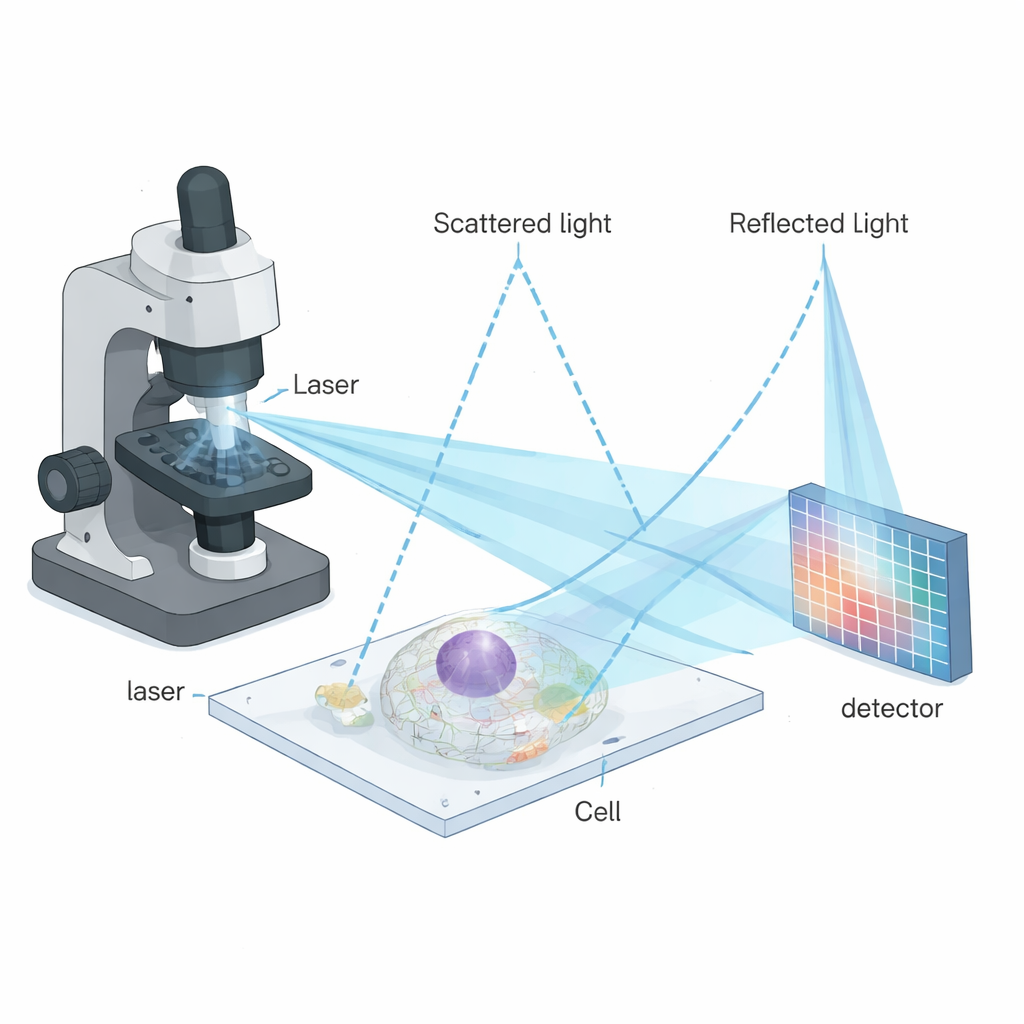
Smarta algoritmer förvandlar brusiga mönster till klara bilder
Eftersom interferometriska signaler bär både intensitets- och faseinformation räcker inte de vanliga bearbetningstricken från fluorescensavbildning. Författarna utvecklade en adaptiv pixel-reassignmentsprocedur (APR) skräddarsydd för koherent ljus. Först omvandlar de varje litet interferensmönster till en ”radial varians”-karta som framhäver symmetricenter utan att bry sig om signalens positiva eller negativa tecken. Detta steg omvandlar effektivt komplicerade interferensfransar till bilder som beter sig mer som konventionella intensitetsbilder. Sedan, med öppen källkodsprogramvara, bestämmer de hur mycket varje detektorpixels bild är förskjuten i förhållande till centrum och skjuter tillbaka dem innan de summeras. Denna förfinade justering koncentrerar den användbara signalen samtidigt som brus genomsnittas ned, vilket ökar kontrast-till-brus-förhållandet med ungefär en faktor fyra jämfört med en tätt stiftad konfokal iSCAT-bild, allt vid samma ljusnivå.
Att följa organeller och cytoskelett i aktion
Med dessa tekniska framsteg vände sig teamet till levande COS-7-celler för att testa hur väl iISM fungerar i praktiken. Vid mycket låg belysningseffekt—ungefär tio gånger lägre per fokuserad punkt än vad konventionella konfokala mikroskop ofta använder—kunde de tydligt urskilja nyckelorganeller: endoplasmatiskt nätverk, mitokondrier, vesikler, aktincytoskelett, plasmamembran och tunna framkantstrukturer kallade lamellipodier. Eftersom den interferometriska kontrasten är mycket känslig för vertikal position kunde liknande organeller uppträda med positiv eller negativ kontrast, vilket avslöjade subtila höjdskillnader på endast några hundra nanometer. Genom att spela in tidsserier följde de vesikler som rörde sig och endoplasmatiska tubuler som omformades under många minuter, utan uppenbar fotoskada och utan tecken på att avbildningen störde cellernas beteende.
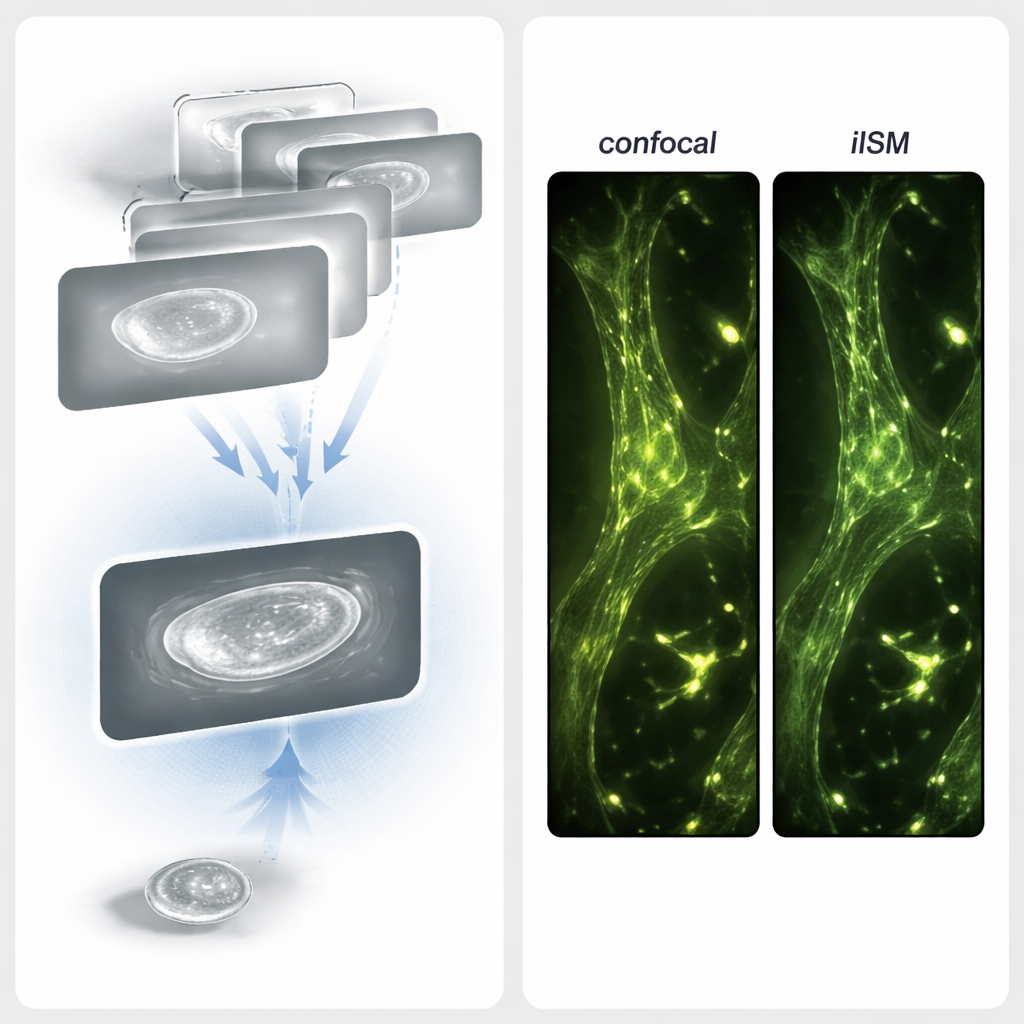
Att matcha färgfria vyer med fluorescerande kartor
För att kontrollera att de färgfria bilderna verkligen speglade verkliga cellulära strukturer utförde forskarna också kombinerade iISM- och fluorescens-ISM-mätningar i fixerade celler. De färgade in aktincytoskelettet med ett rött fluorescerande färgämne och spelade in superupplösta fluorescensbilder sida vid sida med färgfria iISM-bilder av samma region. När de överlade de två kanalernas bilder överensstämde ljusa aktinfilament i fluorescenskanalen nära med filamentösa strukturer i iISM-bilderna. I vissa regioner avslöjade iISM till och med ytterligare spridningsdetaljer—såsom variationer längs filament eller närliggande ofärgade strukturer som fokala adhesioner—som var osynliga i fluorescenskanalen. Tillsammans visar dessa resultat att iISM både kan bekräfta kända strukturer och upptäcka extra information om ofärgade omgivningar.
Fönster mot celler med mindre störning
För icke-specialister är huvudbudskapet att iISM erbjuder ett sätt att se fina detaljer inne i levande celler utan att göra dem artificiellt lysande. Den kombinerar känsligheten hos interferometrisk spridning med förfiningskraften i image scanning och uppnår ungefär 120 nanometers upplösning samtidigt som den använder avsevärt mindre ljus än många befintliga mikroskop. Eftersom den är byggd av komponenter som redan är vanliga i avancerade konfokala system kan den i princip läggas till kommersiella instrument. Framöver kan iISM kombineras med traditionell fluorescens, snabba detektorer eller till och med maskininlärningsbaserade ”virtuella färgningar” för att följa infektioner, transport av last, eller cytoskelettomorganisering i celler under förhållanden som ligger närmare deras naturliga, ostörda tillstånd.
Citering: Küppers, M., Moerner, W.E. Interferometric Image Scanning Microscopy for label-free imaging at 120 nm lateral resolution inside live cells. Light Sci Appl 15, 129 (2026). https://doi.org/10.1038/s41377-026-02210-y
Nyckelord: färgfria bilder, levandecellsmikroskopi, interferometrisk spridning, superupplösning, cellulära organeller