Clear Sky Science · sv
Syntetisk letalitet mellan MCL-1‑hämmning och CAR‑T‑terapi vid aggressiv B‑cellslymfom
Varför detta är viktigt för cancerbehandling
Aggressiva B‑cellslymfom är snabbväxande blodcancerformer som ofta återkommer efter behandling. Även kraftfulla nya metoder som CAR‑T‑cellsterapi, som omprogrammerar patientens egna immunceller för att angripa tumören, misslyckas hos ungefär hälften av patienterna över tid. Denna studie undersöker ett sätt att vända den svagheten till en fördel: att använda ett läkemedel som riktar sig mot ett nyckelprotein för lymfomcellernas överlevnad för att både döda tumörer och göra kvarvarande celler lättare för CAR‑T‑celler att slutföra.
Problemet med envisa lymfomceller
Aggressiva B‑cellslymfom drivs ofta av överdriven aktivitet i en gen som heter MYC, vilken pressar cellerna att dela sig snabbt och också hjälper dem att dölja sig för immunsystemet. Standardbehandlingar och även CAR‑T‑terapi kan lämna kvar små fickor av lymfomceller som tolererar läkemedel och senare orsakar återfall. Dessa ”persisterande” och resistenta celler lever i ett tumörområde fyllt av immunceller som undertrycker effekten och håller bort mördande T‑celler. Författarna undrade om blockering av MCL‑1, ett protein som lymfomceller är beroende av för att undvika programmerad celldöd, kunde blotta en dold svaghet i detta system.
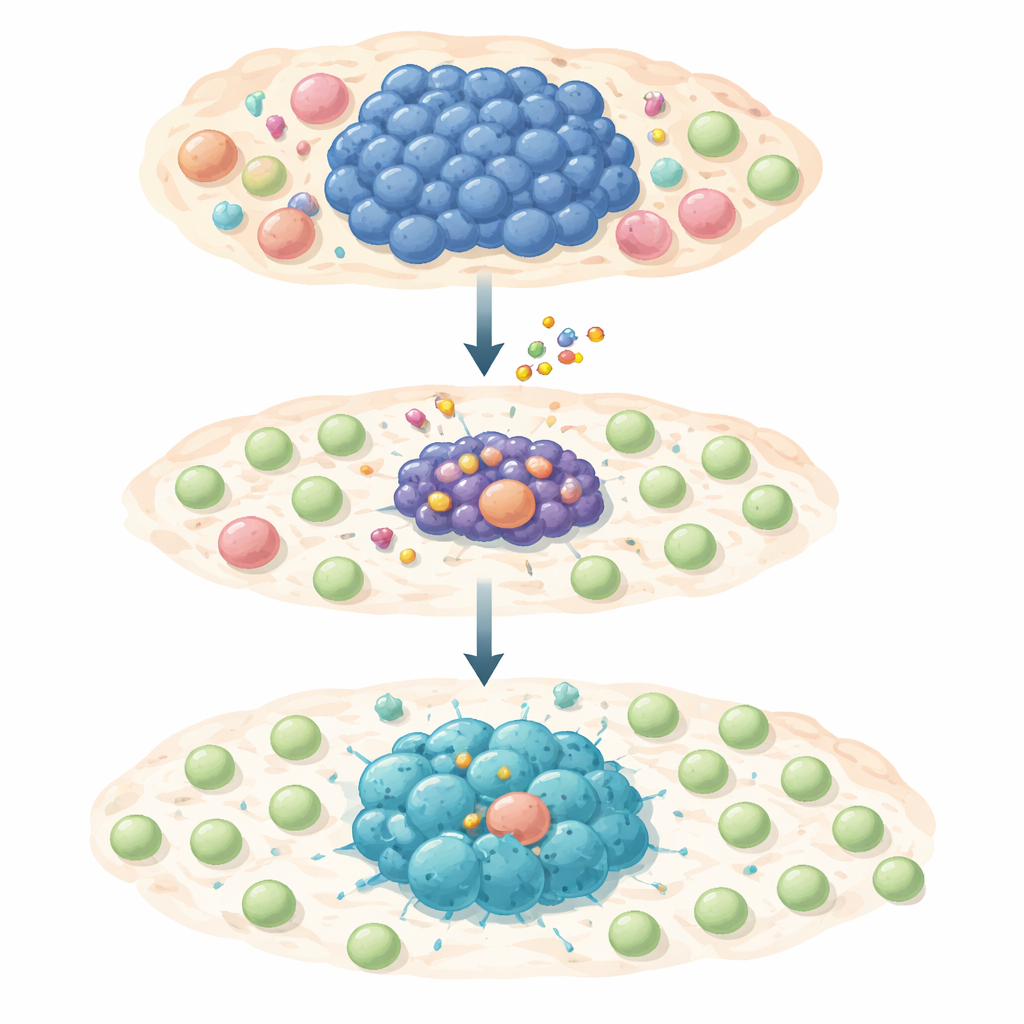
En tvåstegsattack mot tumörens överlevnad och förklädnad
Forskargruppen testade ett selektivt MCL‑1‑hämmande läkemedel, S63845, i ett stort panel av humana lymfomcellinjer som är beroende av MYC. De flesta av dessa cancerceller var mycket känsliga för läkemedlet och genomgick programmerad celldöd när MCL‑1 blockerades. Dock överlevde en liten andel korttids‑ eller långtidsbehandling och blev läkemedelstoleranta eller fullt resistenta. När forskarna studerade dessa överlevare mer i detalj fann de att MYC‑aktiviteten dämpades medan ett annat protein, STAT1, och dess tillhörande interferon‑larmsignal aktiverades. Denna förskjutning slog på gener som driver inflammatoriska signaler och kemokiner — molekylära ”fyrar” som kan dra till sig T‑celler till tumörområdet.
Återväckande av den immuna omgivningen
För att se hur detta fungerar i en levande organism behandlade författarna möss med MYC‑drivna lymfom med en låg dos av MCL‑1‑hämmaren. Läkemedlet minskade tumörbördan samtidigt som normala B‑celler sparades, men dess effekt gick bortom enkel volymsminskning. Behandlade tumörer visade fler CD4‑ och CD8‑T‑celler, färre utmattade T‑celler, färre regulatoriska T‑celler och färre suppressiva myeloida celler — alla tecken på en mer immunvänlig miljö. Enkeltcells‑RNA‑sekvensering av tumör- och omgivande celler bekräftade att kvarvarande lymfomceller hade minskat MYC, ökat STAT1 och starkare interferon‑ och inflammationssignaler, medan den omgivande vävnaden återbefolkades med aktiva T‑ och natural killer‑celler snarare än suppressiva celler.
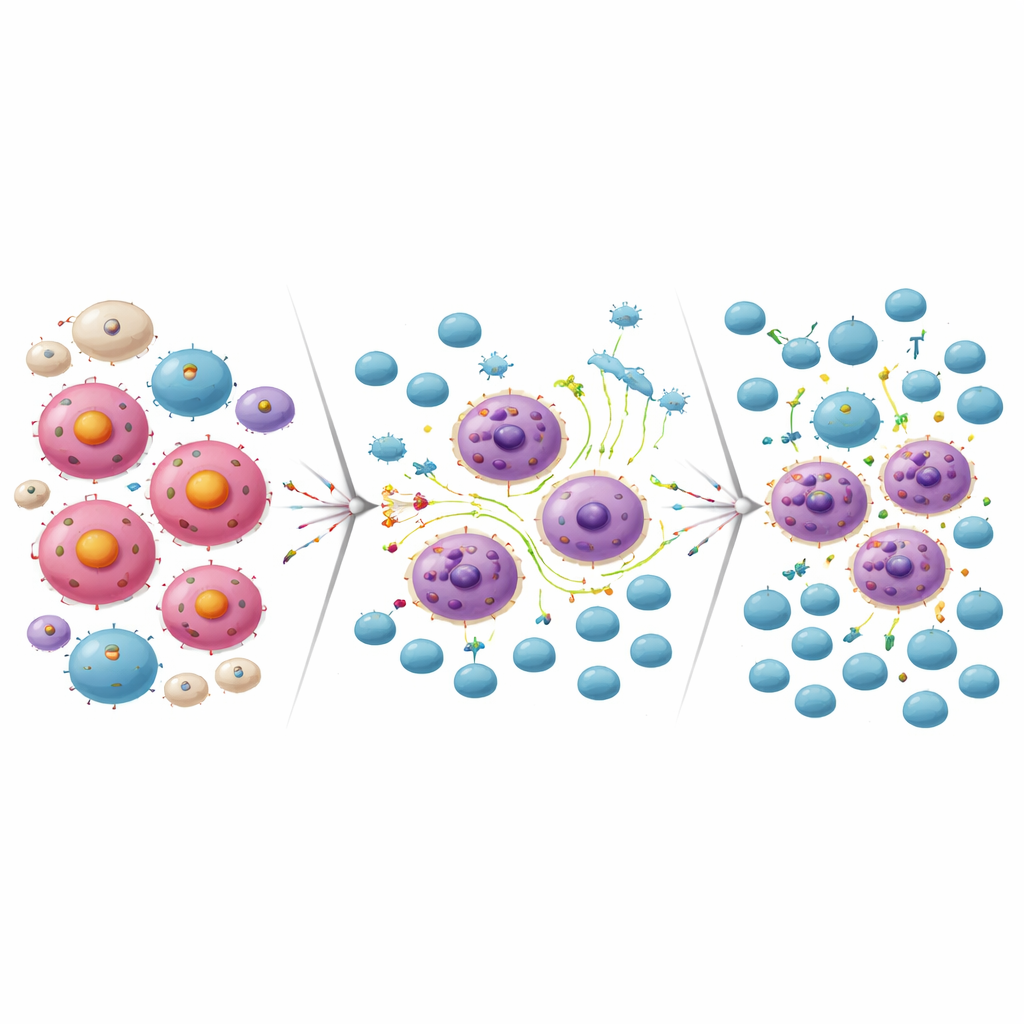
Att vända resistens till en öppning för CAR‑T‑celler
Samma inflammatoriska omprogrammering som hjälpte vissa lymfomceller att överleva MCL‑1‑blockaden gjorde dem också mer sårbara för immunsystemets angrepp. I laboratoriet dödade CD19‑inriktade CAR‑T‑celler effektivt lymfomceller som blivit resistenta mot MCL‑1‑läkemedlet. Omvänt var lymfomceller som blivit resistenta mot CD19 CAR‑T‑terapi mycket känsliga för MCL‑1‑hämmaren. När forskarna kombinerade en subletal dos av MCL‑1‑läkemedlet med CAR‑T‑celler i cellodling utplånade de två behandlingarna tillsammans betydligt fler lymfomceller än någon av behandlingarna för sig. I musemodeller ledde administrering av MCL‑1‑hämmaren följt av CD19 CAR‑T‑celler till nästan fullständig tumörrensning och signifikant längre överlevnad jämfört med enkelbehandlingar.
En ett‑två‑slags strategi med kurativ potential
Förenklat föreslår studien en ”ett‑två‑slags” strategi. Först slår ett MCL‑1‑blockerande läkemedel ner majoriteten av lymfomet och tvingar kvarvarande cancerceller in i ett inflammerat, högt synligt tillstånd som lockar T‑celler och avklär skyddande immunsköldar. Sedan utnyttjar CD19 CAR‑T‑celler denna nyblottade svaghet för att utrota den kvarvarande sjukdomen. Genom att angripa både tumörens interna överlevnadsnätverk och dess skyddande omgivning kan denna kombinerade strategi minska återfall och föra aggressiva B‑cellslymfom närmare långvarig remission.
Citering: Gao, J., Zhao, X., Yin, Q. et al. Synthetic lethality of MCL-1 inhibition and CAR-T therapy in aggressive B-cell lymphoma. Leukemia 40, 638–648 (2026). https://doi.org/10.1038/s41375-026-02884-8
Nyckelord: B‑cellslymfom, CAR‑T‑terapi, MCL‑1‑hämmning, tumörmikromiljö, läkemedelsresistens