Clear Sky Science · sv
CSF1R markerar en delmängd av fosterhematopoetiska multipotenta progenitorceller med förmåga att driva akut myeloisk leukemi
Varför denna forskning spelar roll för spädbarn med leukemi
Leukemi hos mycket små barn är sällsynt men ofta förödande, och många spädbarn svarar dåligt på dagens behandlingar. Denna studie ställer en förrädiskt enkel fråga med stora konsekvenser: vilka tidiga blodceller i embryot går först fel och utlöser en särskilt aggressiv form av spädbarnsleukemi, och kan vi hitta ett tydligt sätt att rikta behandling mot dem?
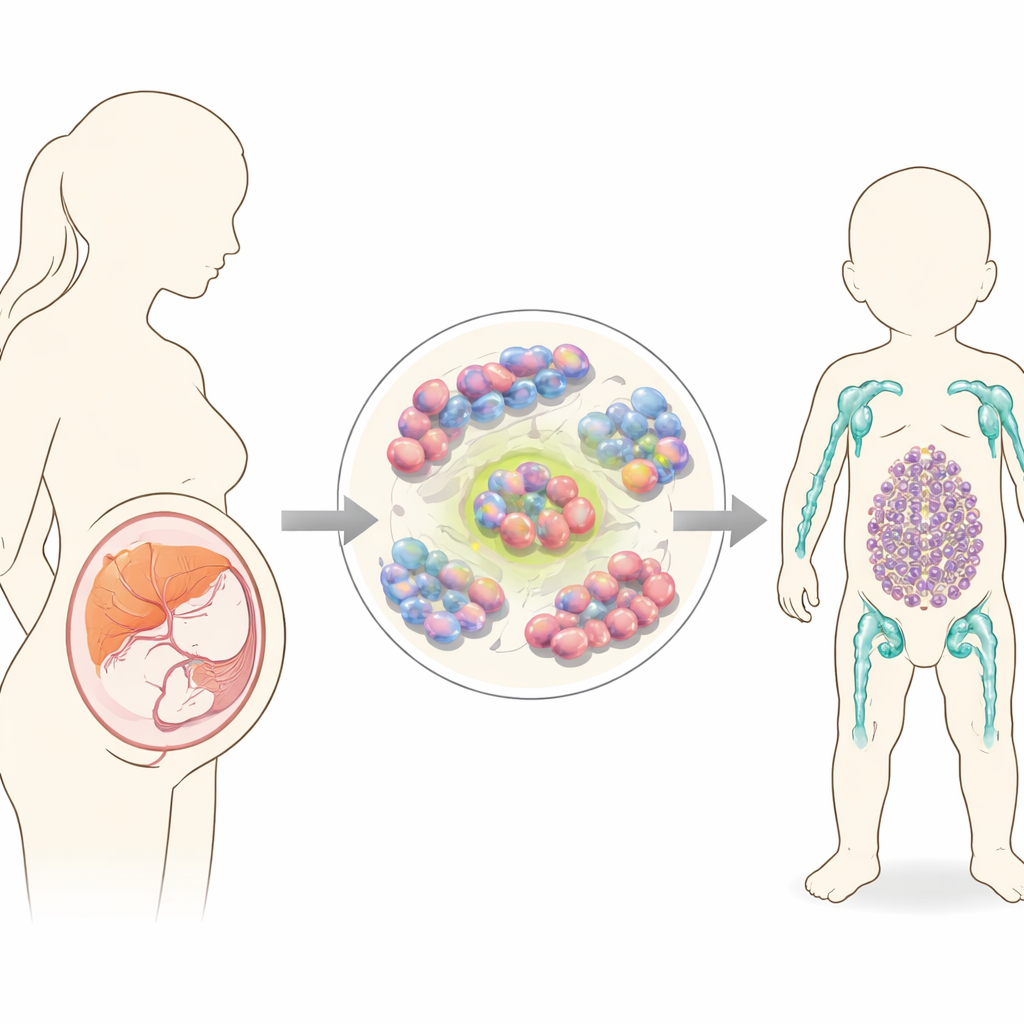
Problemet börjar före födseln
Läkare har länge misstänkt att många spädbarnsleukemier börjar i livmodern. Ledtrådar kommer från blodprover tagna vid födseln och från tvillingar som delar samma cancerframkallande mutationer. Under tidig utveckling förflyttas blodbildningen genom flera organ, inklusive gulsäcken och ett område nära aortan, innan den etableras i fostrets lever och senare i benmärgen. Vid varje plats uppträder och försvinner olika typer av omogna blodceller. Ett vanligt genetiskt fel i spädbarnsleukemi är ett brott och återförening av genen KMT2A med partnergener som MLLT3. Denna omorganisation kan driva antingen en lymfoid leukemi (liknande barn-ALL) eller en myeloid leukemi (AML), men det har varit oklart vilka exakta fosterceller som först omvandlas, och vad som styr dem mot den ena sjukdomstypen framför den andra.
En särskild fosterblodspreursor med myeloid lutning
Forskarna fokuserade på en population i fostrets lever kallad lymphoid-primed multipotent progenitors (LMPPs). Det är tidiga blodceller som fortfarande kan ge upphov till både lymfoida och myeloida linjer. Inom denna grupp riktade de in sig på en delmängd som bär ett ytprotein kallat CSF1R, en sensor för tillväxtsignaler som vanligtvis är kopplad till den myeloida grenen. Med en musmodell där KMT2A::MLLT3-fusionen kan aktiveras under fosterlivet jämförde de CSF1R-positiva och CSF1R-negativa LMPP:er. I laboratoriedishar kunde båda ge upphov till lymfoida kolonier, men CSF1R-positiva celler bildade markant fler kolonier under myeloida förhållanden och producerade oftare "blandade" kolonier med drag av både myeloida och lymfoida celler, vilket tyder på särskilt hög flexibilitet och omvandlingspotential.
Från flexibel precursor till leukemidrivare
För att testa vad som händer i en levande organism transplanterade teamet dessa ändrade fosterceller i immunbristförtjockade möss. Djur som fick KMT2A::MLLT3-uttryckande CSF1R-positiva LMPP:er utvecklade aggressiv akut myeloisk leukemi: deras blod, benmärg, mjälte, lever och till och med centrala nervsystem fylldes av omogna myeloida blaster, och sjukdomen kunde överföras till nya möss med benmärg från de första sjuka djuren. I kontrast visade möss som fick CSF1R-negativa LMPP:er initialt mestadels omogna B-celler i blodet, mer likt lymfoid sjukdom, och tog längre tid att insjukna. Genomiska analyser visade att CSF1R-positiva LMPP:er bar ett "stamlikt" genprogram kopplat till självförnyelse och till kända leukemistamceller hos pediatriska patienter, medan CSF1R-negativa celler visade signaturer närmare akut lymfatisk leukemi.
Överlevnadstrick: självstädning och tillväxtsignalering
Teamet undersökte sedan vad som gör att dessa CSF1R-märkta fosterceller trivs och driver sjukdom. De fann att gener involverade i autofagi—cellernas interna återvinnings- och självstädningssystem—var mer aktiva i de CSF1R-positiva cellerna. Att blockera autofagi med ett läkemedel minskade kraftigt deras förmåga att bilda kolonier. Att störa CSF1R-signaleringen själv skiftade balanserna bort från myeloid produktion och, när det kombinerades med autofagihämning, utplånades kolonibildningen nästan helt. Viktigt är att mänskliga leukemidataset visade att en liknande CSF1R-positiv LMPP-liknande population endast finns under tidig mänsklig utveckling och att CSF1R samt flera autofagirelaterade gener är särskilt aktiva i KMT2A-omorganiserad akut myeloisk leukemi. I en pediatrisk leukemicellinje som bär KMT2A::MLLT3 utlöstes omfattande celldöd av en CSF1R-hämmare, vilket understöder idén att dessa celler förblir beroende av denna signalväg.
Från fosterursprung till framtida terapier
Sammantaget tyder studien på att en övergående, CSF1R-märkt fostrets blodprogenitor sannolikt är startpunkten och motorn för KMT2A::MLLT3-drivna spädbarnsformer av akut myeloisk leukemi. Dessa celler kombinerar stamlik uthållighet med en inneboende myeloid bias och är beroende av både CSF1R-signaler och autofagi för att expandera och upprätthålla leukemin. Eftersom CSF1R är ett ytligt molekylärt mål som redan undersöks för riktade behandlingar, inklusive konstruerade CAR-T-celler hos vuxna, pekar detta arbete mot ett konkret, biologiskt grundat mål som skulle kunna anpassas för sårbara spädbarn vars sjukdom börjar långt innan de föds.
Citering: Camiolo, G., González Silvera, D., Leah, T. et al. CSF1R marks a subset of foetal haematopoietic multipotent progenitor cells with acute myeloid leukaemia propagation properties. Leukemia 40, 540–552 (2026). https://doi.org/10.1038/s41375-025-02856-4
Nyckelord: spädbarnsleukemi, akut myeloisk leukemi, fosterblodets utveckling, CSF1R, leukemistamceller