Clear Sky Science · sv
Löslig Notch‑agonist möjliggör mognad av humana ameloblaster och bildning av emaljliknande vävnad för tandregenerering
Varför det är så svårt att reparera tandemalj
Emalj, det glansiga vita skalet som täcker våra tänder, är det hårdaste materialet i människokroppen — men när det väl är borta är det i princip borta för gott. Mer än 90 procent av vuxna har viss förlust eller skada på emaljen, ändå finns ingen naturlig förmåga hos tänderna att bygga upp detta skyddande skikt igen. Denna studie beskriver ett sätt att odla humana emaljproducerande celler i labb, driva dem till en fullt mogen status och till och med få dem att avsätta emaljliknande mineral i djur. Arbetet öppnar en väg mot framtida terapier som en dag kan reparera tänder med levande vävnad i stället för fyllningar och kronor.
Bygga tandemalj från stamceller
Emalj bildas av specialiserade celler som kallas ameloblaster, vilka dör bort när en tand bryter fram genom tandköttet. Utan dem kan vuxna tänder inte bilda ny emalj. Forskarna använder humana inducerade pluripotenta stamceller — vuxna celler som omprogrammerats tillbaka till ett flexibelt, embryo‑likt tillstånd — för att skapa ”inducerade ameloblaster”. I tidigare arbete kunde dessa labbodlade celler börja likna naturliga emaljbildande celler men avstannade innan de nådde full mognad, och de fungerade bara korrekt när de växte i nära kontakt med odontoblaster, de celler som bildar den underliggande dentinen. Det väckte en central fråga: vad är det egentligen odontoblaster bidrar med som ameloblaster behöver för att slutföra sin utveckling?
Den saknade dialogen mellan tandceller
För att avkoda denna cellulära dialog grävde teamet i singelcells‑genuttryckskartor från utvecklande mänskliga och mus‑tänder. De sökte efter signalvägar som verkade gå specifikt från odontoblaster till ameloblaster under det avgörande fönster då emalj bildas. En väg stack ut: Notch, ett direkt cell‑till‑cell‑kommunikationssystem som används allmänt i embryonal utveckling. I dessa tandkartor fanns Delta‑liknande ligander (särskilt DLL1 och DLL4) främst på odontoblaster, medan Notch‑receptorer koncentrerades på mognande ameloblaster. När forskarna blockerade Notch‑aktivitet med ett läkemedel i sitt samexperiment minskade ameloblasterna kraftigt produktionen av enamelin, ett huvudprotein i emalj — starka bevis för att Notch‑signalering är nödvändig för att emaljbildande celler ska mogna. 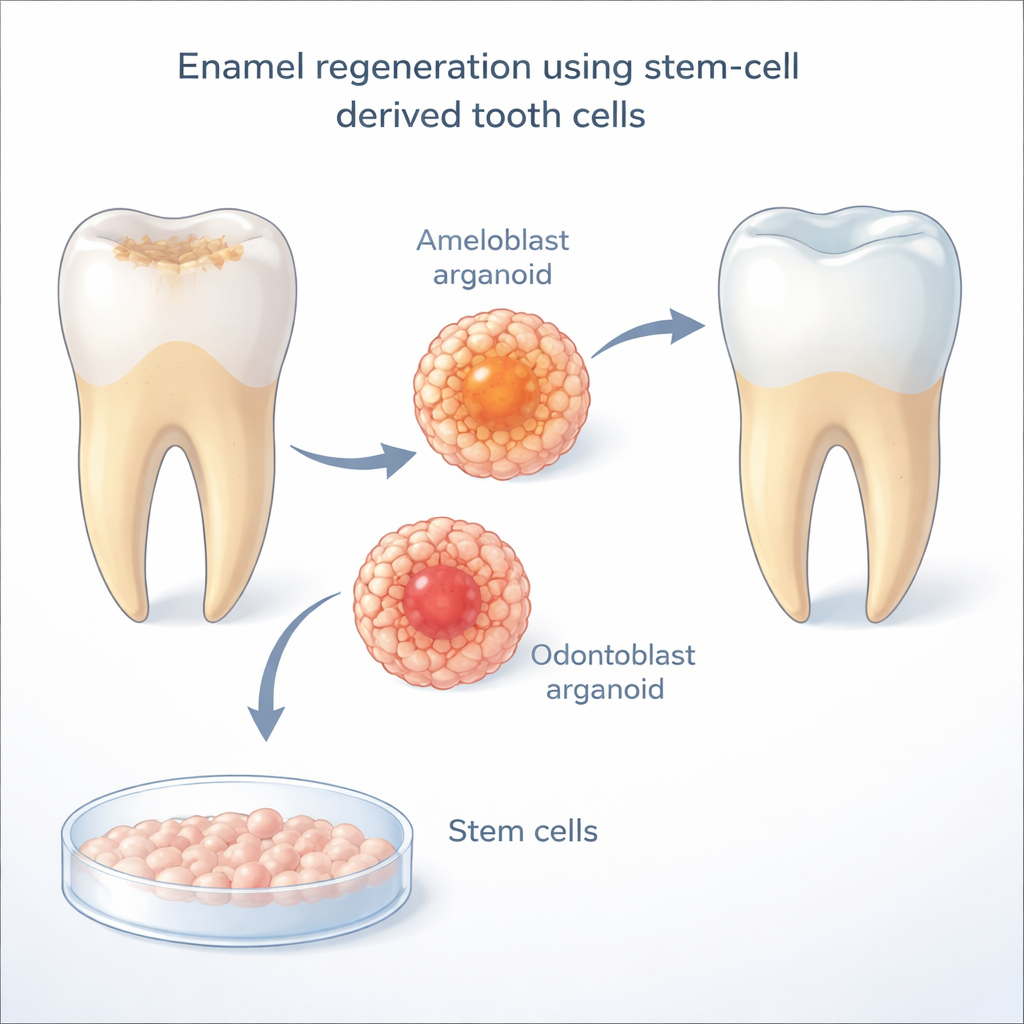
En AI‑designad proteinswitch för emaljceller
För att gå längre ville teamet slå på Notch på ett precist och kontrollerbart sätt, utan att förlita sig på riktiga odontoblaster. De använde ett artificiellt protein kallat C3‑DLL4, designat med beräkningsverktyg. Denna lösliga molekyl arrangerar tre kopior av DLL4‑signaldomänen i ett styvt, trefotat skal, vilket gör att den kan klustra och aktivera Notch‑receptorer på närliggande celler ungefär som en naturlig granncell. I rapportcellinjer slog C3‑DLL4 kraftigt på Notch‑beroende gener. När det tillfördes tidiga ameloblastorganoider — små 3D‑cellkluster odlade från stamceller — drev det en genomgripande förändring i genaktiviteten. Organoiderna skiftade från en omogen profil mot en som matchade sekretoriska och fullt mogna ameloblaster, och slog på känneteckensgener som AMELX, ENAM, MMP20, ODAM, KLK4, TUFT1 och WDR72. Att ta bort Notch‑aktivitet gav motsatt effekt, med stannad mognad och störd produktion av emaljproteiner.
Från organoider till emaljliknande vävnad
Slående nog, när dessa Notch‑aktiverade ameloblastorganoider transplanterades under njurkapseln hos immundefekta möss — en säker, välförsörjd nisch som ofta används för att testa humana vävnader — började de avsätta tät, mineraliserad material. Högupplösta mikro‑CT‑skanningar och klassiska benfärgningstekniker bekräftade närvaron av förkalkade noduli där sådan vävnad normalt inte finns. Mikroskopi visade organiserade, polariserade lager av humana celler som uttryckte nyckelproteiner för emalj och WDR72, en faktor kopplad till korrekt emaljmineralisering. Även om detta material bäst beskrivs som ”emaljliknande” snarare än fullvärdig naturlig emalj, visar det att konstruerade humana ameloblaster i princip kan avsätta hårt mineral i en levande organism. 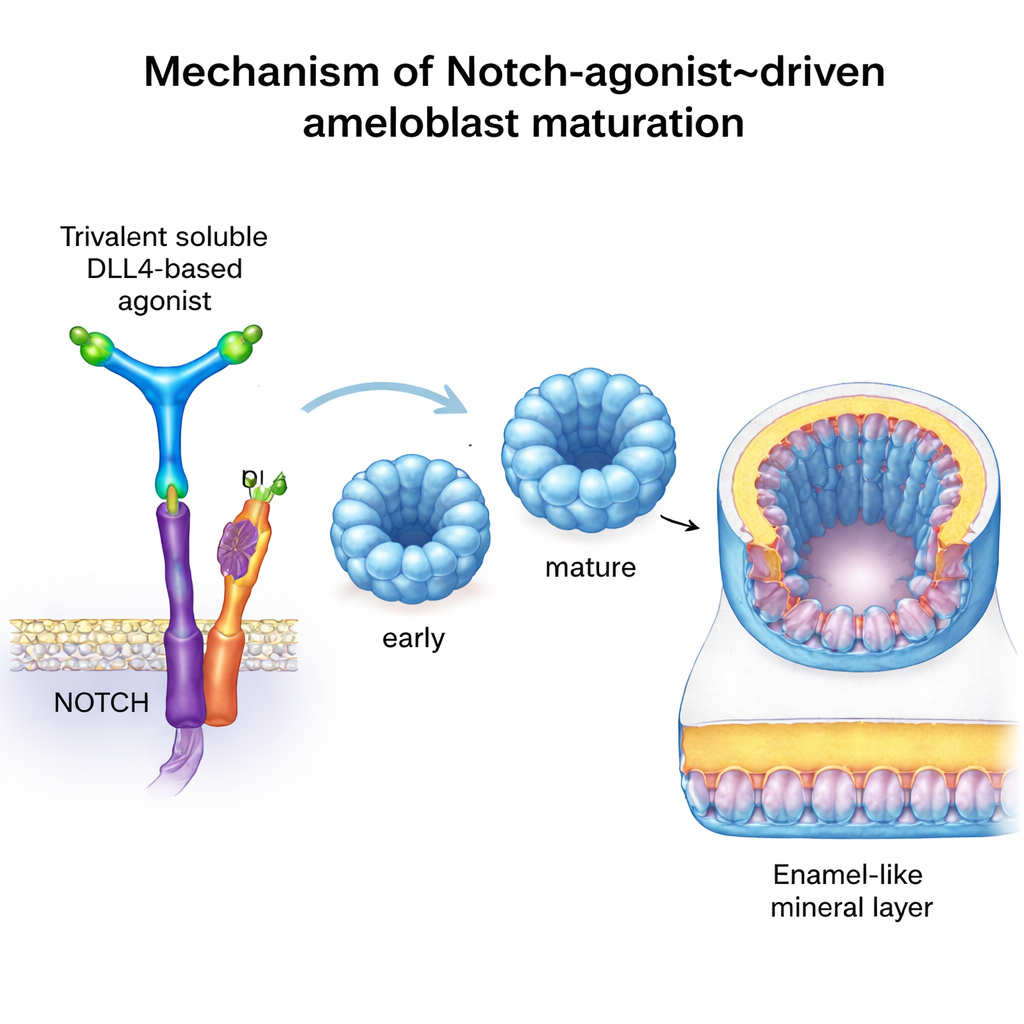
Löser en genetisk gåta bakom svag emalj
Studien tar också itu med en länge olöst gåta kring genen DLX3, vars mutationer orsakar vissa ärftliga emaljfelen och ökar kariesrisken. DLX3 är aktiv i både ameloblaster och odontoblaster, vilket gör det svårt att avgöra vilken celltyp som främst påverkas när något går fel. Genom att använda sitt odontoblastfria organoidsystem och CRISPR‑genredigering tog forskarna bort DLX3 specifikt i ameloblastlinjen. De tidiga stegen i ameloblastbildningen ägde fortfarande rum, men den slutliga mognadsfasen kollapsade: viktiga emaljproteiner såsom enamelin, AMELX, MMP20, KLK4, TUFT1 och WDR72 minskade drastiskt både på RNA‑ och proteinnivå. Detta visar att DLX3 är direkt nödvändigt inne i humana ameloblaster för att slutföra emaljbildningsprogrammet, och hjälper förklara varför varianter nära denna gen är kopplade till sköra, kariskänsliga tänder.
Vad detta kan innebära för framtida tandvård
Tillsammans beskriver dessa fynd en steg‑för‑steg‑karta från stamceller till emaljproducerande organoider till emaljliknande vävnad in vivo, kontrollerad av en justerbar Notch‑"på‑knapp" och genen DLX3. Även om klinisk tandregenerering fortfarande ligger långt fram i tiden, ger detta arbete en kraftfull testbädd för att förstå genetiska tandsjukdomar, screena nya behandlingar och finslipa strategier för att återbygga förlorad emalj med levande celler i stället för inerta material. För patienter är den långsiktiga förhoppningen att besök hos tandläkaren en dag skulle kunna innebära att slitage eller karies repareras med bioingenjörad emalj som beter sig mycket mer som det riktiga materialet.
Citering: Patni, A.P., Mout, R., Alghadeer, A. et al. Soluble Notch agonist enables human ameloblast maturation and enamel-like tissue formation for tooth regeneration. Int J Oral Sci 18, 25 (2026). https://doi.org/10.1038/s41368-026-00429-4
Nyckelord: emaljregenerering, ameloblastorganoider, Notch‑signalering, DLX3, dentala stamceller