Clear Sky Science · sv
KDM6B/Pdk1-glykolytisk vägdriven ZEB2-laktylering främjar bildandet av cellulärt cementum
Varför det är viktigt att skydda tandrötter
Gingivitsjukdom, eller parodontit, är en av de främsta orsakerna till tandförlust hos vuxna. När sjukdomen utvecklas urholkar den tyst de vävnader som förankrar tänderna i käken. En av de viktigaste är cementum, ett tunt, benliknande lager som täcker rotens yta och gör att tanden kan fästa i omgivande ligament och ben. När cementum går förlorat blir tänderna lösa och kan så småningom falla ur. Denna studie ställer en enkel men kraftfull fråga: kan vi förstå på molekylär nivå hur cementum byggs, så att vi en dag kan hjälpa kroppen att återskapa det och behålla tänderna på plats livet ut?
Från tandstödceller till ett läkande mål
Cementum bildas av specialiserade celler kallade cementoblaster, som sitter på rotytan och avsätter ny mineral. Dessa celler beter sig mycket som benceller, men de signaler som talar om när och hur de ska bygga cementum har hittills varit dåligt förstådda. Forskarna fokuserade på ett molekylärt verktyg kallat KDM6B, ett enzym som redigerar kemiska markörer på DNA‑paketerande proteiner och kan slå på gener. Genom att studera mösständer i olika åldrar och cementoblaster odlade i labbet fann de att KDM6B‑nivåerna stiger under den aktiva fasen för cementumbildning och sjunker när tillväxten avtar. När de blockerade KDM6B i celler eller i möss minskade cementoblastaktiviteten och den ”cellulära” delen av cementum – den tjockare, levande delen nära rotspetsen – blev tunnare, vilket tyder på att KDM6B är en nyckelfaktor för frisk cementumtillväxt.
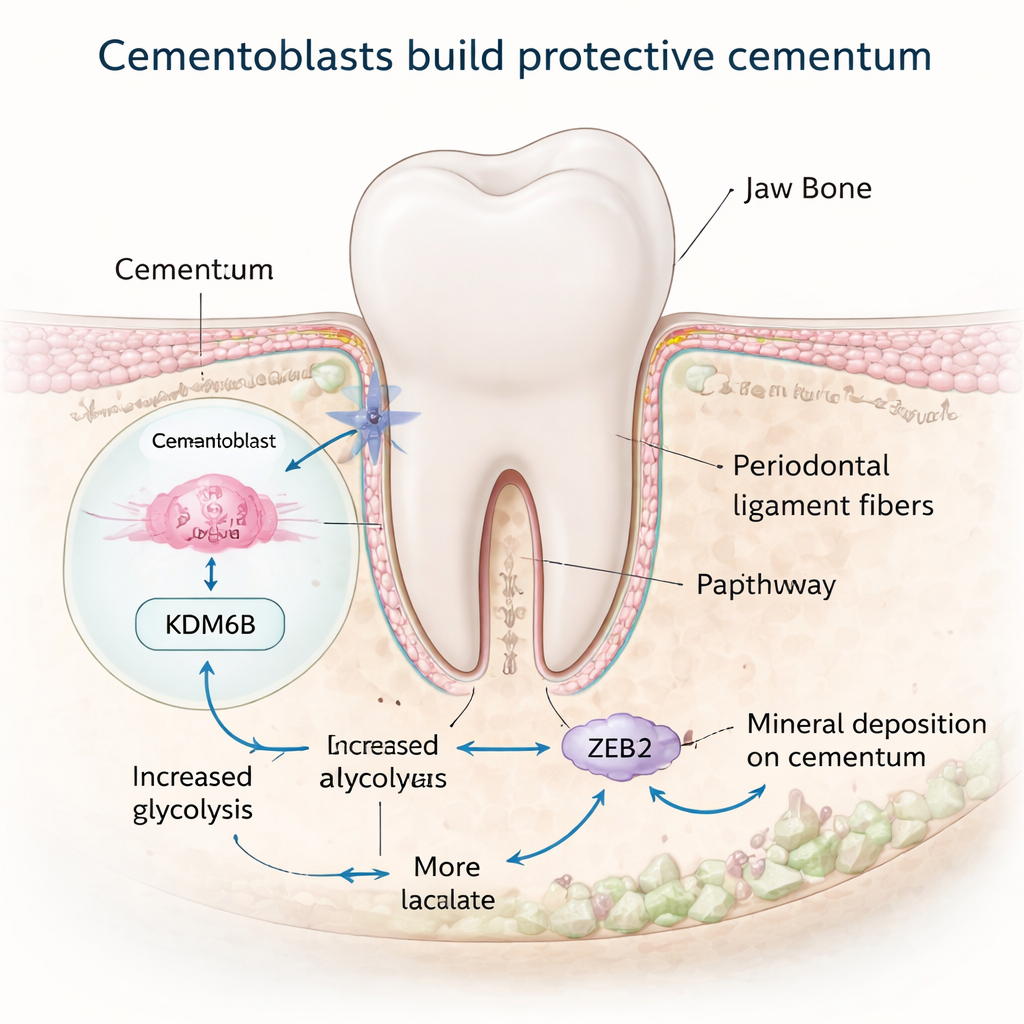
Omskola cellernas metabolism för att bygga mineral
Att bygga mineraliserad vävnad kräver mycket energi, och många celler växlar till ett särskilt högpresterande metaboliskt läge när de gör det. Teamet upptäckte att KDM6B hjälper cementoblaster att omprogrammera hur de använder socker. Normalt föredrar dessa celler en bana som kallas glykolys, som snabbt bryter ner glukos och producerar laktat. När KDM6B reducerades nedreglerades gener som är involverade i glykolys, medan gener kopplade till långsammare, syreberoende energiproduktion var blandade eller ökade, och cellerna producerade mindre energi totalt. En central aktör i detta skifte var enzymet PDK1. Genom att använda genomkartläggning visade forskarna att KDM6B fysiskt tar bort en repressiv markör från DNA‑regionen som styr Pdk1‑genen, vilket tillåter PDK1‑nivåerna att stiga. Återställande av PDK1 i KDM6B‑defekta celler återförde många markörer för mineralbildning, vilket avslöjar en KDM6B–PDK1‑metabolomkoppling som driver cementoblaster.
Gör laktat från avfall till ett användbart signalämne
Laktat uppfattas ofta som en avfallsprodukt från hårt arbetande muskler, men nyare forskning visar att det också kan fungera som en signal som modifierar proteiner. Här ökade högre glykolys som drevs av KDM6B och PDK1 laktatproduktionen i cementoblaster. Forskarna följde sedan en ny typ av proteinmodifikation kallad laktylering, där laktat‑deriverade markörer fästs vid specifika ställen på proteiner. De fann att laktyleringsnivåerna i cementoblaster steg under perioder med aktiv cementumbildning och sjönk i äldre möss och i KDM6B‑defekta celler. Tillsats av enkelt natriumlaktat ökade laktyleringen, återupplivade mineralrelaterade gener och återställde bildningen av mineralnoder både i cellodlingar och i en musmodell, även när KDM6B var blockerat. Det tyder på att laktat i sig kan hjälpa till att rädda försvagad cementum‑byggande aktivitet.
En molekylär förstärkning för en viktig cementumregulator
Teamet undersökte därefter vilka proteiner som blev ”dekorerade” med laktat på ett sätt som påverkade cementum. De inriktade sig på ZEB2, ett genregleringsprotein som redan är känt för att främja cementoblastmineralisering. Genom proteinkartläggning identifierade de specifika platser på ZEB2 som bär laktyleringsmärken och visade att förändring av en kritisk plats försvagade cellens förmåga att slå på mineraliseringsgener. Ytterligare experiment visade att KDM6B–PDK1‑vägen ökar ZEB2‑laktylering och att tillskott av extra laktat kan återställa ZEB2:s aktivitet när PDK1 är låg. I huvudsak kopplas metabolism och genreglering: sockernedbrytning driver laktatproduktion, vilket sedan finjusterar ZEB2 för att hålla igång programmen för cementumbildning.
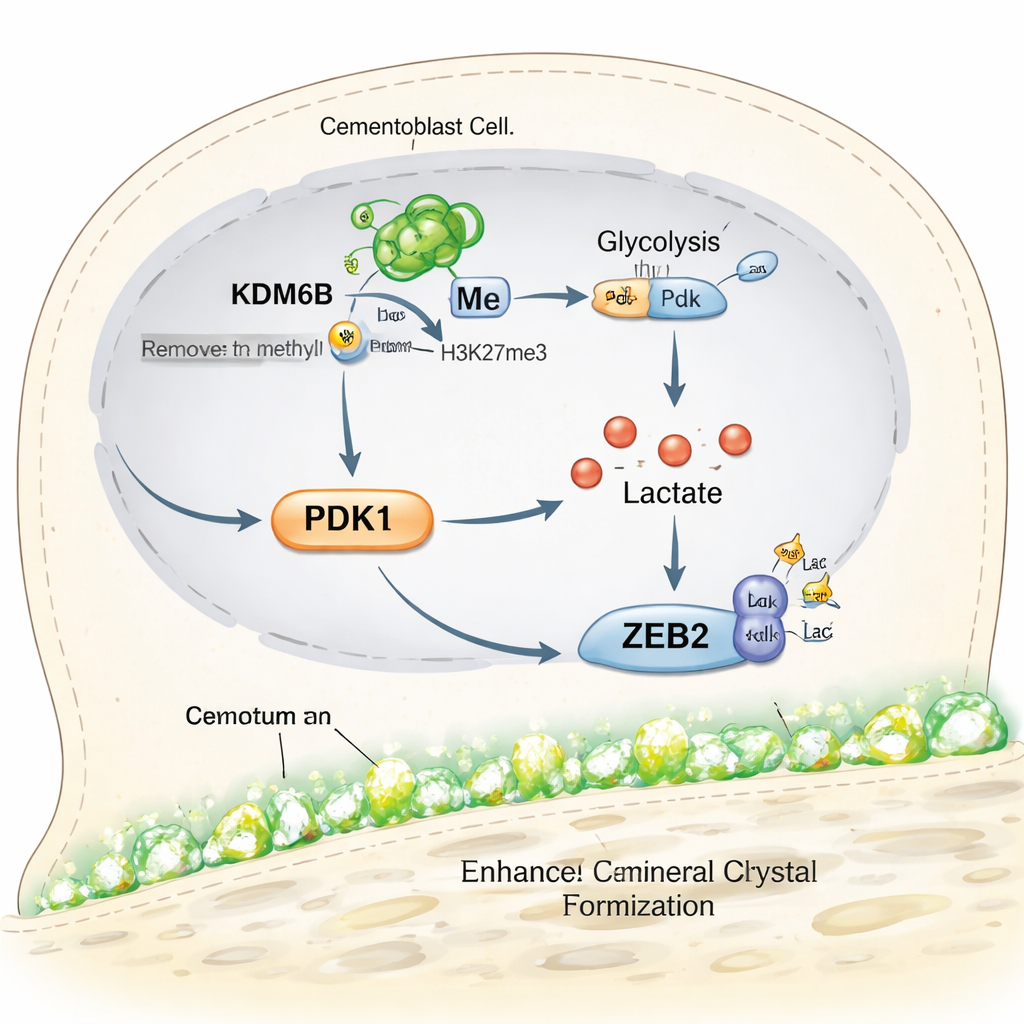
Vad detta innebär för framtida tandbevarande behandlingar
Kort sagt visar studien en händelsekedja inne i cementumbildande celler: enzymet KDM6B öppnar upp Pdk1‑genen, PDK1 driver cellerna mot snabb sockeranvändning, den metabolismen genererar laktat, och laktat kemiskt finjusterar ZEB2‑proteinet för att driva mineralavsättning. När något steg i denna kedja blockeras försämras cementumtillväxten, men noggrant tillsatt laktat kan delvis återställa den. För patienter innebär detta ännu ingen klinisk behandling, men arbetet lyfter fram nya, precisa mål för läkemedel eller biomaterial avsedda att regenerera cementum och stabilisera tänder vid avancerad parodontit. Det tyder också på att liknande metabola ”omkopplare” skulle kunna utnyttjas för att främja benläkning på andra ställen i kroppen.
Citering: Yang, Z., Wang, H., Xiao, J. et al. KDM6B/Pdk1 glycolytic pathway-driven ZEB2 lactylation promotes cellular cementum formation. Int J Oral Sci 18, 21 (2026). https://doi.org/10.1038/s41368-025-00420-5
Nyckelord: regenerering av cementum, parodontit, cementoblastmetabolism, histondemethylas KDM6B, proteinklakylering