Clear Sky Science · sv
Strukturella insikter i sjukdomsassocierade mutationer i mikroRNA‑bearbetningsmaskineriet
Hur små RNA‑saxar formar hälsa och sjukdom
Inne i varje cell finns ett dolt redigeringssystem som trimmar genetiska budskap innan de läses. Det systemet förlitar sig på små RNA‑snuttar kallade mikroRNA, som fungerar som finjusteringsknappar för tusentals gener samtidigt. När de molekylära ”maskinerna” som tillverkar mikroRNA fungerar korrekt växer, delar sig och specialiserar sig celler på ett kontrollerat sätt. Men när dessa maskiner skadas av mutationer kan balansen i genaktivitet förskjutas mot cancer, blodsjukdomar eller problem i hjärnans utveckling. Denna artikel förklarar hur kunskap om dessa maskiners tredimensionella former hjälper forskare att peka ut vad som går fel och hur det kan åtgärdas.
Cellens verktygslåda för att dämpa gener
MikroRNA är korta RNA‑stycken, ungefär 22 byggstenar långa, som inte själva kodar för proteiner. Istället fäster de vid längre budbärar‑RNA och antingen märker dem för nedbrytning eller blockerar deras översättning, vilket effektivt dämpar genuttryck snarare än att stänga av det helt. För att skapa dessa mikroRNA förvandlas längre RNA‑prekursorer i en noggrant uppdelad monteringskedja. Först trimmar enzymet DROSHA de skrymmande primära transkripten i cellkärnan till kortare hårnålsformade bitar. Dessa flyttas sedan till cytoplasman, där ett annat enzym, DICER, mäter och klipper dem till mikroRNA‑stora duplexer. Slutligen laddas en sträng av varje duplex in i ett protein som kallas Argonaute 2 (AGO2), som använder mikroRNA:t som en vägvisare för att hitta matchande budskap och tysta dem. 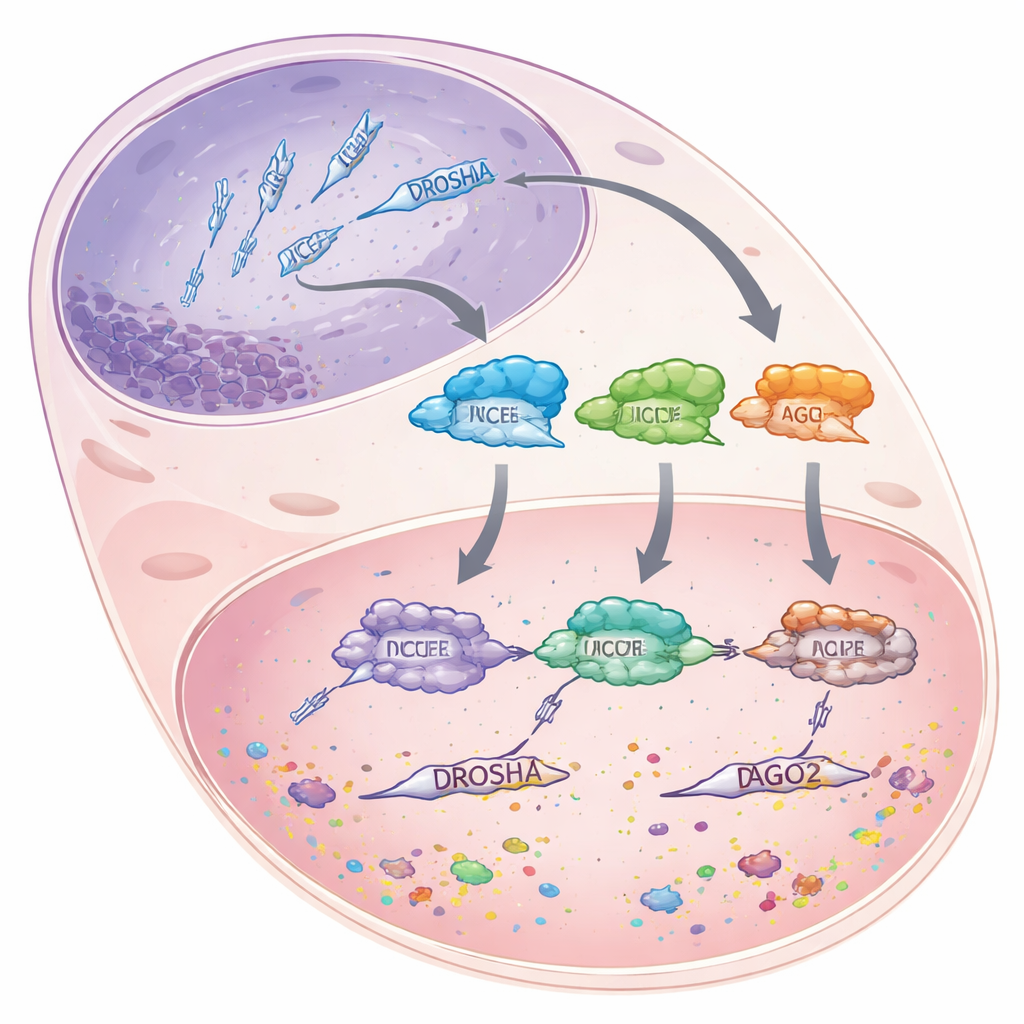
Sköra former med precisa uppgifter
DROSHA, DICER och AGO2 är inte enkla saxar; var och en byggs av flera samverkande delar som måste röra sig i en koreograferad ordning. DROSHA arbetar tillsammans med ett partnerprotein, DGCR8, för att gripa ändarna på en primär mikroRNA‑hårnål och avgöra exakt var klippet ska ske. DICER använder en slags inbyggd linjal formad av sina domäner för att ställa in ett fast avstånd mellan där den håller hårnålens ände och där dess katalytiska centrum gör snittet. AGO2 omsluter en enkel mikroRNA‑sträng så att dess ”seed”‑region exponeras perfekt för att känna igen mål‑budskap, medan metalljoner och nyckelaminosyror i dess kärna är i linje för att skära dessa mål när parningen är tillräckligt stark. I alla tre proteiner guidar positivt laddade fåror och flexibla länkar RNA‑strängarna på plats medan metallbindande fickor och katalytiska rester utför de kemiska snitten.
När saxarna böjs eller blir trubbiga
Genetiska studier hos patienter med cancer, blodsjukdomar och neurodevelopmentella syndrom har avslöjat kluster av mutationer i dessa mikroRNA‑maskiner. Många av de mest skadliga förändringarna ligger direkt i katalytiska centra eller i täta RNA‑greppytor. I DROSHA, till exempel, sitter substitutioner som E1147K och D1219G i kärnan av skärplatsen och stör förmågan att hålla nödvändiga metalljoner, vilket lämnar enzymet oförmöget att bearbeta primära mikroRNA. Andra DROSHA‑mutationer, såsom truncationer som tar bort klippdelen eller förändringar som destabiliserar dess stödhelixar, försvagar hela komplexet och orsakar globala sänkningar av mikroRNA‑nivåer i Wilms tumör, benmärgssjukdomar och sjukdomar i nervsystemet. I DICER klustras återkommande mutationer i ett av dess två klippdomäner, vilket snedvrider produktionen så att ena armen av mikroRNA‑duplexen går förlorad och därmed förskjuter balansen mellan tillväxtfrämjande och tillväxthämmande signaler. 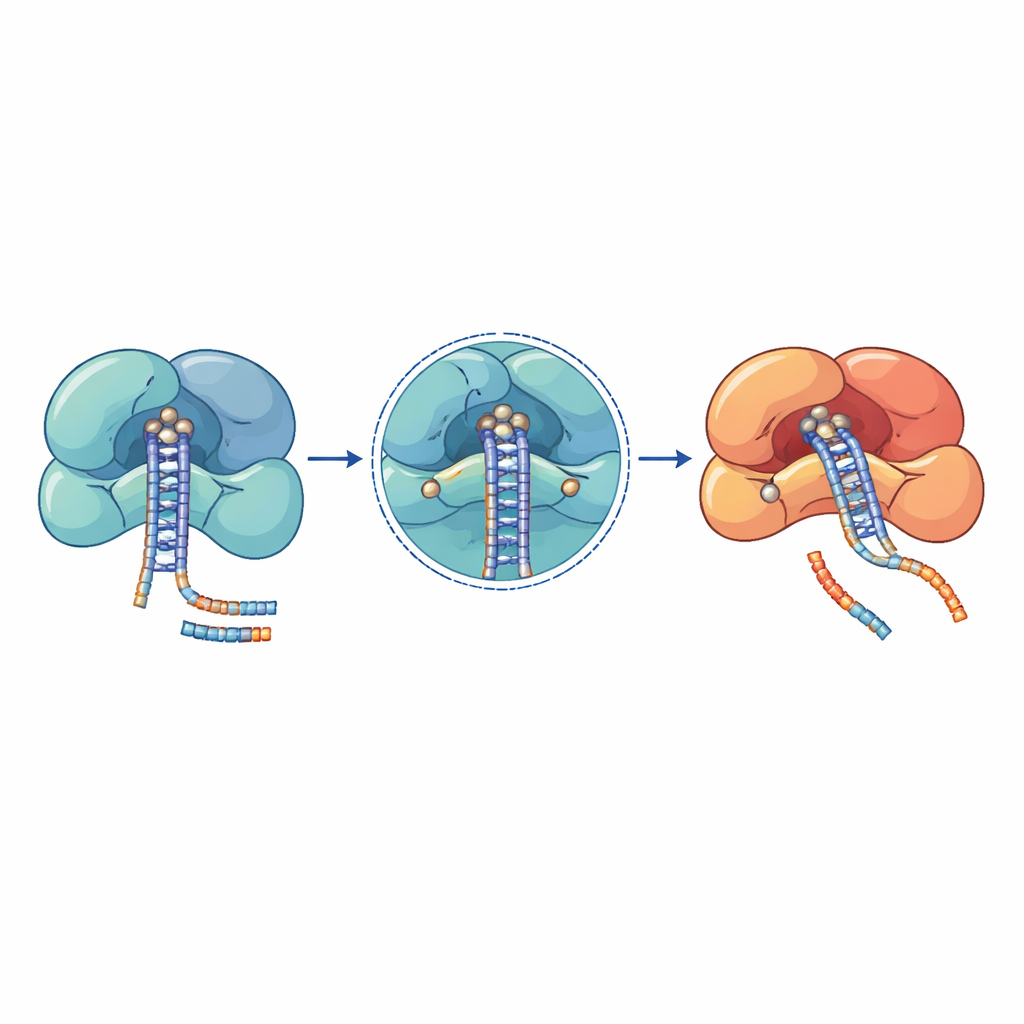
Feljusterade vägvisare i hjärnan och bortom
AGO2‑mutationer berättar en annorlunda men besläktad historia. Direkt träff mot dess katalytiska kärna är sällsynt, troligen eftersom sådana förändringar skulle vara dödliga tidigt i utvecklingen. Istället tenderar sjukdomsassocierade varianter att dyka upp i flexibla länkområden och vid domänskjutfogar som håller ihop AGO2:s form. I Lessel–Kreienkamp‑syndromet, ett neurodevelopmentellt tillstånd, vrider mutationer i dessa länkar och omgivande ytor subtilt hur PAZ, MID och PIWI‑delarna av AGO2 packas och rör sig. Detta kan feljustera guide‑mikroRNA:t eller försvaga dess grepp om mål‑RNA, vilket suddar ut precisionen i gensänkningen under hjärnans utveckling. Liknande strukturella förändringar var som helst i mikroRNA‑vägen — vare sig i DROSHA, DICER eller AGO2 — kan få genomslag och ändra hela nätverk av gener involverade i celltillväxt, blodbildning eller neuronal kopplingsbildning.
Att omvandla strukturella ledtrådar till framtida behandlingar
Genom att lägga sjukdomsmutationer över högupplösta 3D‑kartor av dessa proteiner kan forskare kategorisera exakt hur varje förändring orsakar problem — vare sig genom att slöa ner skärets egg, luckra upp kritiska kontakter med partnerproteiner eller böja viktiga helixar ur riktning. Dessa strukturella insikter öppnar dörren för riktade interventioner: små molekyler som stabiliserar försvagade gränssnitt, designade RNA som styr delvis funktionella enzymer tillbaka mot rätt substrat, eller allosteriska föreningar som knuffar muterade proteiner i mer aktiva former. För en lekmannaläsare är huvudbudskapet att små strukturella justeringar i cellens RNA‑saxar kan få oproportionerligt stora effekter på hälsan, men de ger också precisa handtag för att utforma nästa generations mutationsoch medvetna terapier.
Citering: Lee, H., Lee, J. & Roh, SH. Structural insights into disease-associated mutations in the microRNA processing machinery. Exp Mol Med 58, 639–649 (2026). https://doi.org/10.1038/s12276-026-01669-4
Nyckelord: mikroRNA, RNA‑interferens, DROSHA DICER AGO2, cancergenetik, neurodevelopmentella störningar