Clear Sky Science · sv
Reglerande mekanismer för Snail-protinstabilitet: ubiquitin–proteasomsystemet och chaperonmedierad autofagi
Varför cancerens spridning hänger på ett bräckligt protein
Cancer blir verkligen livshotande när celler lossnar från den ursprungliga tumören och färdas till avlägsna organ. Denna spridning, eller metastas, är delvis beroende av ett kraftfullt ”mästarknapp”-protein kallat Snail, som hjälper celler att luckra upp sina förbindelser och bli mer rörliga. Den här artikeln förklarar hur våra celler normalt håller Snail i kort koppel genom att snabbt bryta ner det via två huvudsakliga avfallshanteringssystem. Att förstå denna balans ger nya idéer för att bromsa eller förhindra metastas.
Från tätt packade celler till kringvandrande inkräktare
I friska vävnader bildar epitelceller ordnade, tegelstensliknande lager som sitter stilla och håller fast vid sina grannar. För att en tumörcell ska kunna fly måste den ofta genomgå en omvandling kallad epitelial–mesenkymal övergång, eller EMT, där den förlorar sina täta kontakter och får förmågan att röra sig och invadera. Snail är en nyckeldrivkraft i denna omvandling: när det finns i cellkärnan släcker det av gener som upprätthåller cell–cell-adhesion och slår på gener som gynnar rörelse och invasion. Höga nivåer av Snail är kopplade till aggressiva cancerformer och sämre patientutfall, så celler har utvecklat sätt att hålla Snail sparsamt och kortlivat under normala förhållanden.
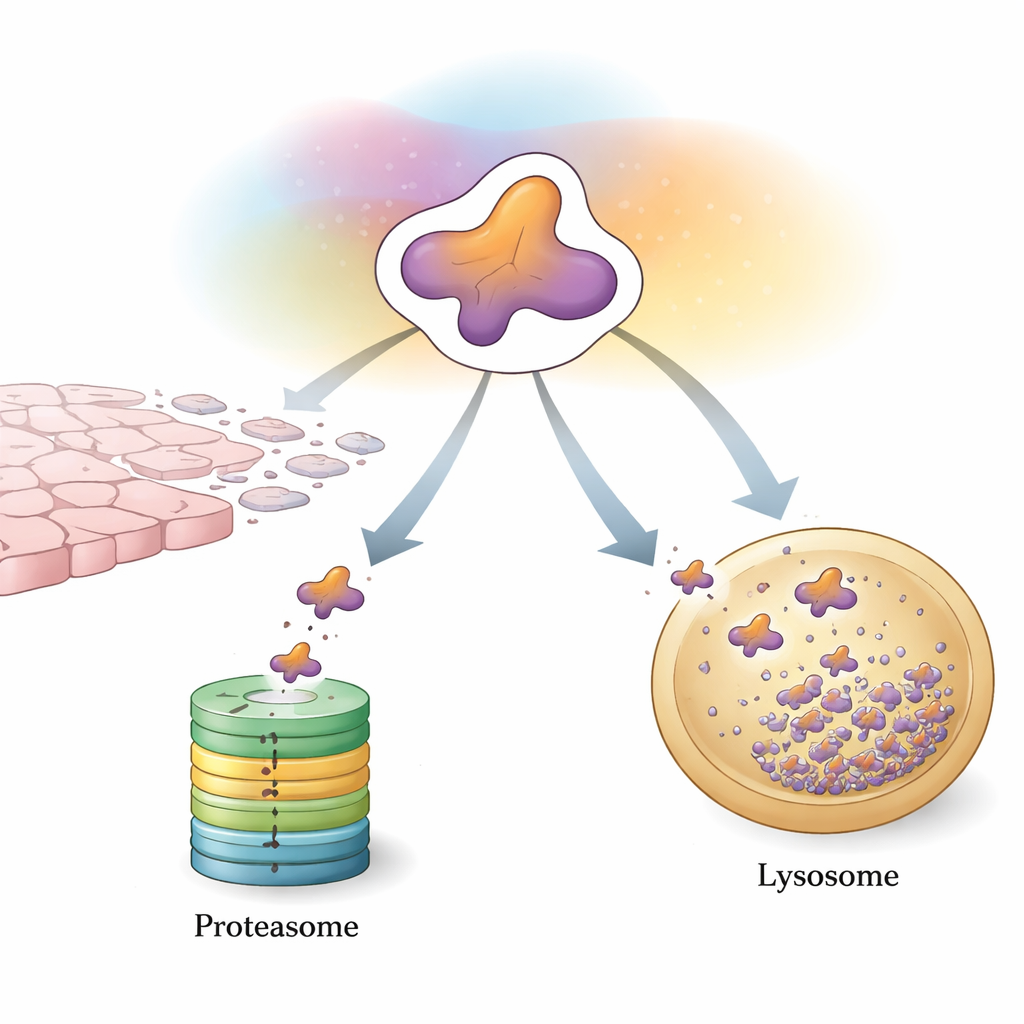
Cellens första kontrollinje: märk och mala ner
Ett huvudsakligt sätt celler kontrollerar Snail är genom ubiquitin–proteasomsystemet, en märk-och-mala-maskin för oönskade proteiner. Specialiserade enzymer sätter fast små ”flaggor” gjorda av ett protein kallat ubiquitin på Snail. När tillräckligt många av dessa flaggor har samlats i ett visst mönster styrs Snail mot proteasomen, ett tunnformigt komplex som finfördelar det. En stor skara hjälpproteiner finslipar denna process. Vissa enzymer fäster kedjor som främjar nedbrytning och snabbt skickar Snail till malverket, vilket hjälper till att hämma tumörtillväxt och spridning. Andra lägger istället kedjor som stabiliserar Snail eller indirekt ökar dess genproduktion och tippar balansen mot EMT och metastas. Kemiska modifieringar som fosforylering och acetylering fungerar som extra brytare, och styr vilka hjälpande proteiner som kan binda Snail och om det kommer att förstöras eller sparas.
Ta bort bromsarna: enzymer som räddar Snail
Berättelsen slutar inte med att märka Snail för nedbrytning. En annan grupp enzymer, kallade deubiquitinaser, kan ta bort ubiquitin-flaggorna och rädda Snail från proteasomen. Många av dessa enzymer är uppreglerade eller förstärkta i cancer, vilket gör att Snail undkommer nedbrytning och kvarstår i kärnan. Deras verkan beror starkt på cellulärt sammanhang: i vissa situationer stabiliserar de direkt Snail, medan de i andra påverkar var Snail befinner sig i cellen eller hur det interagerar med partnerproteiner. Signaler från cancerassocierade vägar, såsom tillväxtfaktorer och stressreaktioner, matar in i detta nätverk och avgör om Snail snabbt ska avlägsnas eller tillåtas driva EMT-programmet.
En andra säkerhetsnät: selektiv leverans till cellens återvinningscentral
Bortom proteasomen förlitar sig celler på autofagi, en samling vägar som transporterar proteiner till sura kompartment kallade lysosomer för nedbrytning. Denna översikt belyser en högst selektiv form känd som chaperonmedierad autofagi (CMA) som en andra stor väg för att kontrollera Snail. CMA känner igen en kort sekvens inom Snail och, med hjälp av eskortproteiner, levererar cytoplasmatiskt Snail in i lysosomer för förstörelse. I mindre aggressiva bröstcancerceller håller detta system Snail till stor del utanför kärnan och mottagligt för lysosomal borttagning. I mer aggressiva, trippelnegativa bröstcancerformer tenderar Snail att ackumuleras i kärnan och kringgå CMA, vilket stärker dess förmåga att utlösa EMT och metastas.
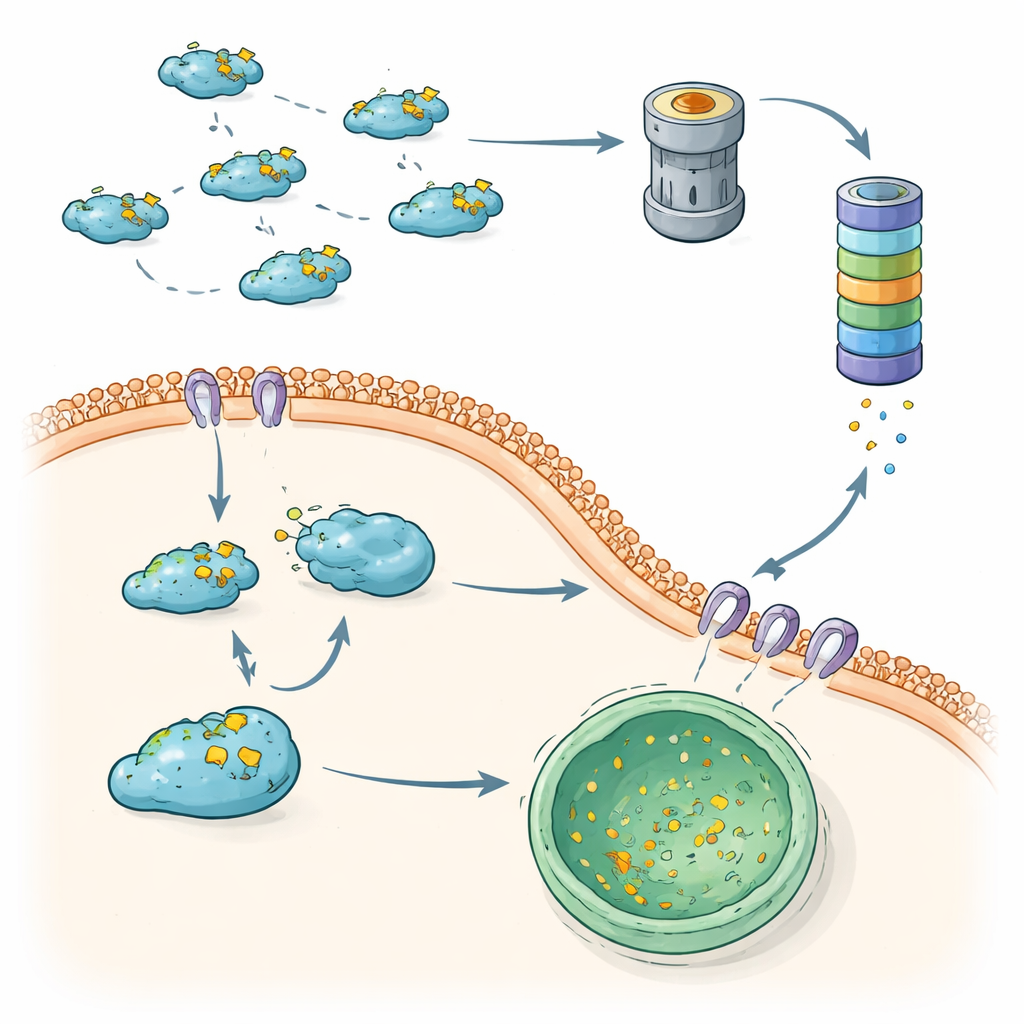
När kvalitetskontrollen fallerar vinner metastasen mark
Tillsammans visar dessa fynd att celler använder två kompletterande ”kvalitetskontroll”-axlar för att begränsa Snail: ubiquitin–proteasomvägen och CMA-baserad lysosomal nedbrytning. När båda fungerar som de ska omsätts Snail snabbt, vilket begränsar EMT och hjälper till att förhindra att tumörceller sprider sig. När någon av axlarna försvagas—genom förändringar i märkningsenzym, deubiquitinaser eller CMA-komponenter—blir Snail mer stabilt, ackumuleras i kärnan och främjar starkt invasivt beteende. Genom att kartlägga dessa sammanlänkade nedbrytningsvägar skisserar artikeln nya terapeutiska möjligheter: läkemedel som återställer eller förstärker Snail-nedbrytning, eller som dirigerar Snail tillbaka mot CMA- eller proteasomal nedbrytning, skulle kunna hjälpa till att återinsätta bromsen på metastas utan att helt stänga av dessa viktiga system för proteinåtervinning.
Citering: Kim, M., Hong, KS., Kim, T. et al. Regulatory mechanisms for Snail protein stability: ubiquitin–proteasome system and chaperone-mediated autophagy. Exp Mol Med 58, 408–415 (2026). https://doi.org/10.1038/s12276-026-01667-6
Nyckelord: cancermetastas, epitelial–mesenkymal övergång, Snail-protein, proteinnedbrytning, autofagi