Clear Sky Science · sv
Metabolisk korsprat mellan cancerassocierade fibroblaster, adipocyter och immunceller som en immunosuppressiv drivkraft i tumörmikromiljön
Varför tumörens omgivning spelar roll
Cancer växer inte i isolering. Den lever i ett livligt kvarter av stödjeceller, fettceller och immunceller som ständigt byter näringsämnen och kemiska signaler sinsemellan. Denna artikel förklarar hur den omgivningens "metabolism" – hur celler använder och delar bränsle – tyst skiftar fördelarna till tumören och mot immunsystemet. Att förstå denna dolda ekonomi av sockerarter, fetter och aminosyror öppnar nya vägar för att förbättra immunterapier och att slå mot tumörens stödsystem.
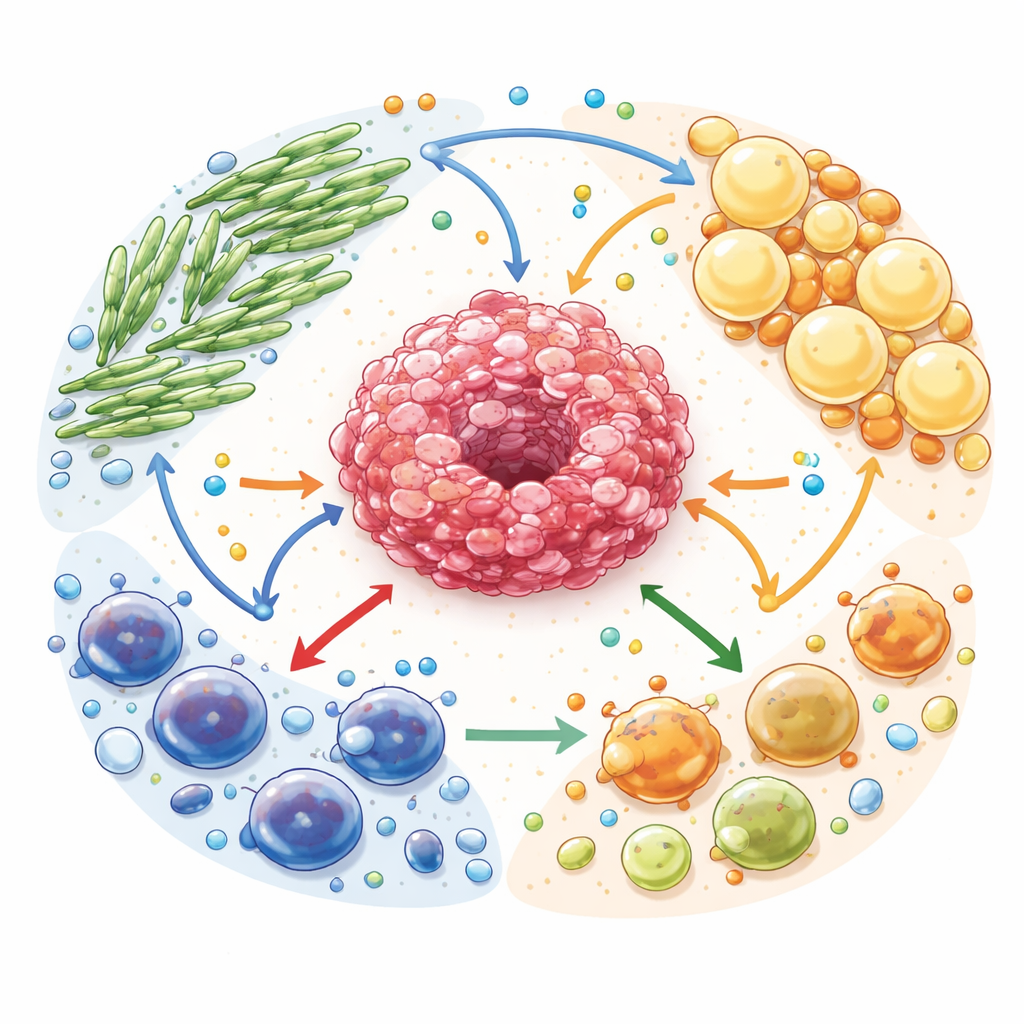
Bränsledelning i ett cancerekosystem
Författarna beskriver tumörmikromiljön som ett komplext ekosystem. Cancerceller omges av cancerassocierade fibroblaster (ärrliknande stödjeceller), cancerassocierade adipocyter (omprogrammerade fettceller) och många typer av immunceller. Alla dessa celler konkurrerar om och utbyter bränslen såsom glukos, fettsyror och aminosyror. Men denna handel är inte neutral: stödjeceller omprogrammeras för att bryta ner sina egna förråd och exportera energirika molekyler som matar cancerceller. Samtidigt ansamlas avfallsnära biprodukter, inklusive laktat och adenosin, som fungerar som kraftfulla signaler som försvagar skyddande immunceller samtidigt som de gynnar dem som dämpar immunangrepp.
Hur fettceller hjälper tumörer och hindrar försvaret
Närliggande fettdepåer gör mycket mer än att lagra kalorier. Under påverkan av tumörsignaler och låg syrehalt omvandlas vanliga fettceller till cancerassocierade adipocyter. De krymper sina fettdroppar, ökar fettnedbrytningen och spyr ut fria fettsyror, inflammatoriska molekyler och små vesiklar fyllda med last. Cancerceller importerar dessa fetter girigt och förbränner dem i sina mitokondrier, vilket ger en flexibel, långvarig energikälla som hjälper dem att överleva stress, sprida sig och motstå behandling. Immunceller i fettfyllda regioner har det sämre: cytotoxiska T‑celler och natural killer‑celler överbelastas av fetter, drabbas av oxidativ stress och glider in i ett "utmattat" tillstånd med förminskad förmåga att förstöra tumörceller. Däremot trivs regulatoriska T‑celler och vissa myeloida celler på dessa lipider, blir mer suppressiva och dämpar ytterligare immunsvaren.
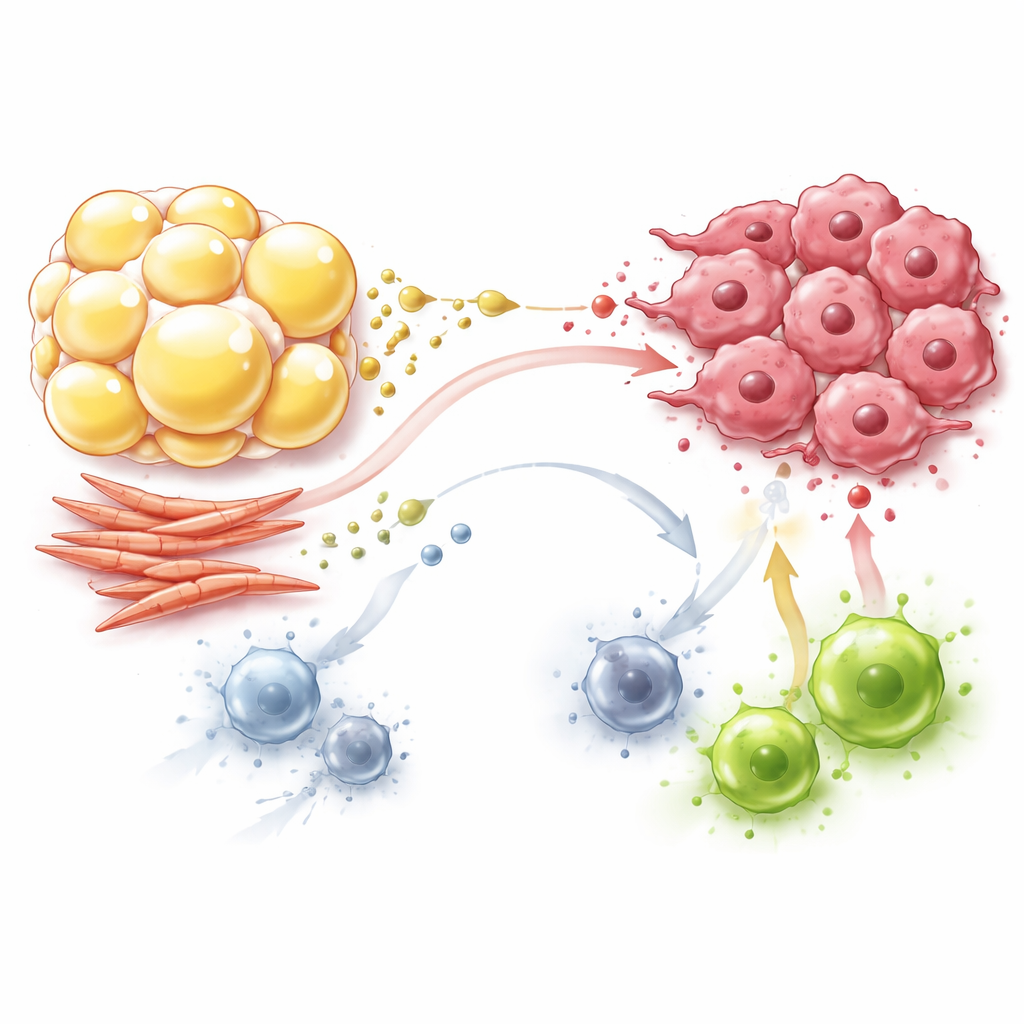
Fibroblaster: byggare som också omkopplar metabolismen
Fibroblaster, länge kända som byggare av ärrliknande vävnad runt tumörer, är också aktiva aktörer i detta metaboliska drama. Cancerassocierade fibroblaster skiftar mot socker‑hungrigt beteende och omvandlar stora mängder glukos till laktat och pyruvat även när syre finns tillgängligt. De exporterar dessa produkter ut i omgivningen där cancerceller återanvänder dem som bränsle för sina egna kraftverk och sparar glukos till tillväxt. Fibroblaster tillverkar och byter också aminosyror såsom glutamin, prolin och asparagin, vilka stödjer både tumörens struktur och dess tillväxt under näringsstress. Samtidigt konsumerar fibroblaster nyckelnäringsämnen och frigör laktat, vilket tränger undan effektor‑T‑celler som är beroende av glukos och driver makrofager och T‑celler mot mer toleranta, mindre aggressiva tillstånd.
Immunceller fångade i en metabolisk fälla
Immunsystemet inne i tumörer formas lika mycket av bränsletillgång som av antigener. Cytotoxiska T‑celler och natural killer‑celler, som behöver snabb sockerförbränning för att driva sitt angrepp, befinner sig i ett landskap avskuret från glukos och översvämmat av laktat, fetter och andra suppressiva metaboliter. Deras motorer stannar, deras mitokondrier skadas och hämmande "bromsar" på deras ytor ökar. Samtidigt är regulatoriska T‑celler och tumörassocierade makrofager väl anpassade till denna hårda miljö. De föredrar fettförbränning och oxidativ metabolism, vilket tillåter dem att frodas där andra misslyckas. Stödda av fibroblaster och adipocyter förstärker dessa celler ett tolerant, sårliknande tillstånd som skyddar tumören och dämpar effekten av checkpoint‑hämmare och andra immunterapier.
Att vända metabolismen till ett terapeutiskt mål
Översikten lyfter fram en växande verktygslåda av experimentella läkemedel utformade för att störa detta stödnätverk utan att enbart förgifta delande celler. Vissa strategier syftar till att blockera fettsläpp från adipocyter eller fettupptag och förbränning i cancerceller. Andra riktar sig mot fibroblastdrivna vägar som genererar laktat, omformar matrisen eller lockar suppressiva myeloida celler. Genom att sänka laktatnivåer, blockera specifika bränsletransportörer eller omprogrammera lipidkänsliga omkopplare inuti celler försöker dessa strategier återställa glukostillgång och mitokondriehälsa hos utmattade T‑ och natural killer‑celler. Det yttersta målet är inte bara att svälta ut tumören, utan att "omskola" dess omgivning så att immunceller återigen ser, når och effektivt angriper cancerceller.
Citering: Kim, T.H., Lim, S.H., Lee, H. et al. Metabolic crosstalk among cancer-associated fibroblasts, adipocytes and immune cells as an immunosuppressive tumor microenvironment driver. Exp Mol Med 58, 366–381 (2026). https://doi.org/10.1038/s12276-026-01650-1
Nyckelord: tumörmikromiljö, cancermetabolism, cancerassocierade fibroblaster, cancerassocierade adipocyter, tumörimmunosuppression