Clear Sky Science · sv
PAK4 vid metabola sjukdomar: reglering av näringssignaler och terapeutiska konsekvenser
Varför en cellulär strömbrytare spelar roll för vardagshälsan
Fetma, typ 2‑diabetes och fettlever tillskrivs ofta enbart kalorier, men djupt inne i våra celler avgör molekylära strömbrytare om vi förbränner eller lagrar bränsle. Denna översikt fokuserar på en sådan brytare, ett protein kallat PAK4, och förklarar hur det svarar på förändrade närings‑ och hormonella signaler och omformar ämnesomsättningen i fett, lever och muskler. Att förstå detta dolda styrsystem kan öppna dörren för nya behandlingar som tar itu med flera metabola sjukdomar samtidigt snarare än att behandla ett symtom i taget. 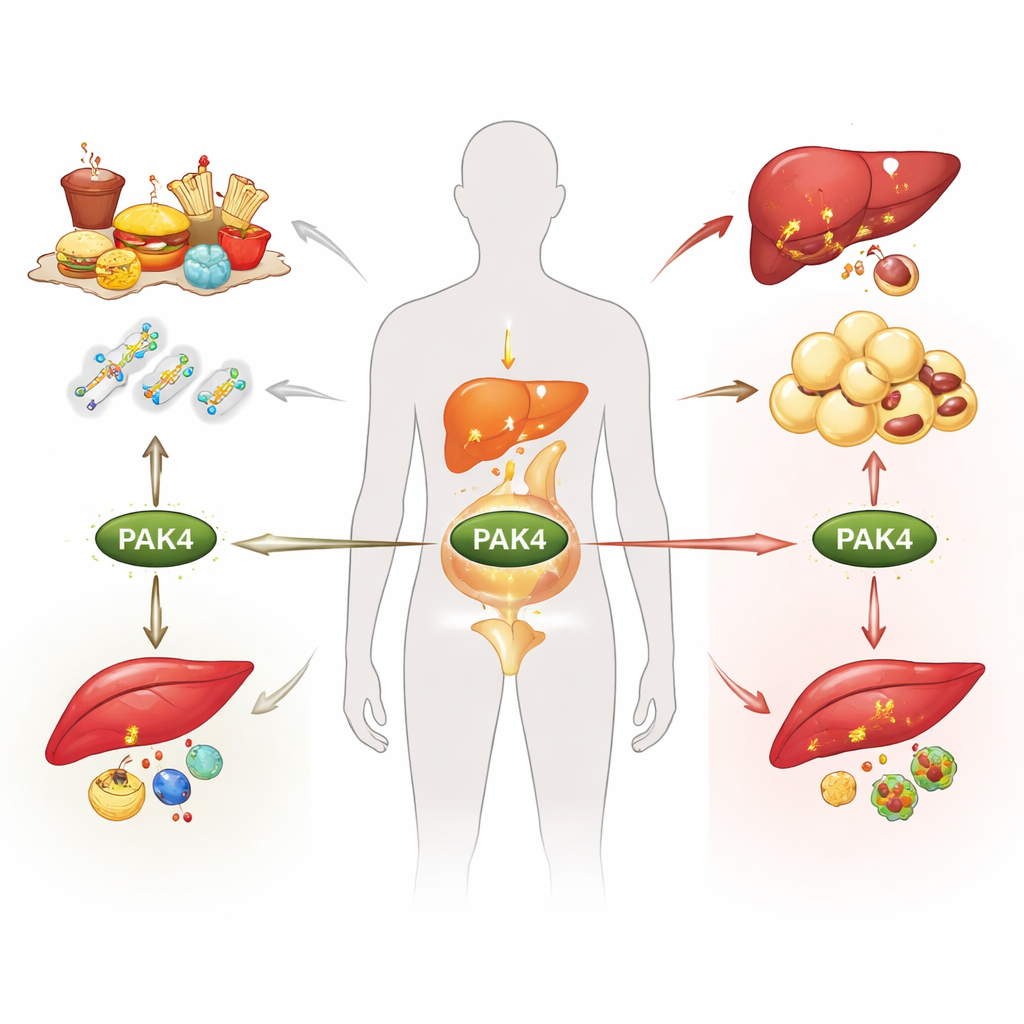
En huvudströmbrytare dold i våra celler
PAK4 tillhör en familj av enzymer som förmedlar signaler från små molekylära ”budbärare” inne i cellerna. Under friska förhållanden finns PAK4 på låga nivåer i kroppens stora metabola organ. När energibalansen rubbas, som vid fetma eller typ 2‑diabetes, ökar dess nivåer i fettväv, lever och skelettmuskulatur. PAK4:s aktivitet styrs på flera sätt: av uppströms budbärare som ändrar dess form och av kemiska märken som läggs till eller tas bort efter att proteinet bildats. Dessa inkluderar fosfatmärken som antingen kan slå på PAK4 eller markera det för destruktion, samt märken som påverkar hur stabilt eller aktivt det är. Fasta, födointag, hormoner och stress påverkar alla dessa märkningar, så PAK4 i praktiken ”känner av” kroppens näringstillstånd och förmedlar den informationen till centrala metabola vägar.
Hur PAK4 tippar fettceller mot lagring
I fettceller agerar PAK4 som en broms för fettförbränning. Normalt, när vi fastar eller när stresshormoner stiger, aktiverar ett annat enzym kallat PKA kontrollerad nedbrytning av lagrat fett i små droppar. Översikten beskriver hur PAK4 motverkar denna process genom att sätta hämmande fosfatmärken direkt på hormonkänsligt lipas och på ett fettsyrabindande protein som hjälper till att transportera fettmolekyler. Dessa förändringar försvagar maskineriet som frigör fett från lagring. PAK4 stöder också bildningen av nya fettceller tidigt i livet genom att hjälpa cellcykelproteiner att driva prekursorceller att bli mogna fettlagrande celler. När PAK4 avlägsnas eller blockeras i djurmodeller förbränner fettceller mer bränsle, visar tecken på ”bruning” som ökar energiförbrukningen, och djuren skyddas mot viktuppgång orsakad av kosten. 
PAK4:s roll i fettlever och musklernas sockerhantering
I levern gynnar PAK4 återigen lagring framför förbränning. Vid fasta eller på en ketogen diet sjunker PAK4‑nivåerna, vilket tillåter leverceller att öka nedbrytningen av fett och ketonproduktionen, som förser andra vävnader med energi och till och med kan bromsa tumörtillväxt. När PAK4 är rikligt förekommande lägger det fosfatmärken på en nukleär korepressor som sedan hämmar PPARα, en huvudreglerare av fettoxidation och ketonbildning. Resultatet blir mer fett som fastnar i levern och färre skyddande ketoner i blodomloppet. I skelettmuskeln stör PAK4 AMPK, en central energisensor som främjar både glukosupptag och mitokondriell aktivitet. Genom att märka AMPK på ett sätt som blockerar dess aktivering minskar PAK4 mängden glukostransportörer på muskelfasans yta och bidrar till insulinresistens. Muskelspecifik förlust av PAK4 hos möss vänder dessa effekter, förbättrar blodsockerkontrollen även under feta förhållanden.
Stress, skydd och kopplingar till andra cellulära brytare
Översikten lyfter också fram PAK4:s effekter bortom vardaglig ämnesomsättning. Under episoder av minskat blodflöde och plötslig reperfusion i organ som levern försvagar PAK4 antioxidantförsvaret genom att märka och destabilisera Nrf2, en nyckelspelare i skydd mot oxidativ stress. Samtidigt spelar en annan familjemedlem, PAK1, ofta mer stödjande roller i hjärtmuskel, skelettmuskel och insulinproducerande celler i bukspottkörteln och hjälper till att upprätthålla normal glukoshantering. Denna kontrast mellan skadlig PAK4‑signalering vid metabola sjukdomar och i allmänhet fördelaktiga PAK1‑effekter understryker behovet av högselektiva läkemedel som slår ner PAK4 utan att störa närbesläktade proteiner som är viktiga för hjärt‑ och endokrin hälsa.
Att omvandla en upptäckt till behandling
Eftersom PAK4 är överaktivt vid cancer och i metabola störningar har läkemedelsutvecklare sökt små molekyler som blockerar dess aktivitet, liksom nya ”degraderare” som märker PAK4 självt för avlägsnande. Tidiga PAK4‑hämmande föreningar visade antitumörpotential men stötte på utmaningar med specificitet och läkemedelsbeteende i kroppen. Nyare molekyler som mer precist riktar in sig på PAK4 har gett slående resultat i feta möss: lägre kroppsvikt utan minskat födointag, friskare lever, mer aktiva muskler och förbättrad blodsockerkontroll. Degraderande läkemedel går ett steg längre genom att fysiskt eliminera PAK4, och tidiga djurstudier tyder på att de kan skydda mot muskelförtvining och vissa cancerformer. Tillsammans stödjer dessa fynd en bild där nedreglering av PAK4 kan lindra fetma, diabetes och fettlever samtidigt och förvandla en en gång obskyr cellulär brytare till ett lovande fokus för framtida metabola terapier.
Citering: Bang, I.H., Park, BH. & Bae, E.J. PAK4 in metabolic diseases: regulation by nutrient signals and therapeutic implications. Exp Mol Med 58, 416–424 (2026). https://doi.org/10.1038/s12276-026-01645-y
Nyckelord: PAK4, metabol sjukdom, fetma, fettlever, insulinresistens