Clear Sky Science · sv
Den redoxkänsliga proteinet HMGB1: intracellulära och extracellulära roller
Varför ett formföränderligt protein spelar roll för hälsan
Inne i nästan varje cell i din kropp finns ett litet protein kallat HMGB1 som beter sig lite som ett multiverktyg. Under lugna förhållanden hjälper det tyst till att organisera DNA. Men när celler är stressade eller skadade kan HMGB1 förflytta sig ur kärnan, smita ut i omgivande vävnad och fungera som en larmignal för immunförsvaret. Denna översiktsartikel förklarar hur små kemiska förändringar drivna av oxidation förvandlar HMGB1 till väldigt olika biologiska personligheter — sådana som kan skydda vävnader, driva inflammation eller till och med bidra till kronisk sjukdom. Att förstå denna molekylära ”humörring” kan öppna nya vägar att dämpa överdriven inflammation utan att helt stänga av immunförsvaret.
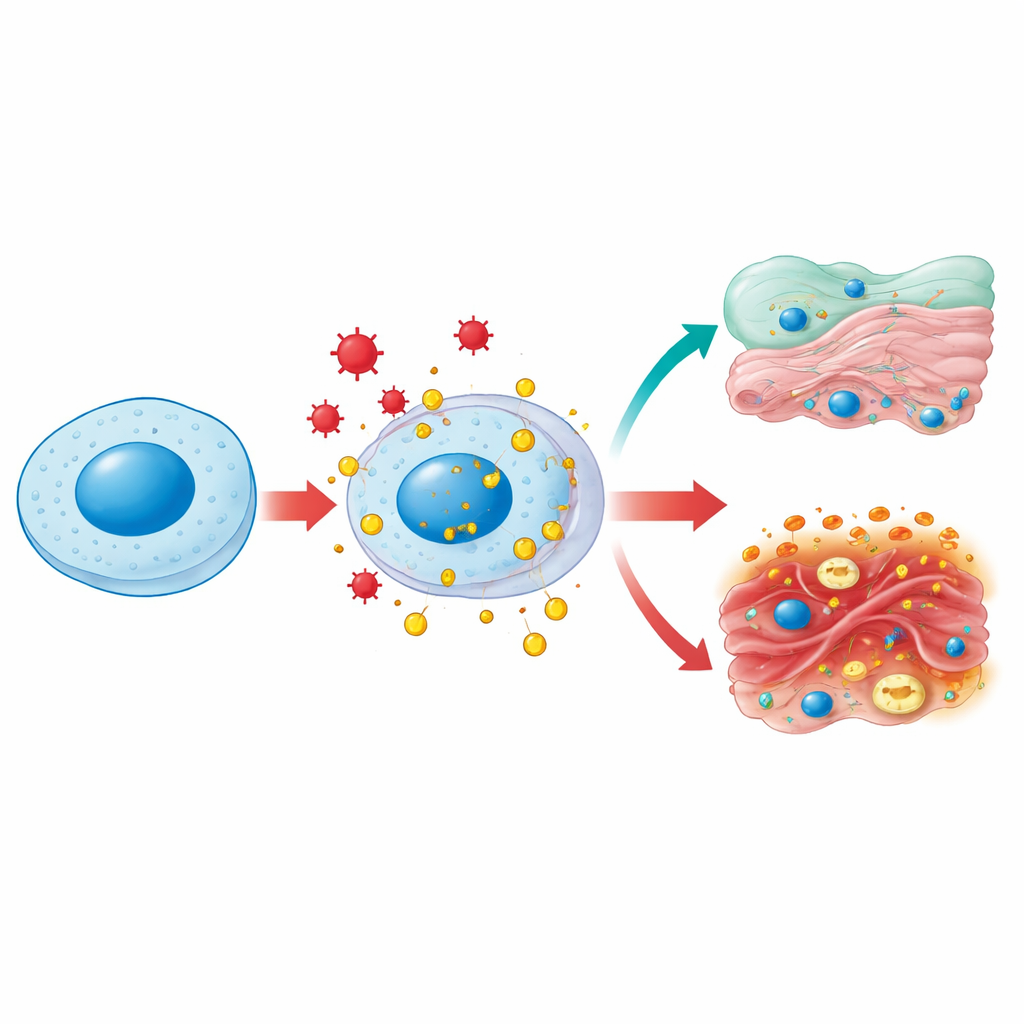
Ett protein, många grannskap
HMGB1 lever normalt i cellkärnan, där det böjer och luckrar upp DNA så att gener kan kopieras och repareras. Under stress — såsom infektion, högt blodsocker eller toxisk skada — kan det kemiskt modifieras och eskorteras ut till cellens vätskeomgivning och vidare utanför cellen. I cytoplasman hjälper HMGB1 till att hålla mitokondrierna, cellens kraftverk, friska genom att främja en renhållningsprocess kallad autofagi och genom att förhindra överdriven fragmentering av dessa organeller. När det frigörs utanför cellen blir HMGB1 en klassisk ”faran-signal”: immunceller känner igen det som ett tecken på att vävnader skadats och skyndar till platsen. Samma molekyl spelar alltså både hushållsroller inne i cellerna och larmroller utanför dem, beroende på var den befinner sig och hur den kemiskt har justerats.
Hur oxidation skriver om dess beteende
Huvudfokus i denna översikt är hur oxidation — reaktioner drivna av reaktiva syrearter (ROS) — omformar HMGB1. Proteinet innehåller tre svavelbärande byggstenar som fungerar som små strömbrytare. I sitt fullt reducerade tillstånd tenderar HMGB1 att stödja cellsöverlevnad och rekrytering av reparerande celler. Mild oxidation kan koppla ihop två av dessa platser inom samma protein och skapa en ”disulfid”-form som är särskilt bra på att fästa vid immunsystemets receptorer såsom Toll‑like‑receptorer och RAGE på cellsurfaer. Denna version stimulerar starkt produktionen av inflammatoriska budbärare. Kraftigare oxidativ stress kan föra molekylen vidare till en överoxiderad form som inte längre effektivt kan binda DNA eller receptorer; denna ”utmattade” version blir immunologiskt tyst och är kopplad till inflammationsresolutionsfasen och celldödsprogram som inte väcker ett immunangrepp.
Från celldödssignaler till sjukdomsdrivare
HMGB1 är djupt sammanflätat med de många sätt celler dör på. Vid våldsamma dödsformer såsom nekros, nekroptos, ferroptos och pyrotos läcker HMGB1 ut eller transporteras aktivt ut ur cellerna och bär på en redoxsignatur som speglar de omgivande oxidativa förhållandena. Tidigt i nekros tenderar det att finnas i en reducerad form, medan långvarig stress driver det mot mer oxiderade tillstånd. När det väl är ute kan reducerat HMGB1 främja skyddande autofagi i vissa cancerceller och hjälpa dem överleva kemoterapi, medan disulfidrika och dimeriserade former förstärker inflammatoriska kaskader och komplementaktivering som kan förvärra vävnadsskada. HMGB1 kan också återkoppla för att driva vissa dödsbanor — till exempel genom att samarbeta med bakteriella lipider för att utlösa nekroptos eller genom att driva järnberoende celldöd i hjärnans stödjeceller efter stroke. På så sätt både markerar och modulerar HMGB1 balansen mellan liv och död i vävnader.
Kopplingar till inflammation, autoimmunitet och cancer
Eftersom dess beteende är så känsligt för oxidation visar olika HMGB1‑varianter upp tydliga mönster över sjukdomar. Disulfidrikt HMGB1 är starkt kopplat till kronisk inflammation: det förekommer i inflammerade leder vid reumatoid artrit, i fibrotisk lever, vid lungsjdior, vid skadeorsakad ischemia–reperfusion efter operation och vid sepsis, där dess nivåer i blodet korrelerar med svårighetsgrad och dödsrisk. Reducerat HMGB1, däremot, följer ofta cellmigration och vävnadsombyggnad, såsom förflyttning av hjärtfibroblaster eller monocyter styrda av kemokinen CXCL12. Överoxiderat, immunologiskt tyst HMGB1 är rikligt i situationer som sena apoptosstadier, där kroppen vill rensa döende celler utan att provocera en attack. I tumörer stödjer disulfidformen en suppressiv, tillväxtgynnsam immunmiljö, medan blockering av HMGB1 kan krympa tumörer och göra checkpoint-immunoterapier mer effektiva.
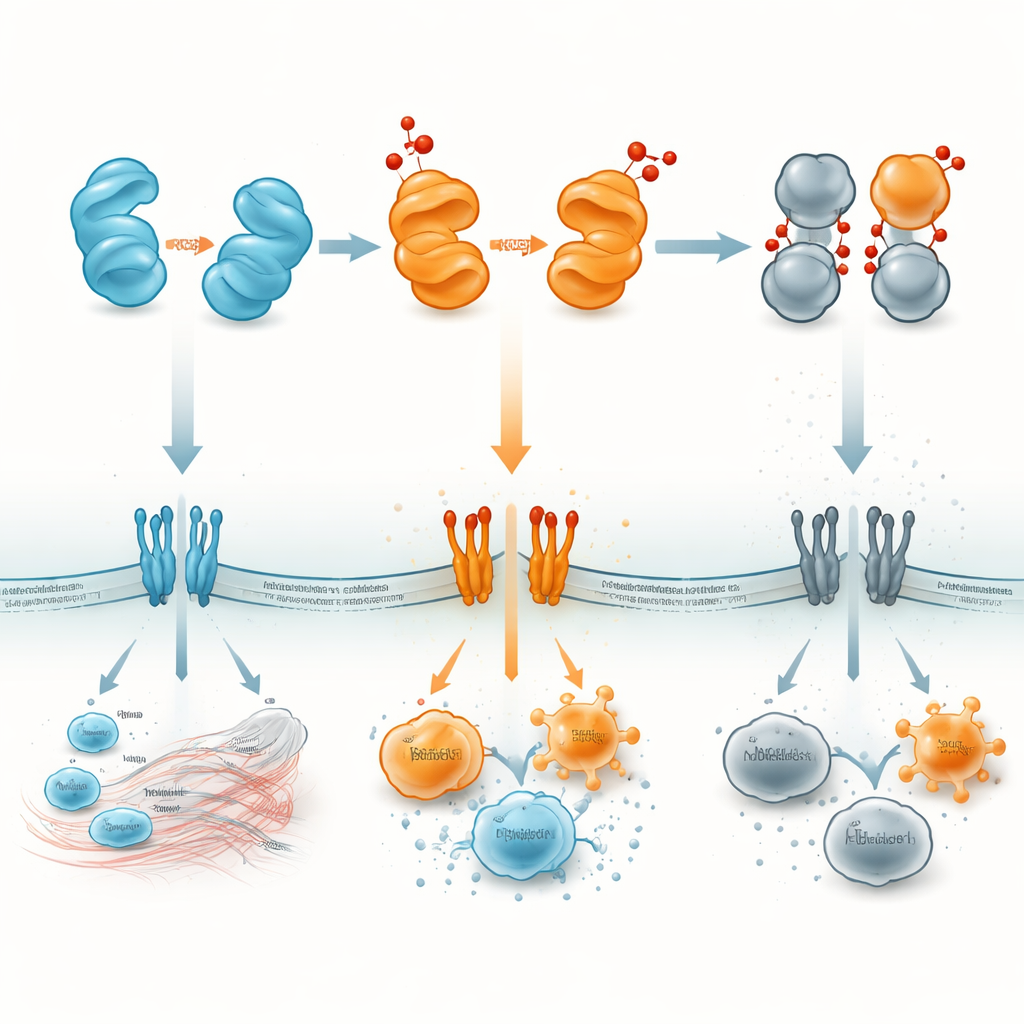
Att förvandla ett molekylärt larm till ett terapeutiskt mål
För en lekmann iakttagare kan HMGB1 ses som ett litet proteinlarm vars volym och budskap ändras med dess kemiska tillstånd. Reducerat HMGB1 tenderar att kalla in reparationslag; disulfid- och dimerformerna kan slå an ett kraftigt alarm som matar skadlig inflammation; och den fullt oxiderade formen blir i praktiken tyst, vilket hjälper inflammationen att klinga av. Genom att kartlägga var och när varje version dyker upp — inne i kärnor, i cytoplasman, i blodet eller i specifika organ — hoppas forskare kunna utforma läkemedel som antingen blockerar de skadliga formerna eller stabiliserar de hjälpsamma. Sådana strategier skulle kunna göra det möjligt för läkare att behandla sepsis, autoimmunitet, stroke, lungsjukdom eller cancer genom att inte bara rikta in sig på HMGB1 i sig, utan på den oxidativa ”dimmern” som styr hur detta protein kommunicerar med immunförsvaret.
Citering: Kwak, M.S., Jung, S.F., Park, I.H. et al. The redox-sensitive protein HMGB1: intracellular and extracellular roles. Exp Mol Med 58, 345–356 (2026). https://doi.org/10.1038/s12276-026-01640-3
Nyckelord: HMGB1, inflammation, oxidativ stress, celldöd, autoimmun sjukdom