Clear Sky Science · sv
UBE2M som en bro som förbinder neddylation och cellcykelreglering i kolorektalt adenomkarsinom
Varför denna forskning är viktig för tarmcancer
Kolorektal cancer är en av de vanligaste och mest dödliga cancerformerna i världen, till stor del därför att tumörceller lär sig dela sig obehindrat. Denna studie avslöjar en tidigare dold kontrollomkopplare som hjälper kolorektala cancerceller att rusa genom en kritisk kontrollpunkt i celldelningen. Genom att visa hur denna omkopplare fungerar på molekylär nivå — och att ett redan godkänt antifungalt läkemedel kan störa den — pekar arbetet mot ett potentiellt nytt sätt att bromsa eller stoppa tumörtillväxt.
Ett dolt kontrollager inne i tumörceller
Celler delar sig inte slumpmässigt; de förflyttar sig genom en ordnad cykel med kontrollpunkter som bekräftar om det är säkert att kopiera DNA och dela sig. Cancerceller manipulerar ofta dessa kontrollpunkter. Forskarna fokuserade på en kemisk märkningsprocess kallad neddylation, som subtilt förändrar proteiner efter att de har bildats. Tidigare studier antydde att neddylation är mer aktiv i många cancerformer, men hur den kopplas till delningscykeln i kolorektala cancerceller var oklart. Med hjälp av stora enkelcellsdataset från mänskliga tumörer, tillsammans med bulk-transkriptionsdata från mer än 1 800 patienter, fann teamet att neddylationsaktiviteten är särskilt hög i maligna tarmceller som befinner sig i G2/M-fasen — den sista porten innan en cell delar sig.
Fokus på ett molekylärt ”bro”-protein
För att ta reda på vilka molekyler som kopplar neddylation till celldelning använde forskarna nätverksliknande beräkningsanalyser för att sålla bland tusentals gener. Ett protein stack ut: UBE2M, ett enzym som hjälper till att fästa den lilla NEDD8-märkningen på andra proteiner. UBE2M var inte bara starkt kopplat till neddylations- och cellcykelvägar i data; det förekom också i mycket högre nivåer i kolorektala tumörer än i närliggande normalt vävnad. Patienter vars tumörer hade högre UBE2M tenderade att få sämre överlevnad, vilket pekar på det som en möjlig drivare snarare än en åskådare. När teamet minskade UBE2M i cancercellinjer och i musmodeller för tumörer, avtog tumörtillväxten, cellerna delade sig mindre och fler celler gick i programmerad celldöd. Omvänt snabbade extra UBE2M på tillväxt och cellcykelprogression.
En relä som skyddar ett nyckelprotein för tillväxt
Vidare undersökte forskarna hur UBE2M hjälper celler att dela sig. De upptäckte att UBE2M inte agerar ensam utan sätter igång ett relä som involverar två andra proteiner, USP39 och PABPC1. Normalt märks PABPC1 för nedbrytning med en kedja av ubiquitin-taggar, som skickar det till cellens proteinnedbrytningsmaskineri. Teamet visade att UBE2M kemiskt modifierar USP39 med NEDD8-taggen. Denna modifiering förbättrar USP39:s förmåga att klippa bort ubiquitinkedjor från PABPC1, rädda det från nedbrytning och göra det mer stabilt. Med mer PABPC1 närvarande blir cellen bättre på att översätta specifika budbärar-RNA till protein, inklusive mRNA för CCNB1, en cyklin som fungerar som gaspedal för G2/M-kontrollpunkten. I praktiken stabiliserar UBE2M PABPC1, vilket i sin tur ökar produktionen av CCNB1 och driver cellerna lättare in i delning.
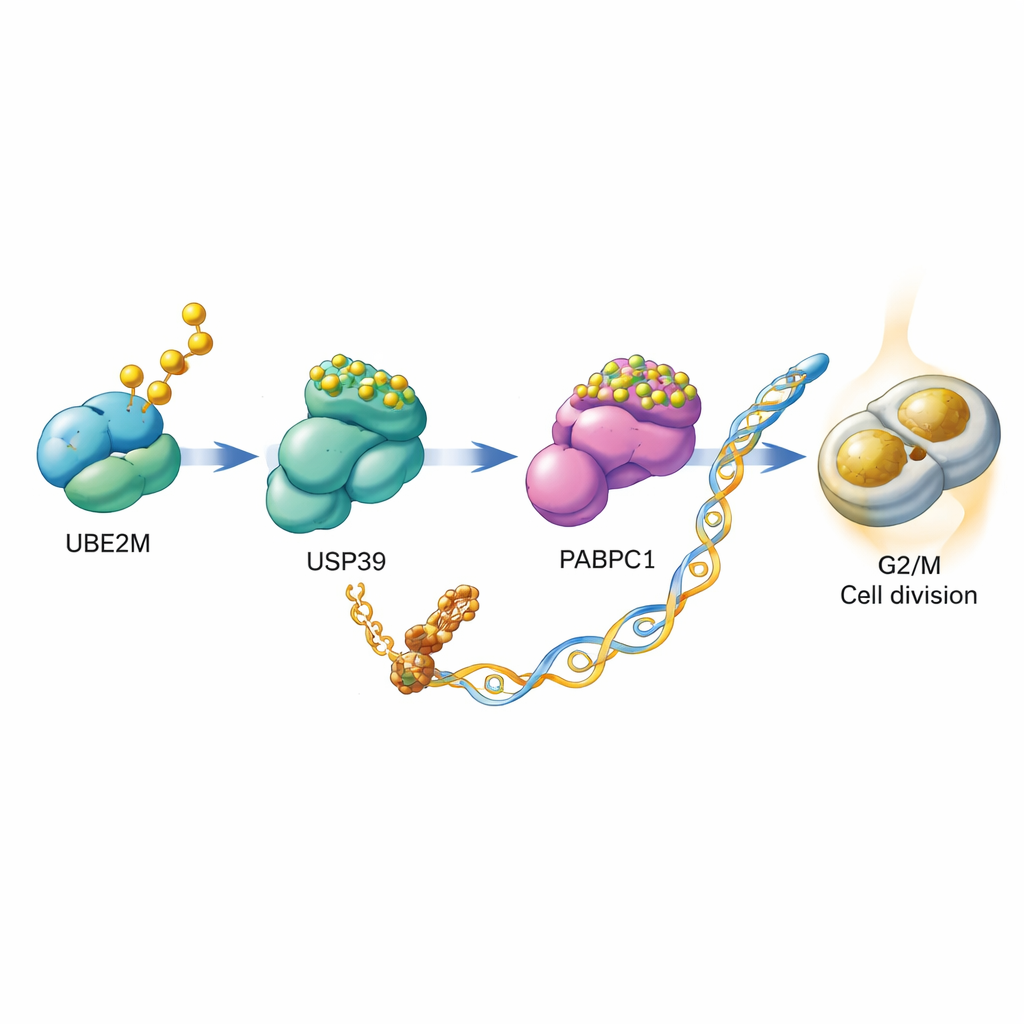
Från molekylär mekanism till läkemedelsmöjlighet
Upptäckten av denna UBE2M–USP39–PABPC1–CCNB1-kedja föreslog en ny sårbarhet i kolorektala cancerceller. Författarna vände sig till mikafungin, ett läkemedel som redan används för att behandla svampinfektioner och nyligen identifierats som en hämmare av UBE2M:s neddylationsaktivitet. I tarmcancerceller odlade i labbet försvagade mikafungin USP39-neddylation, ökade nedbrytningen av PABPC1 och sänkte nivåerna av CCNB1-protein. Som ett resultat bromsade celldelningen, fler celler fastnade vid G2/M-kontrollpunkten och apoptos ökade. I möss inplanterade med kolorektala cancerceller minskade daglig behandling med mikafungin tumörstorleken signifikant jämfört med obehandlade djur, utan att behöva avlägsna UBE2M självt.
Vad detta betyder för patienter på lång sikt
Detta arbete målar en tydlig bild av hur ett enda enzym, UBE2M, kan koppla ett subtilt proteinmärkningssystem till beslutet om en tarmcancercell ska dela sig. Genom att stabilisera en translationsfaktor (PABPC1) via USP39 ökar UBE2M indirekt nivåerna av en stark cellcykeldrivare, CCNB1, vilket tillåter tumörer att växa snabbare. Även om mer forskning och kliniska tester krävs, tyder resultaten på att blockera detta relä — potentiellt med omdisponerade läkemedel som mikafungin — skulle kunna erbjuda en ny riktad strategi för att sakta ner kolorektal cancerprogression och förbättra patientutfall.
Citering: Wang, Z., Wang, Y., Chen, Y. et al. UBE2M as a bridge spanning neddylation and cell cycle regulation in colorectal adenocarcinoma. Exp Mol Med 58, 501–518 (2026). https://doi.org/10.1038/s12276-026-01636-z
Nyckelord: kolorektal cancer, cellcykel, neddylation, UBE2M, målstyrd terapi