Clear Sky Science · sv
Läkemedelsinducerad gastrointestinal toxicitet och barriärintegritet: cytoskelettmedierad nedsättning i en kliniskt relevant human tarmepitelmodell
Varför biverkningar i tarmen spelar roll
Många läkemedel som bekämpar cancer, inflammation eller andra sjukdomar kan oavsiktligt skada tarmens slemhinna. När denna inre "hud" i tarmen skadas kan patienter drabbas av diarré, smärta, illamående och dåligt näringsupptag, ibland så allvarligt att läkare måste avbryta eller sänka livräddande behandlingar. Idag missar laboratorietester ofta dessa problem innan läkemedel når patienter. Den här studien presenterar en mer realistisk laboratoriemodell av den mänskliga tarmen och visar hur den kan upptäcka tarm‑skadande läkemedel tidigare och avslöja hur de försvagar kroppens naturliga barriär.
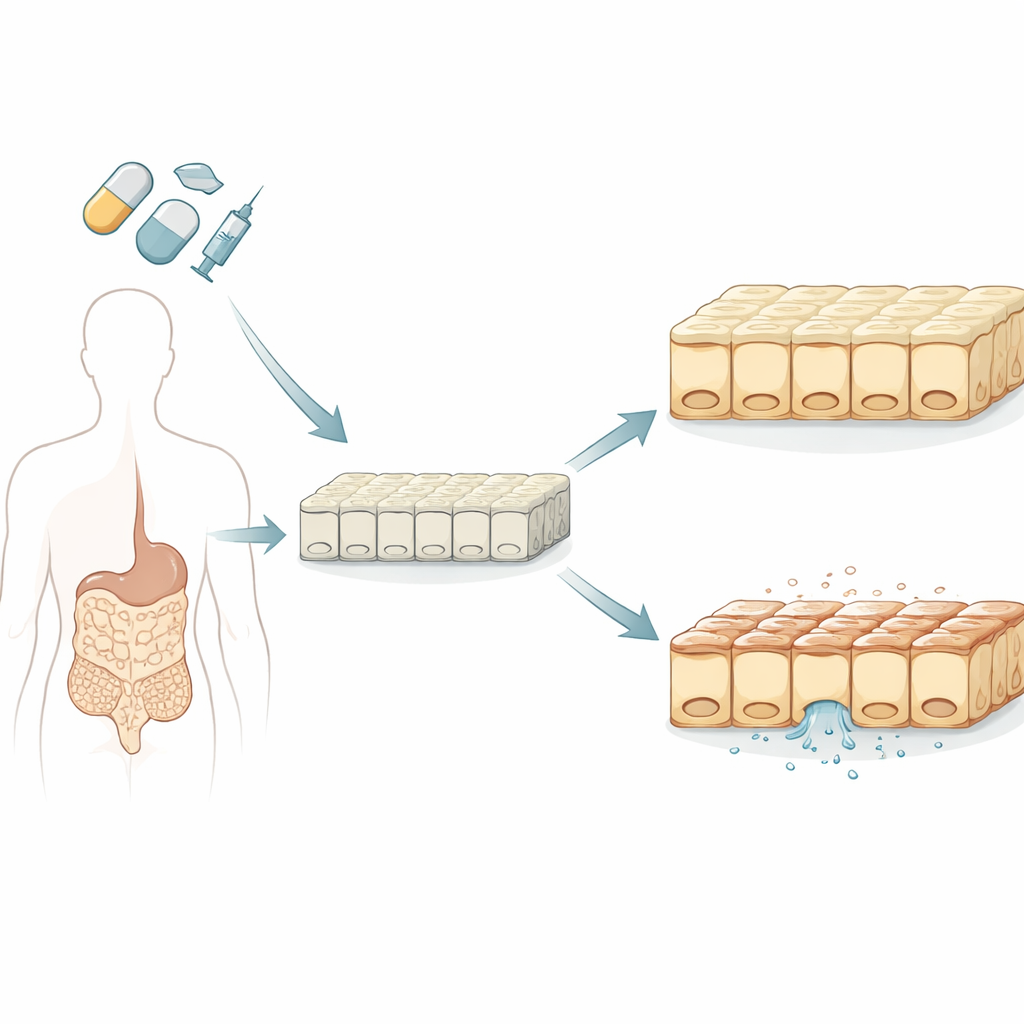
Att bygga en bättre mini‑tarm
Forskarna började med att odla skivor av mänskliga tarmceller i laboratoriet med hjälp av stamceller, som kan differentiera till flera vävnadstyper. Till skillnad från den traditionella cancer‑härledda cellinjen som länge använts för läkemedelstestning, bildade dessa stamcells‑härledda celler ett blandat samhälle som mer liknar den verkliga tunntarmen, inklusive bägarceller som utsöndrar slem och hormonproducerande celler. Teamet bekräftade att dessa laboratorieodlade slemhinnor hade realistisk täthet mot läckage, korrekt topp‑och‑botten‑polaritet och viktiga transport‑ och metabolismegenskaper som påverkar hur läkemedel passerar genom och bearbetas av tarmen.
Mätning av barriärens elektriska täthet
För att testa tarmsäkerhet fokuserade gruppen på transepithelial elektriskt motstånd, eller TEER, en icke‑invasiv avläsning av hur väl intilliggande celler tätar mot varandra. Högt TEER betyder en tät, skyddande barriär; fallande TEER betyder att väggen mellan tarm och blodomlopp blir läckande. Forskarna jämförde TEER med ett standardtest för cellsurvival som mäter energimolekyler såsom ATP. De exponerade både sin nya tarmmodell och den äldre cancermodellcellen för 17 läkemedel som är kända för att skilja sig i hur ofta de orsakar gastrointestinala biverkningar, inklusive vanliga kemoterapiläkemedel, riktade cancerpiller och smärtstillande som ibuprofen och andra antiinflammatoriska medel.
Att hitta dold skada innan cellerna dör
I detta panel av läkemedel överträffade TEER‑mätningarna i det stamcells‑härledda tarmskiktet det traditionella ATP‑testet och den äldre cancercellsbarriären. Flera kemoterapiläkemedel visade liten förändring i ATP, vilket tyder på att cellerna fortfarande var levande, men de orsakade stora fall i TEER och tydliga skador i live‑dead‑färgningar. Det innebär att barriären kan svikta innan cellerna dör helt — en tidig varning som klassiska livsduglighetstester missar. När teamet jämförde sina laboratorieresultat med kliniska register över hur ofta varje läkemedel utlöser tarmsymptom, flaggade den nya TEER‑assayn korrekt nästan alla högre‑risk läkemedel och gav rätt lugnande besked för låg‑riskläkemedlen, med mycket hög noggrannhet.
Hur läkemedel undergräver det inre skelettet
För att ta reda på vad som gick fel inne i cellerna analyserade forskarna genaktivitet efter behandling med två kemoterapiagentser som riktar sig mot mikrotubuli, en nyckelkomponent i cellens inre skelett. De fann breda minskningar i gener involverade i cytoskelettet, cell‑till‑cell‑adhesion och extracellulär matrix — nätverket som hjälper celler att förankra sig i sin omgivning. Ytterligare experiment visade dosberoende ökningar i reaktiva syreföreningar, instabila syreinnehållande molekyler som kan skada cellulära strukturer. Tillsammans pekar dessa förändringar på en kedja av händelser där vissa läkemedel stör det inre ramverket och förbindelserna mellan tarmceller, lossar barriären och tillåter substanser att läcka mellan cellerna.
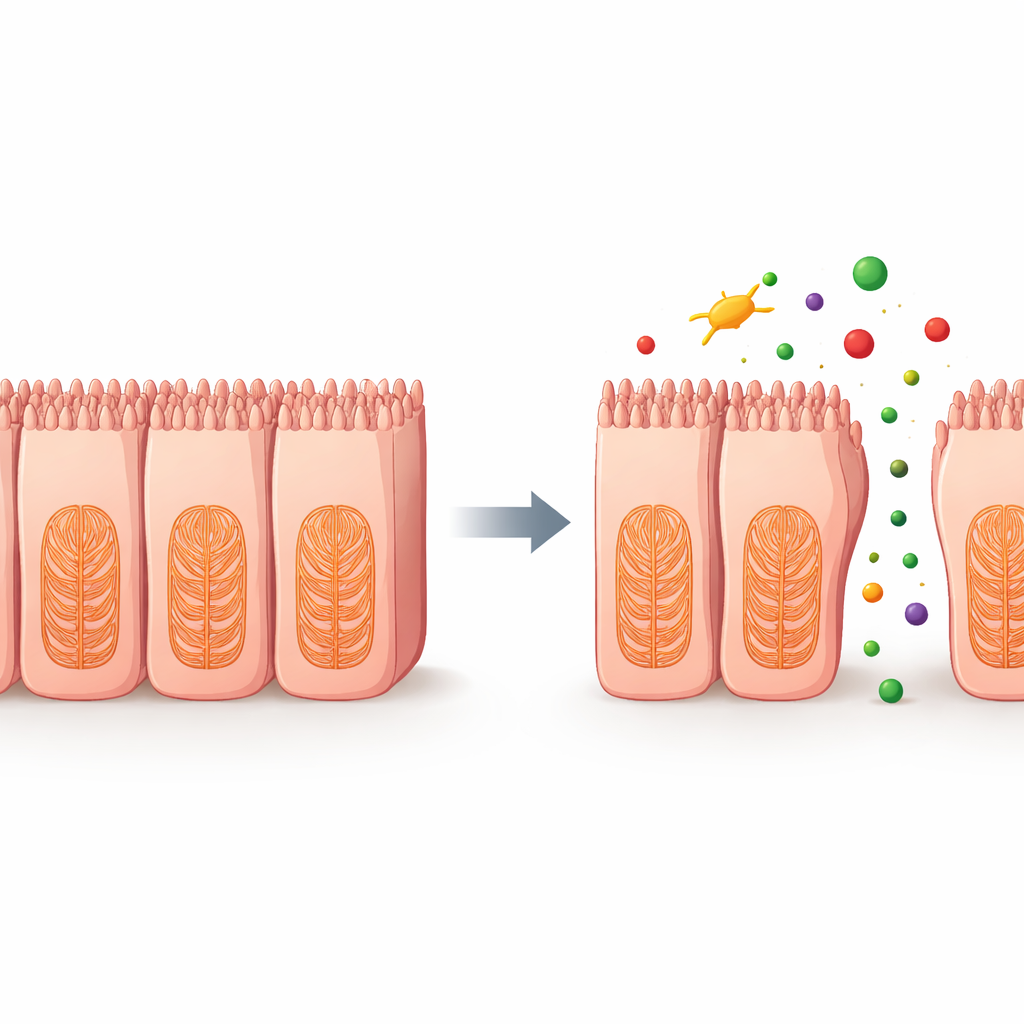
Vad detta betyder för patienter
Denna studie visar att ett stamcellsbaserat mänskligt tarmepitel, parat med enkla elektriska mätningar av barriärtäthet, kan förutsäga vilka läkemedel som sannolikt orsakar tarmskador mer tillförlitligt än långvariga laboratoriemetoder. Genom att upptäcka barriärförsvagning tidigt — och koppla den till underliggande skada i det cellulära skelettet — kan denna plattform hjälpa läkemedelsutvecklare att kassera eller omdesigna riskfyllda föreningar innan de når kliniken. På längre sikt kan sådana realistiska “mini‑tarm”‑tester minska obehagliga eller farliga gastrointestinala biverkningar för patienter samtidigt som de gör det möjligt för läkare att använda kraftfulla behandlingar säkrare.
Citering: Yu, W.D., Lee, S., Cho, HS. et al. Drug-induced gastrointestinal toxicity and barrier integrity: cytoskeleton-mediated impairment in a clinically relevant human intestinal epithelium model. Exp Mol Med 58, 487–500 (2026). https://doi.org/10.1038/s12276-025-01635-6
Nyckelord: gastrointestinal toxicitet, intestinal barriär, stamcellsmodell, Läkemedelssäkerhet, kemoterapi biverkningar