Clear Sky Science · sv
CDK13 driver klarcellig njurcancer genom METTL16-medierad m6A-modifiering av ACLY-mRNA
Varför fettfyllda njurtumörer är viktiga
Klarcellig njurcancer ser ofta blek och oljig ut i mikroskopet eftersom dess celler är fyllda med fett. Det ovanliga utseendet är inte bara kosmetiskt; det speglar en djupare omprogrammering av hur dessa cancerceller hanterar bränsle. Denna studie ställer en enkel men viktig fråga: vilken molekylär brytare får njurtumörceller att hamstra fett, och kan den brytaren slås av för att bromsa sjukdomen?
En dold dirigent för tumörtillväxt
Forskarna fokuserade på ett protein kallat CDK13, en del av en familj enzymer som normalt hjälper celler att dela sig. Genom att analysera stora patientdatamängder och tumörprover fann de att CDK13-nivåerna konsekvent är högre i klarcellig njurcancer än i normalt njurvävnad. Patienter vars tumörer hade mer CDK13 tenderade att ha större, mer avancerade cancerformer och sämre prognos. När teamet sänkte CDK13 i njurcancercellinjer växte cellerna långsammare och fick svårt att gå igenom cellcykeln, vilket tyder på att CDK13 agerar som en dold dirigent som koordinerar både tillväxt och överlevnad.
Från socker till fett: omkoppling av cellens bränslefabrik
Eftersom klarcellig njurtumörer är fyllda av lipider undersökte teamet om CDK13 också styr hur dessa celler tillverkar fett. Med en kombination av genuttrycksprofilering och mikroskopiska fettdyrningar visade de att ökade nivåer av CDK13 ökar ansamlingen av lipiddroppar inne i cancerceller, medan minskad CDK13 har motsatt effekt. CDK13 påverkade starkt ett enzym kallat ACLY, som omvandlar ett vanligt metabolt mellanprodukt till acetyl-CoA, startmaterialet för att bygga fettsyror och kolesterol. Höga CDK13-nivåer gick hand i hand med högt ACLY i patienttumörer, och båda proteinerna koncentrerades i samma områden i tumörvävnaden. När ACLY konstgjort höjdes återställdes många av de tillväxt- och fettlagringsdefekter som orsakats av CDK13-förlust, vilket placerar ACLY som en viktig downstream-effektor i denna bana. 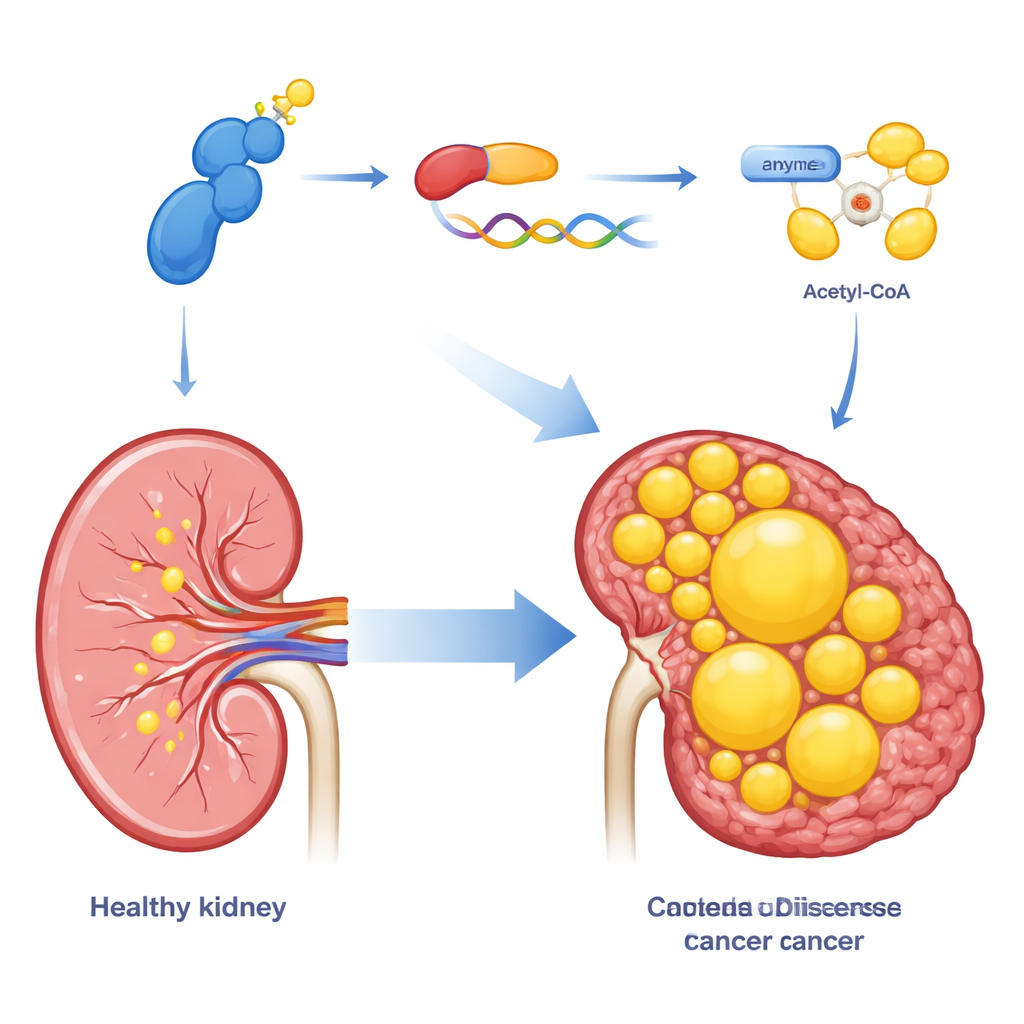
Ett lager-på-lager budskapssystem i cancerceller
I stället för att verka direkt på ACLY som en enkel av- och på-knapp utövar CDK13 sin effekt genom ett lager-på-lager budskapssystem byggt på RNA, molekylen som för över genetiska instruktioner från DNA till proteinmaskineriet. Författarna upptäckte att CDK13 fysiskt binder till och kemiskt modifierar ett annat enzym, METTL16, som pryder specifika RNA-meddelanden med små kemiska märken kallade metylgrupper. CDK13 lägger till en fosforyleringstagg på METTL16 på en bestämd plats, vilket gör METTL16 mer aktiv. I sin tur placerar METTL16 extra metylmärken på RNA-blåkopian för ACLY. Dessa märken förändrar inte den genetiska koden i sig, men de ändrar hur cellen behandlar det meddelandet. Ett tredje protein, YTHDC2, känner igen det märkta ACLY-RNA:t och skyddar det från nedbrytning, vilket tillåter mer ACLY-protein att produceras över tid. Denna kaskad—CDK13 som aktiverar METTL16, METTL16 som märker ACLY-RNA, och YTHDC2 som vaktar det märkta meddelandet—skapar en kraftfull drivkraft för fettsyntes. 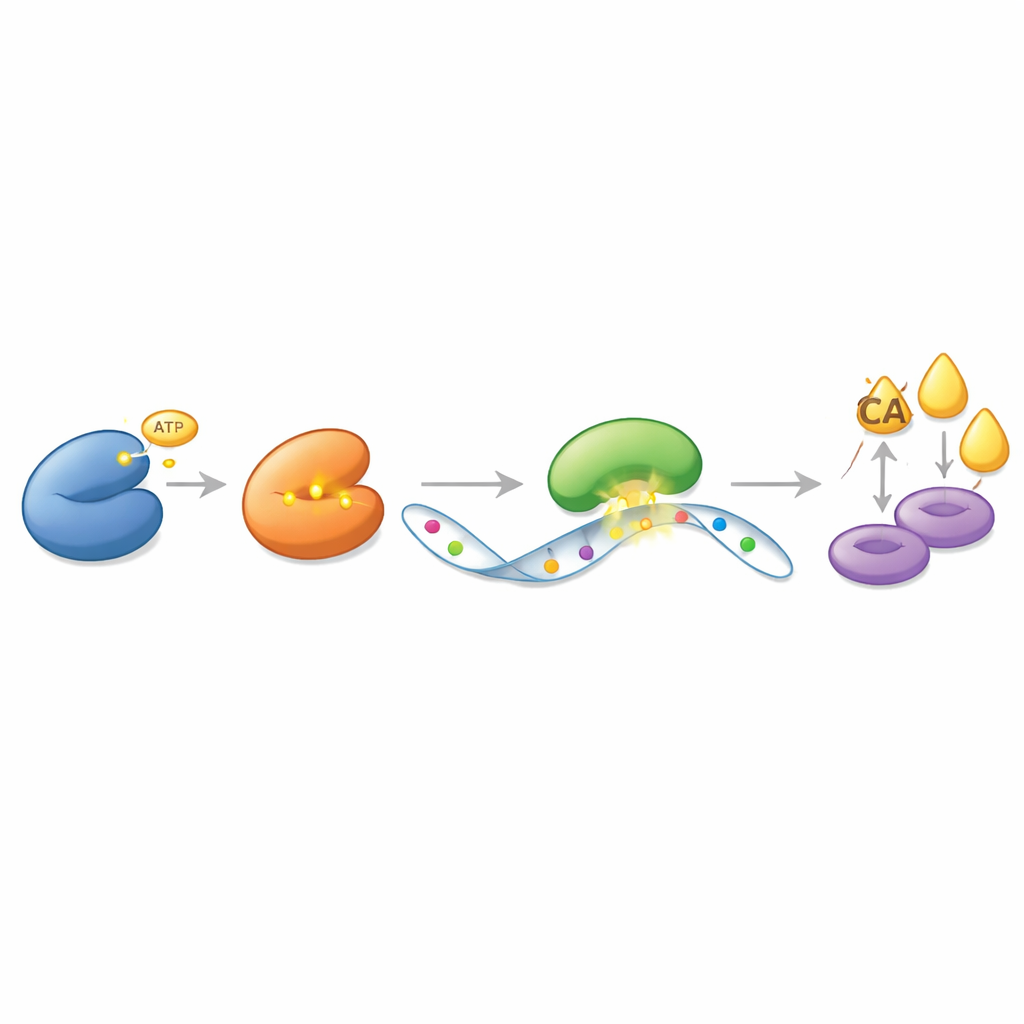
Test av kedjan i celler, möss och patientprover
Styrkan i arbetet ligger i hur grundligt författarna testade denna händelsekedja. I odlade njurcancerceller minskade störning av vilken del som helst av CDK13–METTL16–ACLY-axeln antalet lipiddroppar och saktade ner proliferation. Hos möss som fick mänskliga njurcancerceller inopererade krympte tumörer och fettdepåerna inom dem när CDK13 eller ACLY hämmades, medan samtidig blockering av båda gav en ännu starkare effekt. Teamet använde också en småmolekylförening, 1NM-PP1, som hämmar CDK13-aktivitet. Denna läkemedelslika agent minskade den aktiverande taggen på METTL16, sänkte ACLY-nivåerna och dämpade tumörtillväxt, särskilt i kombination med METTL16-utarmning. I patientdatamängder tenderade CDK13, METTL16 och ACLY att stiga och falla tillsammans, vilket förstärker idén att denna axel är aktiv i verkliga cancerformer, inte bara i laboratoriemodeller.
Vad detta kan innebära för framtida behandlingar
För icke-specialister är huvudbudskapet att denna studie blottlägger en ny kontrollratt för ”fabriken för fett” inne i klarcellig njurtumörer. Istället för att enbart rikta in sig på enzymerna som tillverkar lipider visar forskarna en högre nivå i kommandokedjan som stabiliserar instruktionerna för dessa enzymer. Genom att avbryta CDK13–METTL16–ACLY-axeln kan det bli möjligt att beröva tumörer de fetter de behöver för att växa och sprida sig, samtidigt som normala celler påverkas i mindre utsträckning. Trots att arbetet fortfarande är prekliniskt och 1NM-PP1 ännu inte är ett läkemedel mot njurcancer, pekar fynden mot nya strategier som kombinerar kinasehämmare med läkemedel som riktar RNA-modifierande enzymer, vilket erbjuder ett mer precist sätt att behandla denna metabolt drivna form av njurcancer.
Citering: Chen, J., Liu, H., Zhang, Y. et al. CDK13 drives clear cell renal carcinoma through METTL16-mediated m6A modification of ACLY mRNA. Exp Mol Med 58, 472–486 (2026). https://doi.org/10.1038/s12276-025-01634-7
Nyckelord: klarcellig njurcellscarcinom, lipidmetabolism, CDK13, RNA-metylering, ACLY