Clear Sky Science · sv
Två koder för RNA-redigering genom deaminering vid mänskliga sjukdomar
Hur celler skriver om sina egna budskap
Varje cell i din kropp läser ständigt instruktioner från DNA för att bygga och underhålla dig. I årtionden antog vi att dessa instruktioner kopierades till RNA och sedan troget översattes till proteiner. Denna översiktsartikel visar att berättelsen är mycket mindre stel: celler "skriver faktiskt om" många RNA-budskap efter att de skapats, genom att byta ut enstaka kemiska bokstäver på sätt som kan förändra hur vår kropp fungerar, subtilt eller dramatiskt. Att förstå detta dolda redigeringslager hjälper till att förklara varför människor utvecklar autoimmuna sjukdomar, neurologiska störningar, metabola problem, infektioner och cancer — och hur vi så småningom kan behandla dem.
Två sätt att ändra en enda bokstav
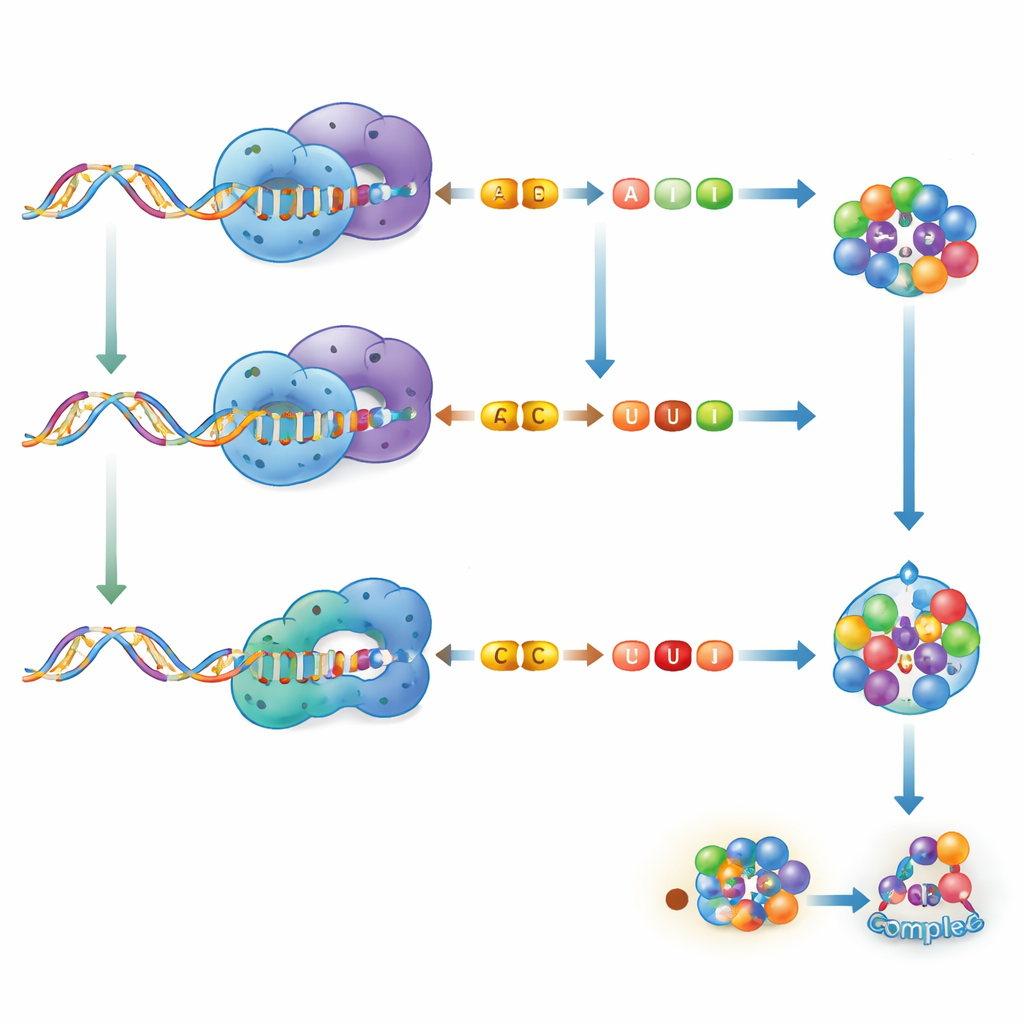
Författarna koncentrerar sig på två huvudtyper av RNA-redigering som förekommer hos människor. Den ena kallas A-till-I-redigering och utförs av enzymer kända som ADAR. De omvandlar basen adenosin (A) till inosin (I), vilket cellens maskineri i huvudsak läser som om det vore guanosin (G). Den andra är C-till-U-redigering, hanterad av enzymer i APOBEC-familjen, som konverterar cytidin (C) till uridin (U). Båda processerna avlägsnar en liten kemisk grupp från en enkel bas, men de skiljer sig åt i var de verkar, vilka RNA de föredrar och hur kraftfullt de omformar RNA-strukturen. A-till-I-redigering ändrar ofta hur RNA-strängar parar sig och kan diversifiera proteiner eller förändra hur andra molekyler binder RNA. C-till-U-redigering tenderar att vara mer subtil strukturellt, men kan ändå införa stoppkodon, justera proteinsekvenser eller finjustera regulatoriska regioner i RNA.
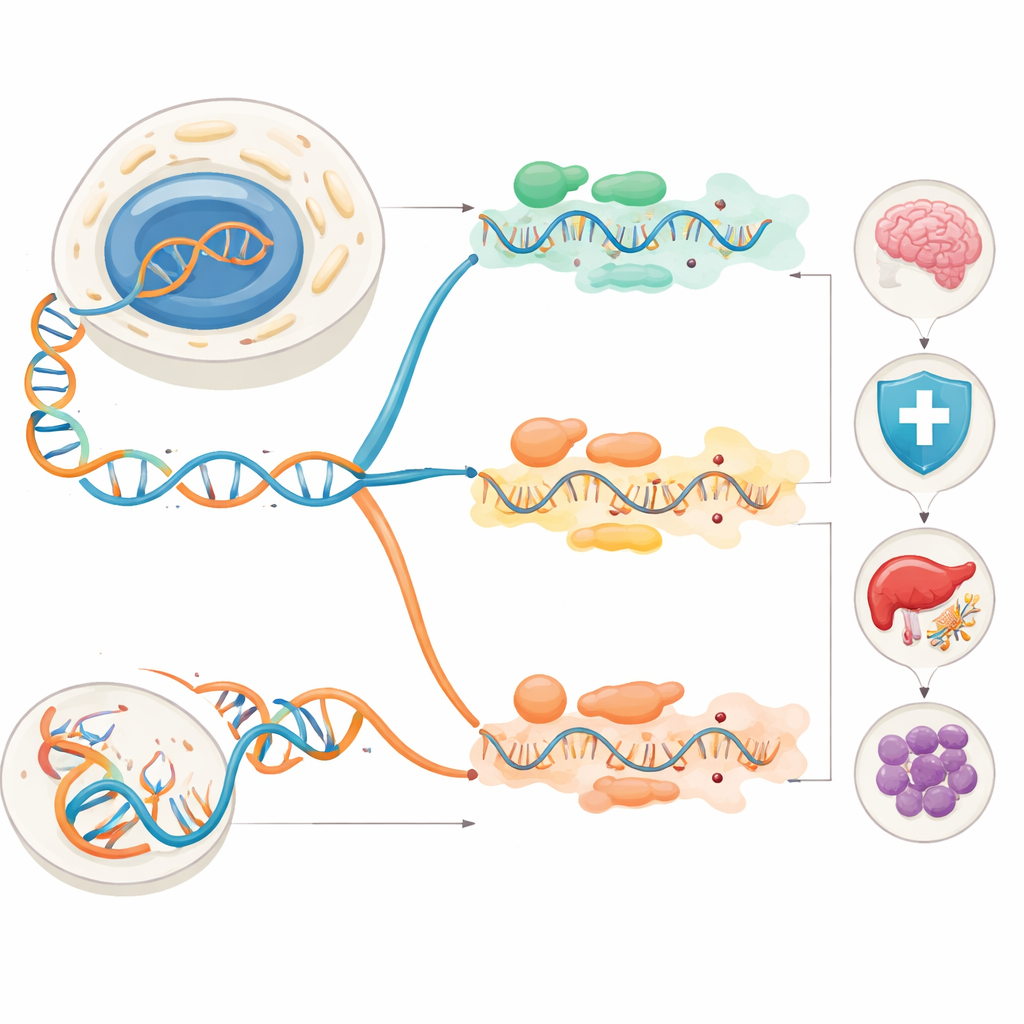
Från redigerade budskap till hälsa och sjukdom
Eftersom dessa redigeringshändelser kan ändra proteindelar eller de regulatoriska regionerna omkring dem, påverkar de många aspekter av normal biologi. I immunsystemet redigerar ADAR1 dubbelsträngat RNA som cellen själv skapar så att virussensorer inte misstar dem för främmande angripare. När ADAR1 misslyckas förblir immunlarmen "på", vilket leder till kronisk interferonsignalering och autoimmuna tillstånd som Aicardi–Goutières syndrom. APOBEC-enzymer redigerar också RNA i immunceller, formar hur makrofager svarar på stress och inflammation och kan bidra till sjukdomar som systemisk lupus. I nervsystemet är ADAR2-redigering avgörande för att stämma av hjärnans receptorer som kontrollerar kalciumflöde; utan den får möss anfall och dör tidigt. APOBEC-driven redigering av vissa receptor-RNA i neuroner kan öka deras känslighet och är kopplad till epilepsi, degeneration och kognitiva problem.
Virus, metabolism och kopplingen till cancer
RNA-redigering påverkar också hur vi interagerar med virus, hanterar energi och utvecklar cancer. ADAR1 kan redigera virala genom direkt, ibland försvaga viruset och ibland, som i hepatit D-virus, hjälpa det att slutföra sin livscykel. APOBEC-enzymer, kända för att angripa retrovirus, lämnar ett starkt C-till-U-signatur i RNA hos SARS-CoV-2, vilket både begränsar viruset och samtidigt genererar mutationer som kan underlätta viral evolution. I metabolismen hjälper ADAR2 pankreas betaceller att justera insulinsekretionen som svar på kost, medan ADAR1- och ADAR2-aktivitet påverkar risken för diabetes och fettlever. APOBEC1s klassiska roll är att redigera RNA för apolipoprotein B, vilket producerar ett förkortat protein som är viktigt för transport av kostfetter; när denna redigering saknas utvecklar möss allvarliga lipid- och kolesterolproblem.
Hur redigerat RNA formar tumörer
Samma enzymer som skyddar oss kan också driva cancer när de regleras fel. Stora cancersekvenseringsprojekt har avslöjat tiotusentals A-till-I-redigeringsställen och utbredda APOBEC-relaterade mutationer. I bröstcancer kan ADAR1-redigering antingen driva eller dämpa tumörbeteende beroende på mål-RNA, vilket påverkar cellinvasion, metastasering och överlevnad. I glioblastom, en dödlig hjärntumör, stödjer ADAR1 cancerceller med stamcellsegenskaper, medan ADAR2 generellt fungerar som en broms på tillväxt genom att redigera både proteinkodande RNA och cancerfrämjande mikroRNA. I leukemier ökar ADAR1 ofta maligna stamliknande celler och dämpar tumörsuppressiva mikroRNA, medan ADAR2 redigerar specifika mål på sätt som bromsar sjukdomen. APOBEC-medierad C-till-U-redigering av vissa RNA i blodcancer kan antingen förvärra eller förbättra patientutfall, vilket understryker hur kontextberoende dessa förändringar är.
Ofrågade frågor och framtida möjligheter
Trots en explosion av katalogiserade redigeringsställen kämpar forskare fortfarande med att skilja meningsfulla redigeringar från bakgrundsbrus. Många upptäckta förändringar kan ha liten påverkan, men en minoritet har tydligt livsavgörande konsekvenser för celler och organismer. Författarna hävdar att framtida arbete måste identifiera vilka enzymer och hjälpproteiner som styr enskilda ställen, och sedan testa vad som händer när dessa enskilda baser tvingas vara alltid redigerade eller aldrig redigerade. Sådana studier kommer att klargöra hur RNA-redigering bidrar till specifika sjukdomar och visa om justering av redigeringsmönster kan bli en ny klass av precisionsbehandlingar — för att dämpa ett överaktivt immunsystem, stämma hjärnkretsar, korrigera metabola obalanser eller göra tumörer mer sårbara för behandling.
Varför detta spelar roll för vardagshälsan
Enkelt uttryckt visar denna artikel att våra celler inte bara läser den genetiska koden; de korrekturläser och reviderar den aktivt i RNA-stadiet, med två parallella "redigeringskoder". När dessa små redigeringar sker på rätt plats och i rätt mängd hjälper de till att hålla vårt immunsystem i balans, våra hjärnor stabila, vår ämnesomsättning flexibel och våra försvar mot virus skarpa. När redigeringsmaskineriet är överaktivt, felplacerat eller trasigt kan dessa samma förändringar skicka oss mot autoimmunitet, infektion, demens, metabola sjukdomar eller cancer. Genom att kartlägga och förstå dessa enkelbokstavsomskrivningar hoppas forskare diagnostisera sjukdom tidigare, förutsäga vem som löper risk och så småningom utforma behandlingar som skjuter redigeringsprocessen mot hälsa.
Citering: Min, D.J., Lee, S., Lee, Ys. et al. Two codes of RNA editing by deamination in human diseases. Exp Mol Med 58, 382–395 (2026). https://doi.org/10.1038/s12276-025-01633-8
Nyckelord: RNA-redigering, ADAR, APOBEC, autoimmunitet, cancer