Clear Sky Science · sv
Interferonreglerande faktor 5 bidrar till emfysenens patogenes via NLRP3 och Ly6C‑uttryckande celler
Varför denna lungstudie är viktig
Kroniskt obstruktiv lungsjukdom (KOL) och emfysem berövar miljontals människor andan, ofta länge efter att de slutat röka. Befintliga läkemedel kan hjälpa till att vidga luftvägarna, men de gör lite för att lugna den glödande inflammation som fortsätter att äta upp lungorna. Denna studie avslöjar en molekylär ”härförare” för den skadan och pekar på ett nytt sätt att skydda de sköra luftblåsorna och bromsa försämringen av lungfunktionen.
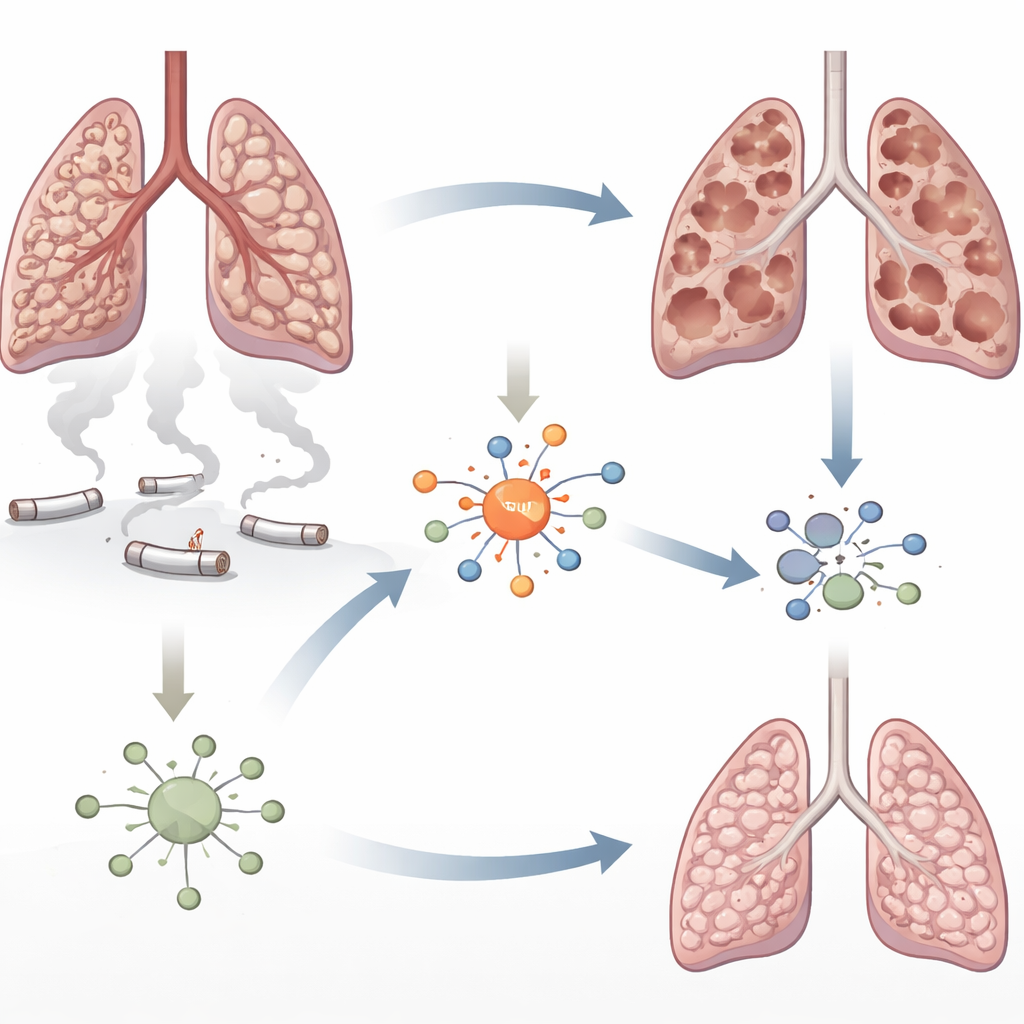
Närmare titt på rök‑skadade lungor
Emfysem kännetecknas av den gradvisa nedbrytningen av de små luftblåsorna som utbyter syre och koldioxid. Cigarettrök badar lungorna i giftiga partiklar som skadar celler och lockar vågor av immunceller. Författarna fokuserade på ett protein kallat interferonreglerande faktor 5 (IRF5), känt för att driva inflammation vid autoimmuna sjukdomar men som inte studerats väl i KOL. Tidigare arbete hade antytt att IRF5‑nivåer stiger i rökexponerade lungor. Här ville forskarna ta reda på om IRF5 bara följer med inflammationen eller faktiskt bidrar till nedbrytningen av lungvävnaden.
Att stänga av en nyckelomkopplare i möss
För att undersöka IRF5:s roll konstruerade teamet möss som helt saknar genen för detta protein. De exponerade sedan normala och IRF5‑defekta djur för cigarettrök i flera veckor och jämförde lungornas skick. Hos normala möss orsakade rök tydliga tecken på emfysem: väggarna mellan intilliggande luftblåsor försvann och lämnade stora, överfyllda utrymmen. I kontrast var möss utan IRF5 till stora delar skyddade från denna strukturella skada, även om rök fortfarande förde immunceller in i luftutrymmena och ökade många inflammatoriska molekyler. Det pekade på IRF5 som en avgörande länk mellan rökexponering och den faktiska nedbrytningen av lungarkitekturen.
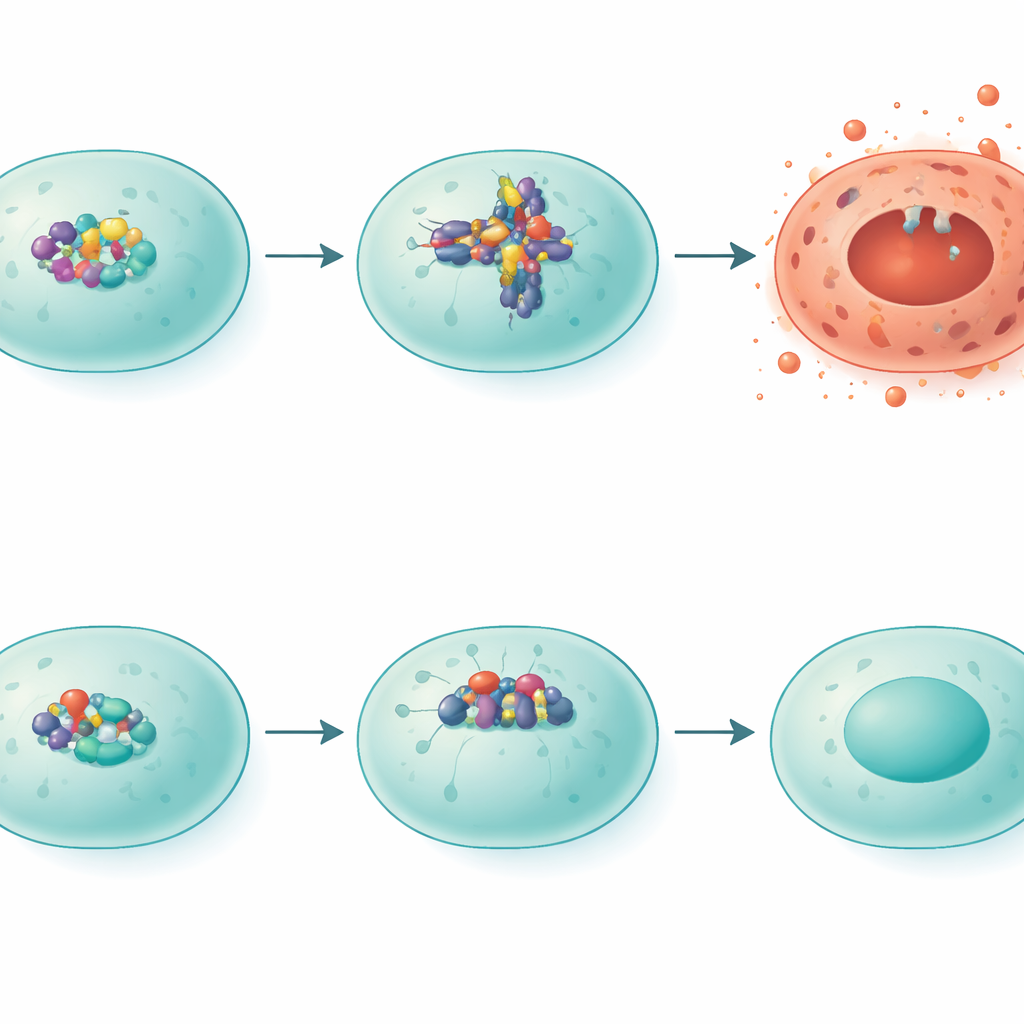
Hur IRF5 driver celler mot eldande död
Forskarlaget zoomade sedan in på en särskild form av våldsam celldöd kallad pyroptos, som spränger hål i cellmembran och spiller inflammatoriskt innehåll ut i omgivande vävnad. Ett proteinkomplex känt som NLRP3 står i centrum för denna process. I rökexponerade normala möss steg NLRP3‑nivåerna, och mönster av ett annat protein, gasdermin D, överensstämde med ett pyroptosliknande tillstånd. I IRF5‑defekta möss var NLRP3‑nivåerna mycket lägre och gasdermin D klipptes till alternativa former förknippade med mindre destruktiva utfall. När teamet konstgjort ökade IRF5 i lungrelaterade celler i laboratoriet steg NLRP3‑nivåerna, vilket bekräftar att IRF5 fungerar som en transkriptionell omkopplare som slår på denna skadliga väg.
Skyddande immunceller kliver in i bilden
IRF5 omformade också sammansättningen av immunceller i lungan. I möss som saknade IRF5 såg man en markant ökning av en undergrupp av blodburna celler starkt märkta av en ytmolekyl kallad Ly6C. Dessa Ly6C‑höga celler inkluderade både monocyter och T‑celler och förekom i större antal efter rökexponering. När forskarna renade Ly6C‑höga celler från IRF5‑defekta möss och infunderade dem i vanliga rökexponerade djur utvecklade mottagarna mindre luftblåsdestruktion och visade lägre NLRP3‑nivåer i lungan. Ytterligare experiment visade att IRF5 direkt dämpar aktiviteten i Ly6C‑genen, vilket tyder på att när IRF5 är närvarande produceras eller upprätthålls färre av dessa potentiellt skyddande celler.
Mänskliga lungor bekräftar signalen
För att pröva om dessa fynd kan vara relevanta för människor undersökte författarna lungvävnad från patienter som genomgick operation för lungcancer. De jämförde prover från individer med god gasutbyteskapacitet med dem med betydande emfysem. IRF5‑proteinnivåerna var avsevärt högre i lungor från emfysemsgruppen. Även om studien inte var tillräckligt stor för att exakt koppla IRF5 till symtomens svårighetsgrad eller försämringsperioder, matchade mönstret fynden från mössen: mer IRF5 i sjuka lungor, mindre i friskare.
Vad detta kan innebära för framtida behandlingar
Tillsammans målar arbetet upp IRF5 som en central koordinator av rökdriven lungskada. Den förstärker en celldödsmekanism centrerad kring NLRP3 och styr immunceller bort från Ly6C‑höga populationer som verkar hjälpa till att bevara luftblåsornas struktur. För patienter är implikationen enkel: ett läkemedel som dämpar IRF5‑aktivitet skulle i teorin kunna reducera de mest destruktiva formerna av inflammation utan att stänga av immunsystemet helt. Även om sådana terapier ännu inte finns för KOL ger denna studie ett tydligt molekylärt mål och en biologiskt sannolik väg mot behandlingar som gör mer än att bara vidga trånga luftvägar — de skulle faktiskt kunna skydda lungans ömtåliga stomme.
Citering: Heo, SH., Park, S.Y., Kim, N.H. et al. Interferon regulatory factor 5 involves the pathogenesis of emphysema through NLRP3 and Ly6C expressing cells. Exp Mol Med 58, 425–435 (2026). https://doi.org/10.1038/s12276-025-01632-9
Nyckelord: emfysem, KOL, inflammation, lungimmunitet, celldöd