Clear Sky Science · ru
Кватернерная природа происхождения фибрилляции серповидного гемоглобина: исследование методом молекулярной динамики
Почему эта история о крови важна
Серповидно-клеточная анемия начинается с крошечного изменения в одном белке крови, но способна изменить форму эритроцитов, закупоривать сосуды и вызывать пожизненные боли. В этом исследовании проводится детальное, основанное на физике, изучение того, как именно эта единственная замена заставляет гемоглобин складываться в жесткие волокна внутри клетки. Используя современные компьютерные симуляции, авторы связывают атомные подробности с проблемами на уровне клетки и дают новые подсказки о том, как будущие лекарства могли бы препятствовать «залипанию» гемоглобина в кровотоке.
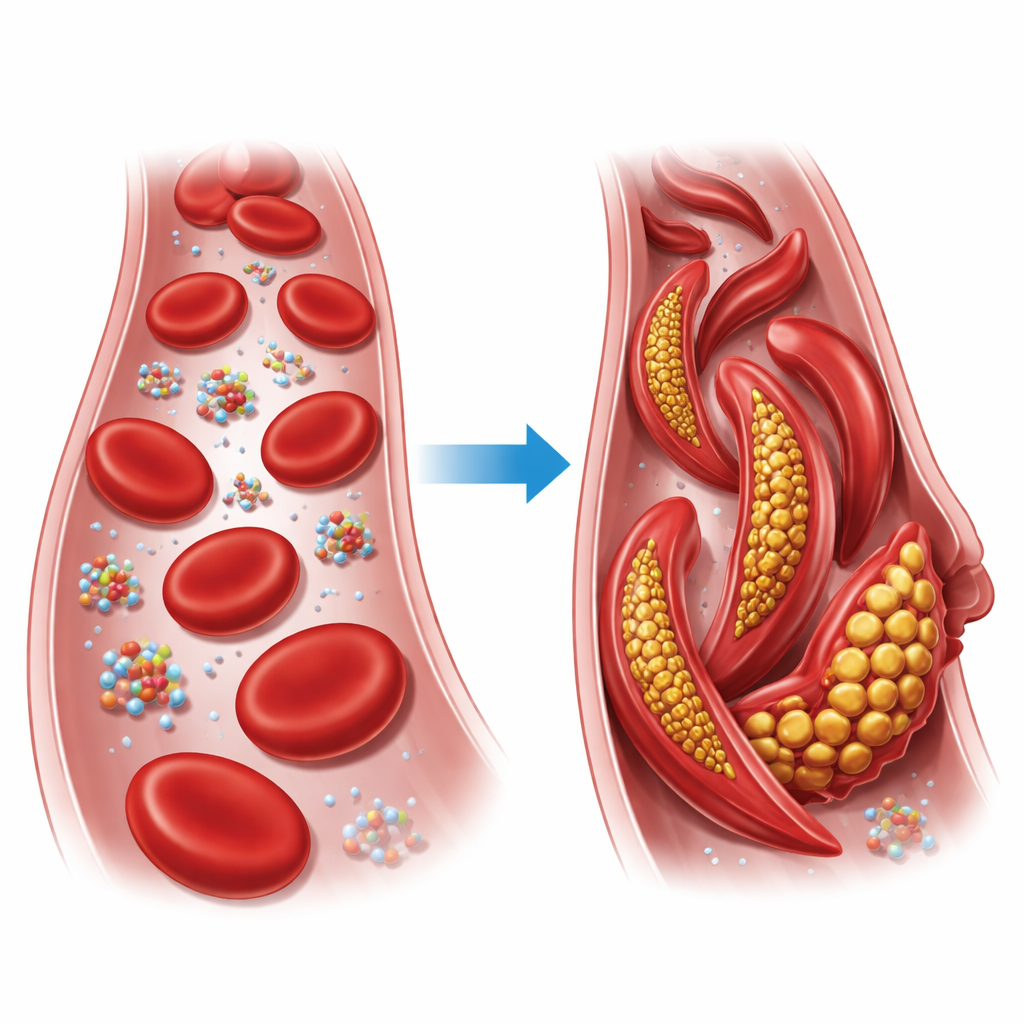
Маленькая замена с большими последствиями
Гемоглобин — это белок, переносящий кислород и заполняющий наши эритроциты. Каждая молекула гемоглобина состоит из четырех цепей, которые могут принимать две основные конформации — расслабленное (R) и напряженное (T) состояние. При серповидно-клеточной болезни в одной из этих цепей происходит замена всего одного остатка: зарядный глутамат замещается «жирной» валином на шестой позиции бета-цепи. При низком содержании кислорода такая измененная форма, называемая серповидным гемоглобином, объединяется в длинные волокна, которые искажают обычно круглые эритроциты в жесткие серповидные формы, способные закупоривать мелкие сосуды и лишать ткани кислорода.
Отслеживание меняющейся формы гемоглобина
Авторы сосредотачиваются на том, как целые молекулы гемоглобина поворачиваются и упаковываются друг относительно друга в волокне. Они отслеживают это масштабное изменение формы с помощью одного угла, измеряющего, как две половины белка скручиваются относительно друг друга. С помощью симуляций молекулярной динамики — виртуальных экспериментов, рассчитывающих движение атомов во времени в воде и соли — они плавно изменяют этот угол в широком диапазоне и вычисляют энергетическую стоимость каждой конформации. Они обнаруживают, что как нормальный, так и серповидный гемоглобин при температуре тела могут исследовать множество таких форм. Серповидный гемоглобин демонстрирует небольшое предпочтение одному из углов, но этих конформационных предпочтений недостаточно, чтобы объяснить, почему стабильно формируют волокна только серповидные молекулы.
Почему серповидные волокна сцепляются, а нормальные распадаются
Чтобы добраться до сути формирования волокон, исследование измеряет силу притяжения соседних молекул гемоглобина вдоль и поперек волокна. Команда вычисляет когезионную энергию — суммарную силу, удерживающую единицы вместе — для множества разных общих форм. Для серповидного гемоглобина эта когезионная энергия остается отрицательной (то есть привлекательной) на всем протестированном диапазоне углов, поэтому волокна остаются стабильными и не распадаются легко. Для нормального гемоглобина, напротив, в некоторых конформациях когезионная энергия становится положительной, что делает волокна на таких углах нестабильными и склонными к самопроизвольному разрушению. Ключевое различие — в том, как мутировавшие боковые цепи валина заправляются в соседние белки: у серповидного гемоглобина эти «жирные» участки образуют прочные контакты как в боковом направлении, так и вдоль оси волокна, прямо способствуя росту волокна.
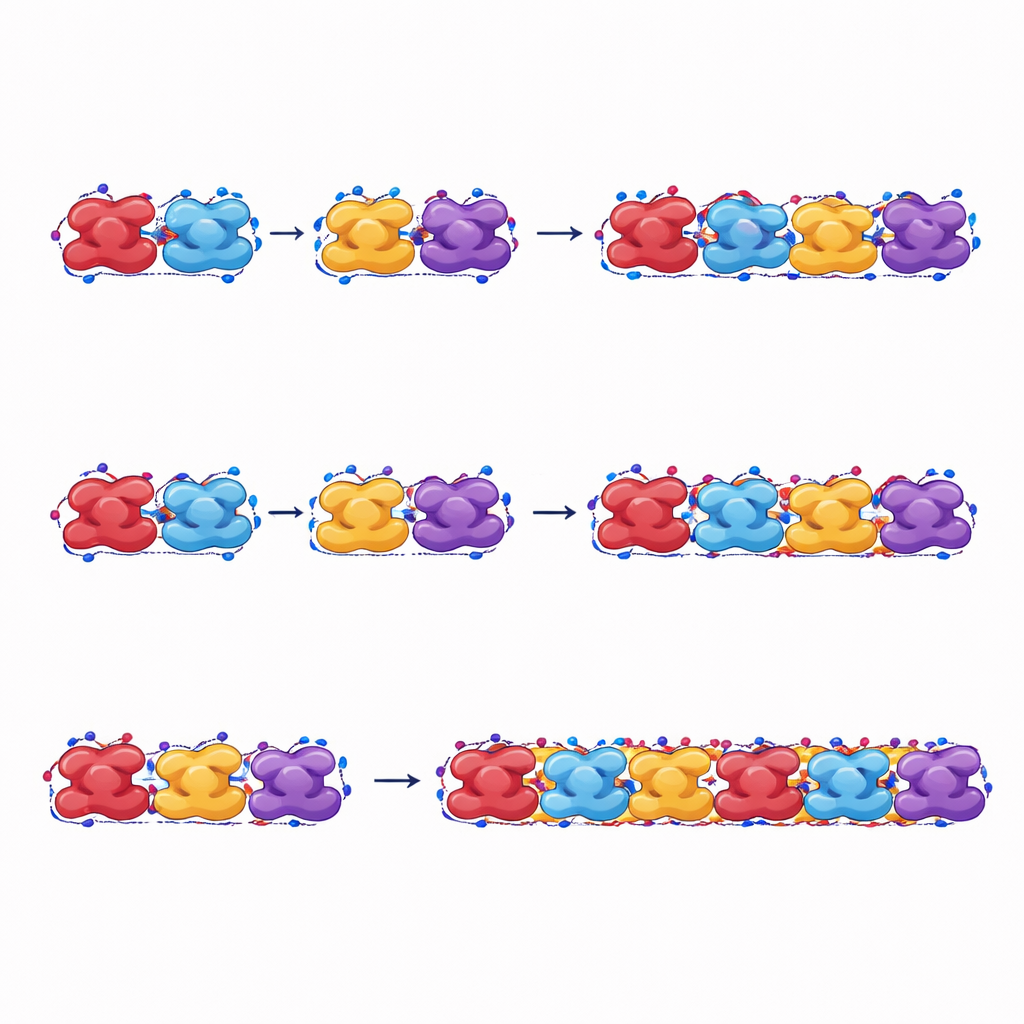
Как эти волокна выдерживают нагрузку и разрушаются
Авторы также растягивали смоделированные волокна, чтобы имитировать механическое напряжение. При растяжении вдоль своей длины волокна из серповидного гемоглобина выдерживали более высокие силы и деформации и рассеивали больше энергии перед разрывом, чем волокна из нормального гемоглобина. Даже расслабленная форма серповидных волокон, которая не является той, в которой волокна первоначально появляются, все же может сохранять целостность цепочки за счет пластических изменений формы, помогая волокну удерживаться после формирования. Волокна нормального гемоглобина, напротив, легче разделяются между соседними единицами и поглощают меньше энергии перед разрушением, что подтверждает их меньшую стабильность под нагрузкой.
Подсказки для будущих терапий и новых материалов
В совокупности симуляции показывают, что одна замена аминокислоты меняет способ взаимодействия молекул гемоглобина, скручивая общую сборку в углы, которые усиливают притяжение, особенно в напряженном состоянии. Эта комбинация геометрии и «липкости» позволяет серповидному гемоглобину образовывать длинные жесткие волокна, устойчивые к тепловому движению и механическому растяжению, что в конечном итоге деформирует эритроциты и блокирует кровоток. Указывая на конкретные особенности общей организации белка, которые контролируют стабильность волокон, работа предполагает, что эффективные антисерповидные препараты могли бы действовать, смещая гемоглобин в конформации, где образование волокон становится энергетически невыгодным и механически хрупким — превращая смертельную молекулярную пробку обратно в свободно текущий кровоток.
Цитирование: Jiang, M., Qin, Z. The quaternary structure origin of the fibrillation of sickle hemoglobin: a molecular dynamics study. npj Soft Matter 2, 7 (2026). https://doi.org/10.1038/s44431-026-00019-8
Ключевые слова: серповидно-клеточная анемия, волокна гемоглобина, агрегация белков, молекулярная динамика, заболевания крови