Clear Sky Science · ru
Преодоление разрыва между вычислениями и экспериментом: использование больших языковых моделей для приоритизации терапий при болезни Альцгеймера на основе сравнения обучающих моделей
Почему это важно для семей и пациентов
Болезнь Альцгеймера лишает людей памяти, независимости и качества жизни, при этом по-настоящему эффективные методы лечения по‑прежнему редки. В этом исследовании рассматривается более быстрый способ поиска новых терапий с использованием уже существующих препаратов — путем сочетания мощных вычислительных моделей с большой языковой моделью (тот же тип ИИ, что применяется в повседневных чатботах) для обработки огромного объема медицинских данных и научных статей. Цель — сократить длинный список возможных препаратов до небольшого, реалистичного набора, который ученые и врачи смогут реально проверить на пациентах.
Повторное использование старых лекарств для новой цели
Создание полностью нового препарата с нуля может занять более десяти лет и стоить миллиарды долларов без гарантии успеха. Альтернативой является «переназначение лекарств» — поиск новых применений для препаратов, уже одобренных для других состояний, например при болезни Паркинсона или депрессии. Поскольку у таких препаратов известны профили безопасности, они часто могут быстрее перейти в клинические испытания для Альцгеймера. Но современные компьютерные методы, которые сканируют биологические базы данных и медицинскую литературу, теперь генерируют огромные списки кандидатов — значительно больше, чем исследователи способны реально оценить вручную — что создает новое узкое место в процессе.
Объединение нескольких продвинутых моделей
Исследовательская команда решила эту задачу, создав рамочную систему переназначения лекарств для болезни Альцгеймера, которая стартует с трех разных продвинутых вычислительных моделей. Каждая модель анализирует большой биомедицинский «чертеж», называемый графом знаний, связывающий болезни, препараты, гены и другие медицинские понятия, и предлагает лекарства, которые могли бы помочь при Альцгеймере. Поскольку каждая модель обнаруживает паттерны по‑разному, их списки не полностью совпадают. Авторы объединили по 30 лучших предложений от каждой модели в единый пул из 90 кандидатов, а затем использовали большую языковую модель (LLM) в роли автоматического, но осторожного рецензента: она читала опубликованные исследования по каждому препарату и оценивала, выглядели ли аргументы за применение при Альцгеймере полезными, нейтральными или вредными.
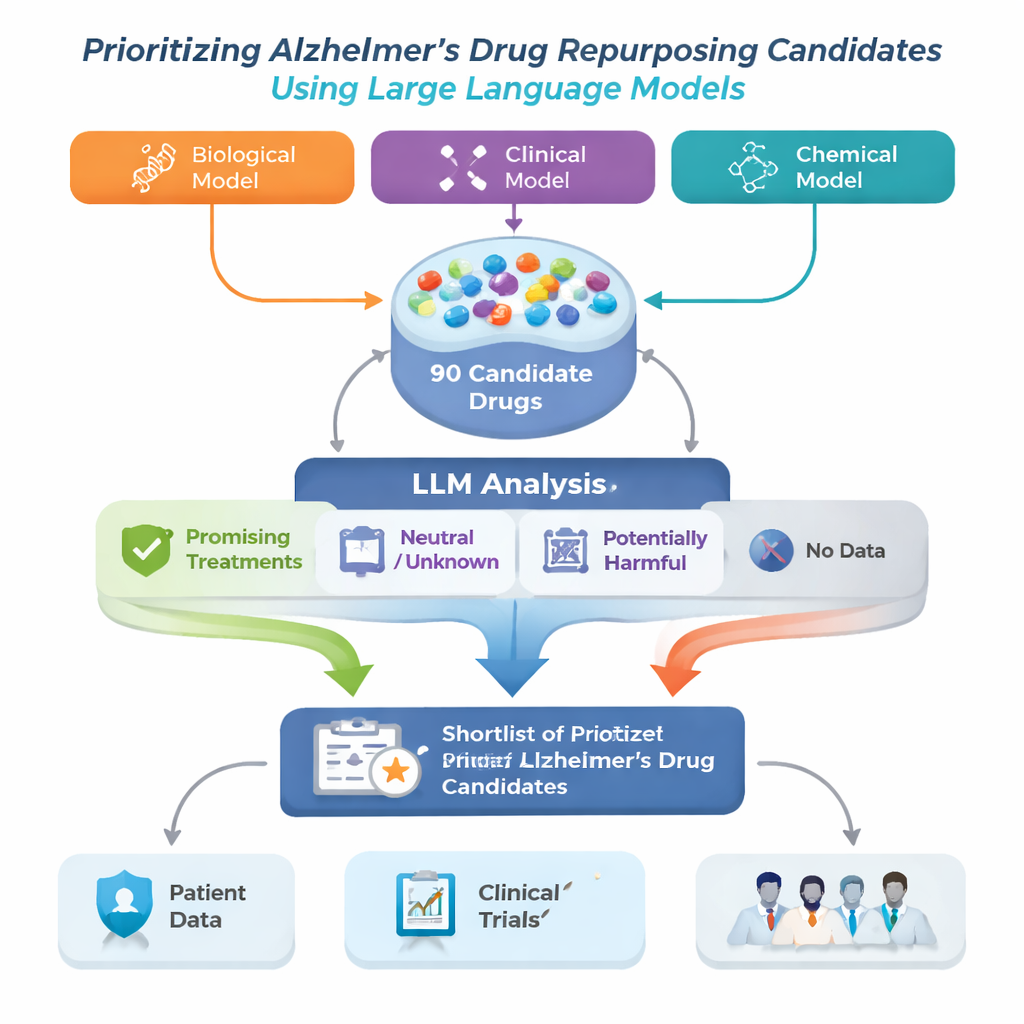
Как ИИ «читает» медицинскую литературу
Для каждого кандидата система извлекала до 200 научных аннотаций из PubMed и подробные описания препаратов из фармацевтической базы данных. LLM инструкировали основывать своё суждение только на показанном ей тексте и помечать каждую аннотацию как положительную, нейтральную или отрицательную в отношении лечения Альцгеймера. Эти метки затем переводились в простые оценки: долю аннотаций, помеченных как положительные, нейтральные или отрицательные. С использованием двух наборов правил — более строгого, требующего явных положительных доказательств, и более мягкого, отмечающего любое намёк на пользу — система сортировала препараты по четырем группам: перспективные терапии, потенциально вредные, неясные или нейтральные и препараты без публикаций, связанных с Альцгеймером. Эта последняя группа, хотя и малоизученная, может содержать особенно новые возможности.
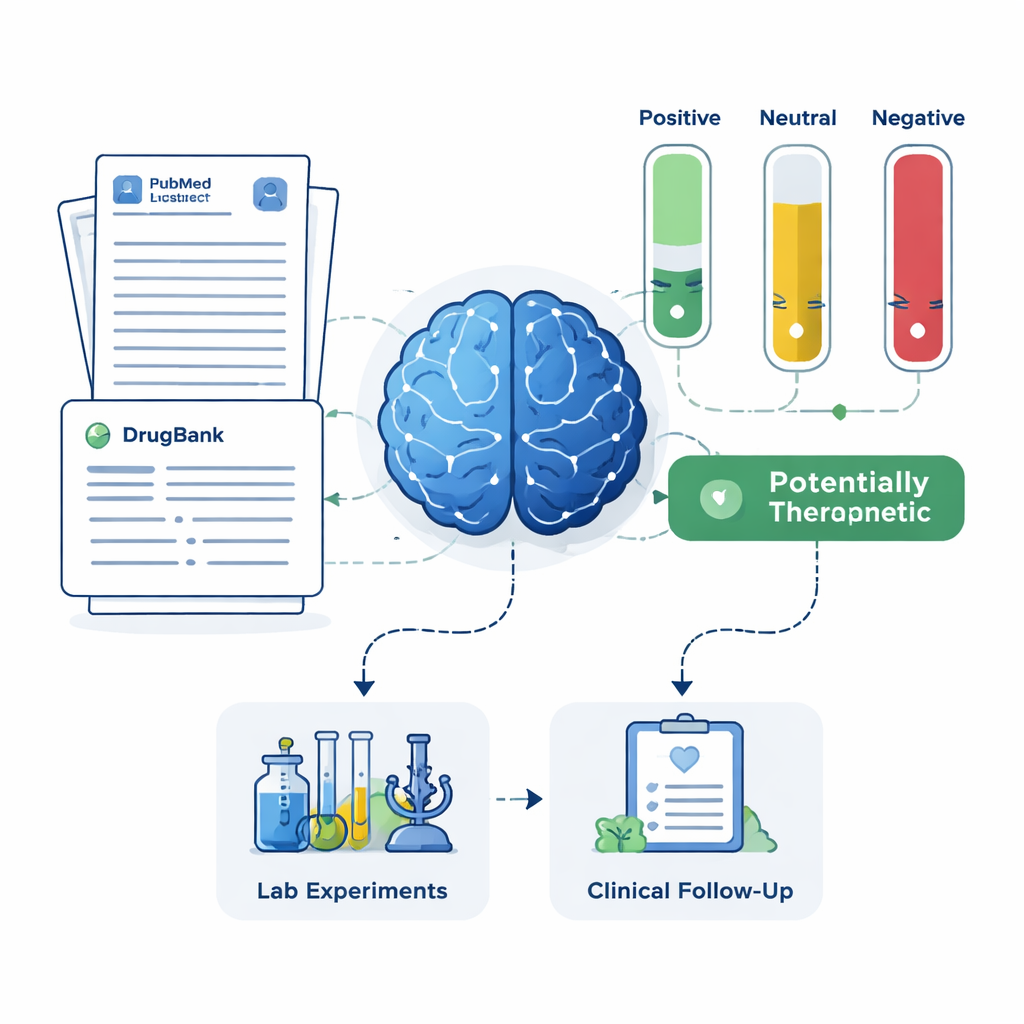
Сопоставление с реальными пациентами и клиническими испытаниями
Чтобы проверить, имело ли короткое соглашение ИИ смысл в реальном мире, команда сравнила свои результаты с двумя независимыми источниками: крупным регистром пациентов с Альцгеймером и записями о зарегистрированных клинических испытаниях. Система успешно выявила мемантин — существующий препарат при Альцгеймере с сильными защитными сигналами в данных пациентов и обширной историей испытаний — как кандидат с высоким приоритетом. Она также выделила такие препараты, как магний, миноциклин, пимавансерин, тестостерон и доксициклин, которые имеют разный уровень поддерживающих исследований, но считались многообещающими экспертными клиницистами. В то же время система идентифицировала препараты, литература по которым указывала на возможный вред или отсутствие пользы, и рекомендовала снизить их приоритет либо исследовать на предмет побочных эффектов, а не рассматривать для лечения.
От компьютерных предсказаний к практическим шагам
В обыденном смысле эта рамочная система действует как сверхбыстрый, внимательный научный помощник, который читает тысячи статей, сверяет паттерны в больших медицинских базах данных и передает экспертам-людям гораздо короче и лучше организованный список кандидатов на лекарства от Альцгеймера для дальнейшей работы. Исследование показывает, что сочетая разные типы ИИ — графовые модели для генерации идей и языковую модель для оценки доказательств — исследователи могут быстрее находить как хорошо обоснованные препараты, так и интересные новые варианты для тестирования. Хотя этот подход сам по себе не лечит Альцгеймер, он предлагает мощный новый способ связать вычислительно сгенерированные идеи с кропотливой работой лабораторных экспериментов и клинических испытаний, потенциально ускоряя путь к более эффективным методам лечения.
Цитирование: Li, M., Niu, S., Xu, Y. et al. Bridging the computational-experimental gap: leveraging large language model to prioritize Alzheimer’s therapeutics based on comparison of learning models. npj Health Syst. 3, 20 (2026). https://doi.org/10.1038/s44401-026-00074-3
Ключевые слова: Болезнь Альцгеймера, переназначение лекарств, искусственный интеллект, большие языковые модели, графы знаний