Clear Sky Science · ru
Мутация APP E590D увеличивает образование пептидов Aβ и Aη и усугубляет тау-патологию
Почему эта редкая мутация важна
Болезнь Альцгеймера обычно воспринимают как медленное накопление двух вредных белков — амилоида и тау — в головном мозге. У большинства людей болезнь развивается без единой очевидной причины, но в некоторых семьях встречаются редкие изменения в генах, которые могут резко изменить баланс. В этой работе изучается одно такое редкое изменение в гене предшественника амилоида (APP) и показано, как оно может существенно усилить выработку токсичных фрагментов белка и усугубить процесс, известный как тау-патология. Понимание этого редкого примера даёт подсказки, которые могут иметь более широкое значение для того, как запускается и затем ускоряется болезнь Альцгеймера.
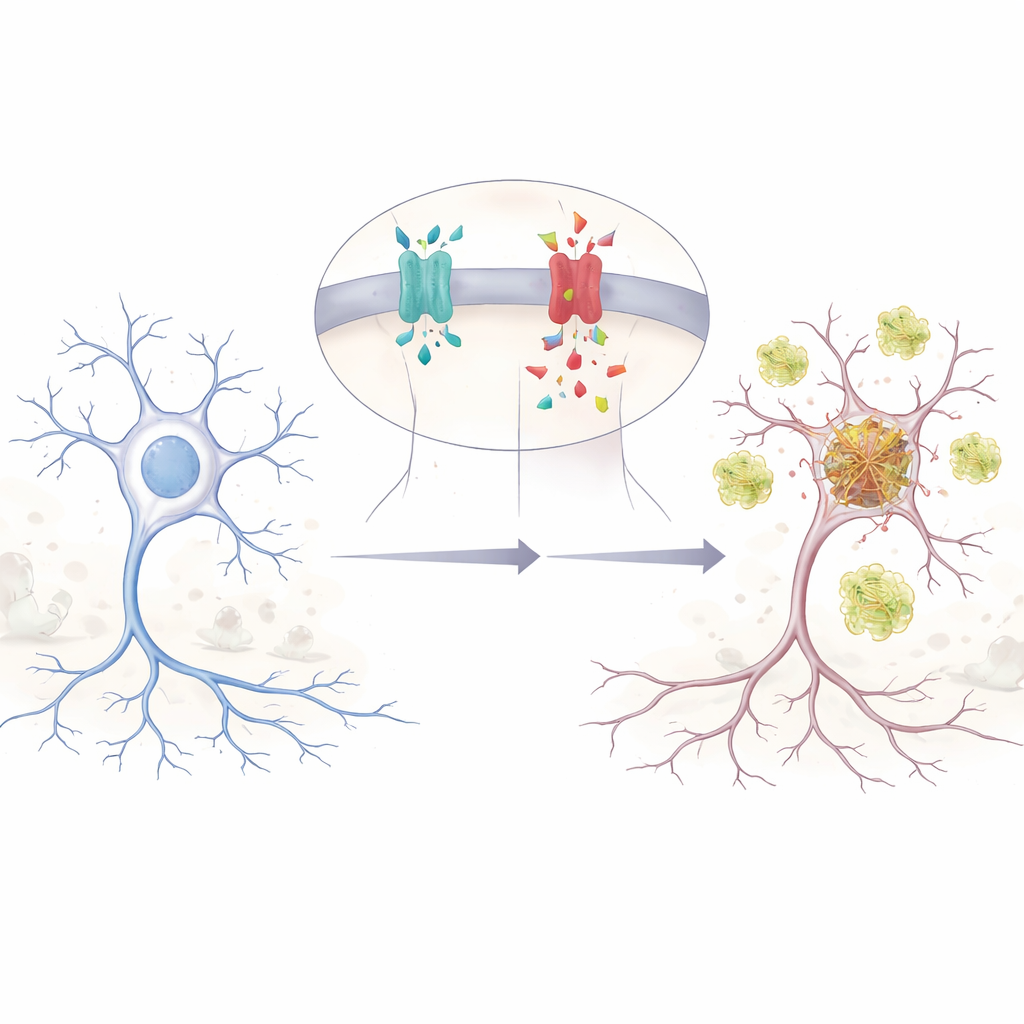
Небольшое генетическое изменение с большими последствиями
Авторы сосредотачиваются на однобуквенной замене в гене APP, обозначаемой как E590D в основной мозговой форме APP. Эта мутация была описана лишь у двух человек, у обоих с подтверждённой болезнью Альцгеймера в относительно молодом возрасте и с необычными, очень ранними нарушениями памяти и поведения. Из‑за своей редкости учёные сомневались, является ли она действительно причинным фактором или просто случайной находкой. Чтобы выяснить это, команда воссоздала мутацию в человеческих клетках и в нейронах мыши, затем проследила, как APP расщепляется на различные фрагменты. Они обнаружили, что мутантный APP производит значительно больше амилоида бета (Aβ) — липкого пептида, давно связанного с болезнью Альцгеймера — чем нормальный APP при сопоставимых уровнях.
Два токсичных пептида вместо одного
APP может разрезаться несколькими способами, подобно бревну, распиливаемому в разных местах. Классический путь при болезни Альцгеймера генерирует Aβ, но другой разрез даёт менее известный фрагмент, называемый Aη. Ранее показали, что Aη может повреждать связи между нейронами и ослаблять способность мозга укреплять воспоминания. В своих экспериментах исследователи обнаружили, что мутация E590D не только повышает уровень Aβ; она также значительно увеличивает уровни Aη и одного предшествующего фрагмента, который питает оба пути. Это означает, что мутация смещает обработку APP в сторону двойного удара токсичных пептидов, что потенциально нарушает работу мозговых цепей ещё до того, как можно ожидать появления классических амилоидных бляшек.
Как мутация ускоряет внутриклеточный трафик
Чтобы понять, почему образуется больше токсичных фрагментов, команда изучила, где локализуется APP и как он перемещается по поверхности клетки. Многие разрезы, создающие Aβ, происходят только после того, как APP захватывается внутрь клетки в процессе эндоцитоза. С помощью визуализации и биохимических приёмов, которые помечают белки на поверхности и отслеживают их внутренизацию, учёные показали, что мутантный APP менее представлен на внешней стороне клетки и быстрее захватывается в внутриклеточные отсеки, чем нормальный APP. Оказавшись в ранних эндосомах, APP встречается с ферментами, генерирующими Aβ, и изменённый трафик, по‑видимому, даёт этим ферментам больше возможностей действовать. Одновременно увеличивается и разрезание в η‑сайте на поверхности, что объясняет рост Aη.
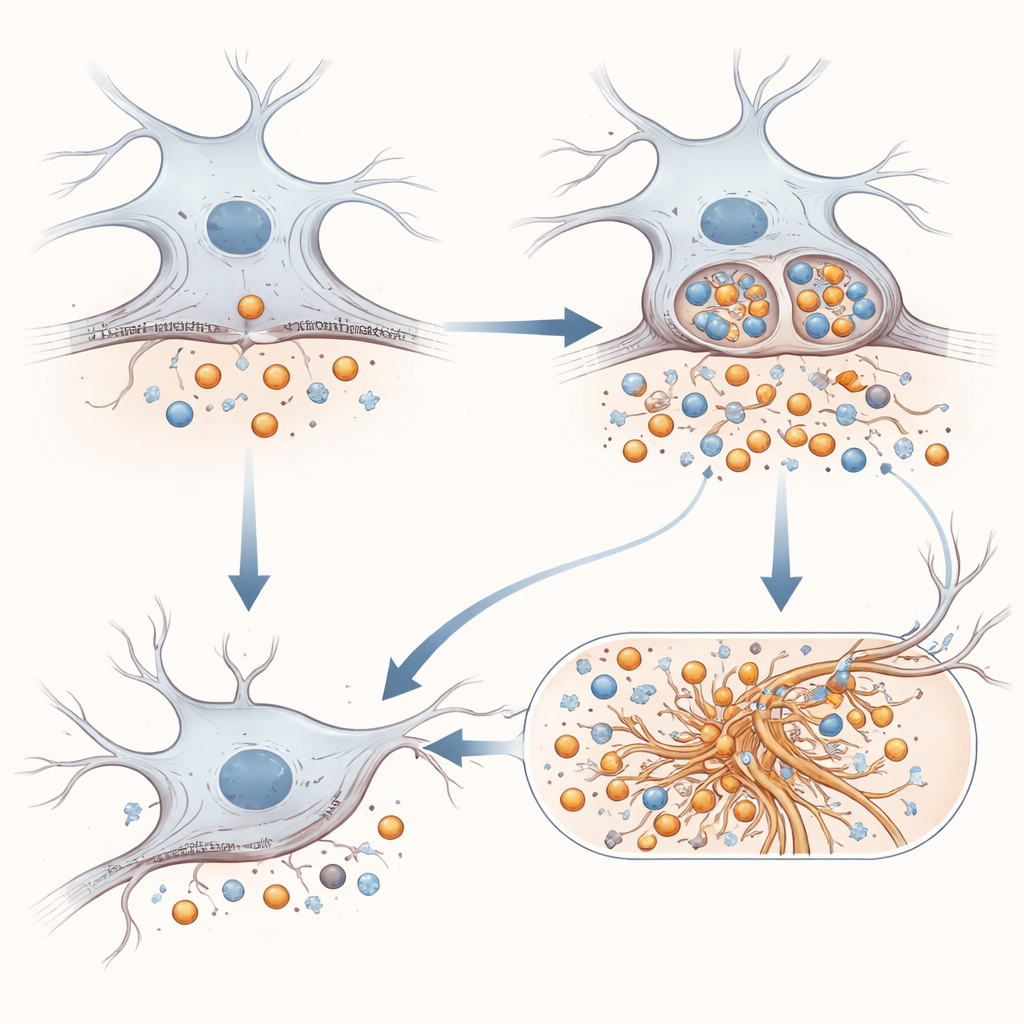
От фрагментов белка к спутанному тау и воспалению мозга
История не ограничивается лишь амилоидными фрагментами. Исследователи проверили, влияет ли мутантный APP на тау — структурный белок, образующий скрученные волокна при многих видах деменции. В клеточных моделях, которые загораются при посеве тау и образовании новых кластеров, присутствие APP с E590D приводило к более сильной агрегации, чем нормальный APP или отсутствие APP. В модели мыши, уже предрасположенной к проблемам с тау, введение вируса, экспрессирующего мутантный APP в гиппокамп, усугубляло образование тау-сплетений и вызывало более выраженную активацию астроцитов и микроглий — опорных и иммунных клеток мозга. Любопытно, что стандартные растворимые фрагменты амилоида было трудно обнаружить в этих мозгах мышей, но специфический фрагмент, происходящий от APP, появлялся только при наличии мутации, что указывает на изменённую обработку в живой ткани.
Что это означает для понимания болезни Альцгеймера
В сумме результаты показывают, что эта редкая мутация APP не является безобидной. Она сдвигает обработку APP в сторону выработки более чем одного токсичного пептида, ускоряет этапы внутренизации, благоприятствующие вредным разрезам, и усиливает спутывание тау и воспаление в мозге. Для неспециалистов ключевая идея в том, что биология болезни Альцгеймера определяется не одним «плохим актёром», а сетью взаимодействующих фрагментов белка и клеточных ответов. Изучение таких мощных, хоть и необычных генетических вариантов даёт увеличенное представление о этой сети. В данном случае это свидетельствует о том, что терапиям, возможно, придётся учитывать как амилоид, так и альтернативные производные APP-пептиды, такие как Aη, а также их совместное влияние на тау, вместо того чтобы нацеливаться на один путь в одиночку.
Цитирование: Liu, T., Wetzel, L., Roy, D. et al. APP E590D mutation increases generation of Aβ and Aη peptides and exacerbates tauopathy. npj Dement. 2, 21 (2026). https://doi.org/10.1038/s44400-026-00069-9
Ключевые слова: Болезнь Альцгеймера, предшественник амилоида (APP), тау-сплетения, нейровоспаление, генетическая мутация