Clear Sky Science · ru
Платформа высокого пропускного потока и количественного анализа с использованием 2D диссоциированных человеческих церебральных органоидов для моделирования нейровоспаления при болезни Альцгеймера
Почему инфекции могут играть роль в потере памяти
Болезнь Альцгеймера обычно описывают как медленное накопление липких белков в мозге, но накопленные доказательства указывают на то, что инфекции могут способствовать запуску этого процесса. В этом исследовании эту идею изучают с помощью крошечных лабораторно выращенных моделей человеческого мозга, чтобы ответить на простой вопрос: может ли распространённый вирус, вызывающий простудные волдыри, спровоцировать изменения в человеческих мозговых клетках, похожие на Альцгеймера, и способны ли противовирусные препараты частично обратить эти изменения?
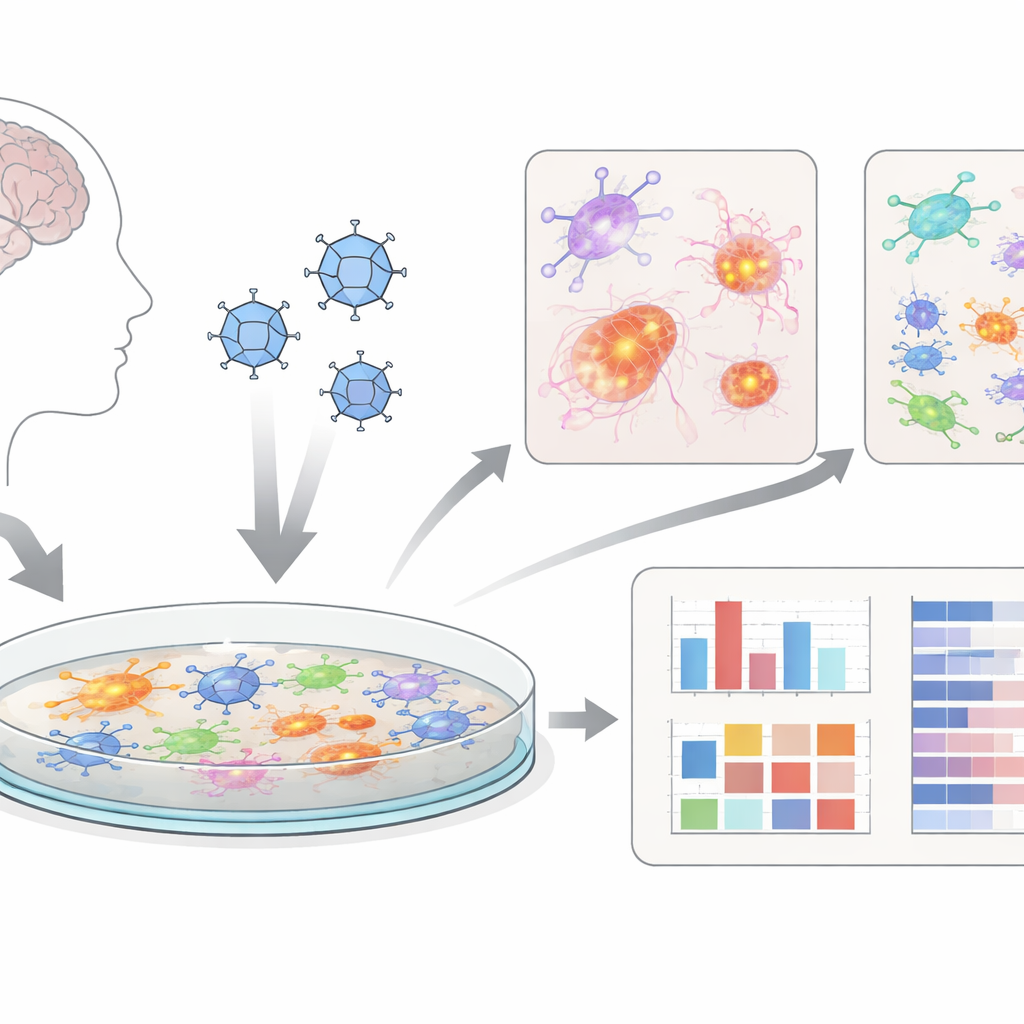
Мини‑мозги на чашке Петри
Вместо того чтобы работать только на животных, исследователи использовали «церебральные органоиды» — скопления клеток, похожих на мозговые, выращенные из человеческих стволовых клеток. Затем они осторожно расщепили эти трёхмерные органоиды на плоские слои смешанных мозговых клеток, включая нейроны, вспомогательные астроциты и иммуноподобные микроглии. Эти двумерные культуры, которые они называют dcOrgs, легче равномерно инфицировать и удобно исследовать в условиях высокого пропускного потока — то есть одновременно проверить многие пластины и лекарственные условия. Это делает систему привлекательной в качестве скринингового инструмента для новых лечений.
Вирус простуды как искра
Команда инфицировала dcOrgs вирусом простого герпеса 1 типа (HSV-1), вызывающим большинство простудных волдырей и давно подозреваемым в участии в развитии деменции у некоторых людей. Они сравнили инфицированные культуры с имитированными контрольными, с культурами, получившими антивирусный препарат (ацикловир), с культурами, подвергнутыми другому вирусу (грипп A), и с вирусом, инактированным ультрафиолетом. С помощью автоматизированного анализа клеток и одноклеточного секвенирования они подтвердили, что HSV-1 устойчиво инфицировал многие типы клеток в чашке, тогда как инактивированный вирус и грипп вызвали очень другие, более мягкие варианты изменений.
Альцгеймероподобные изменения внутри и между клетками
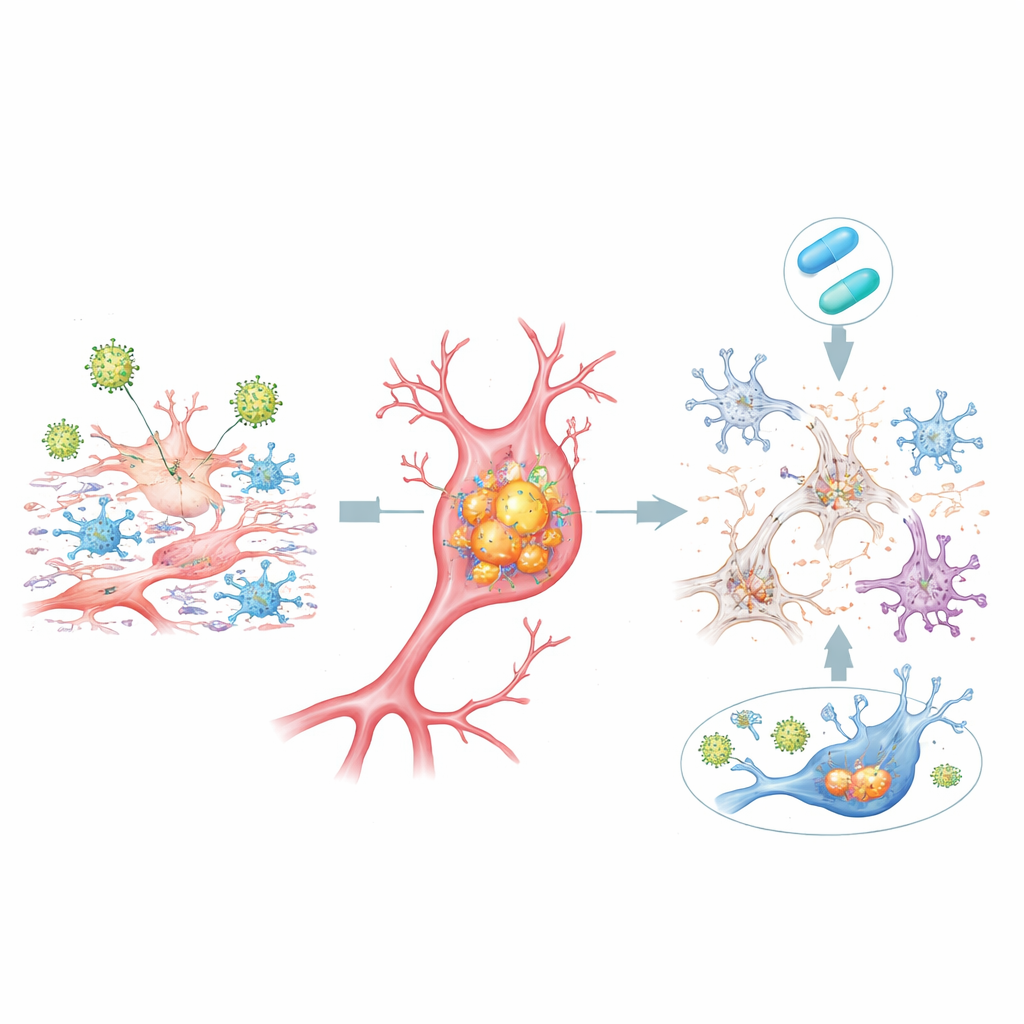
В dcOrgs, инфицированных HSV-1, многие клетки накапливали высокие уровни тех же форм белков, что и в мозге при болезни Альцгеймера: внутри клеток наблюдались скомпонованные бета-амилоидные отложения и несколько «фосфорилированных» форм тау — другого ключевого белка болезни. Эти накопления наиболее тесно ассоциировались с клетками, содержащими вирусные белки, и особенно выражались в умирающих клетках. Одновременно меньшие количества более длинного фрагмента бета-амилоида (Aβ42) выделялись в окружающую жидкость по сравнению с более короткими формами — сдвиг, который отражает паттерны, измеренные в спинномозговой жидкости пациентов с болезнью Альцгеймера. Также изменялись популяции клеток: число нейронов сокращалось, тогда как астроциты и микроглии увеличивались, что отсылает к потере нейронов и реактивному воспалению, наблюдаемым в тканях мозга пациентов.
Активность генов связывает модель с человеческой болезнью Альцгеймера
При изучении активности генов по всему геному исследователи обнаружили, что инфекция HSV-1 в dcOrgs включала и выключала многие гены, ранее связанные с риском Альцгеймера в больших генетических исследованиях у людей. Эти изменения не наблюдались в более простых культурах стволовых клеток или в dcOrgs, инфицированных гриппом, что указывает на специфическое взаимодействие между HSV-1 и смешанной мозгоподобной средой. Одноклеточное секвенирование показало, что часть сдвигов в генах, связанных с Альцгеймером, происходила в клетках, которые были подвергнуты воздействию вируса, но содержали мало или не содержали вирусного генетического материала сами по себе, намекая, что сигналы от инфицированных соседей могут распространять вредные воспалительные программы.
Что может и чего не может исправить антивирусное лечение
Добавление антивирусного препарата ацикловира вскоре после воздействия HSV-1 уменьшало экспрессию вирусных генов, ослабляло многие воспалительные ответы, снижало накопление токсичного бета-амилоида и тау внутри клеток и частично восстанавливало баланс различных типов клеток. Для значительной доли генов, связанных с Альцгеймером, уровни их активности смещались обратно в сторону нормы. Однако не все изменения были обратимы: значительная группа человеческих генов оставалась неизменной или даже ещё больше нарушалась лечением, особенно когда препарат был менее эффективен в блокировании поздних вирусных генов. Это подчеркивает, что хотя остановка репликации вируса может помочь, она не обязательно полностью отменяет биологическую каскаду, если та уже запущена.
Что это значит для понимания болезни Альцгеймера
Для неспециалиста вывод таков: человеческий вирус, вызывающий простудные волдыри, действуя в реалистичной смеси человеческих мозговых клеток, может быстро вызвать многие признаки болезни Альцгеймера — от белковых сгустков и умирающих нейронов до генетических паттернов, уже обнаруженных у пациентов. Плоская органоидная система, разработанная здесь, быстрая, количественная и масштабируемая, что делает её мощной площадкой для тестирования антивирусных препаратов и других терапий, направленных на снижение воспаления в мозге. Хотя это не доказывает, что инфекции герпеса вызывают болезнь Альцгеймера у каждого пациента, это укрепляет идею о том, что для части людей хронические или реактивирующиеся вирусные инфекции могут быть важной частью головоломки — и потенциальной мишенью для профилактики.
Цитирование: Olson, M.N., Barton, N.J., Feng, L. et al. A high-throughput, quantitative platform using 2D dissociated human cerebral organoids to model neuroinflammation in Alzheimer’s disease. npj Dement. 2, 20 (2026). https://doi.org/10.1038/s44400-026-00066-y
Ключевые слова: болезнь Альцгеймера, вирус простого герпеса, органоиды мозга, нейровоспаление, антивирусная терапия