Clear Sky Science · ru
Кодирование функциональных рёбер в графах для моделирования пространственно-варьирующихся связей в микроокружении опухоли
Почему важно картографировать «соседство» рака
Рак не растёт в изоляции. Опухолевые клетки существуют в оживлённом окружении иммунных клеток, клеток поддержки, кровеносных сосудов и химических сигналов, все они плотным образом расположены в пространстве. То, как эти «соседи» организованы и насколько сильно они влияют друг на друга, может определять, будет ли рак распространяться, реагировать на лечение или оставаться под контролем. В этой статье представлена SPIFEE — новая система искусственного интеллекта, превращающая микроскопические изображения и молекулярные карты опухолей в сети, что помогает исследователям выявлять, какие взаимодействия между клетками и путями наиболее связаны с типом заболевания и исходом для пациента.
Преобразование ткани в сетевую карту
Современные исследования рака измеряют гораздо больше, чем просто внешний вид опухоли под микроскопом. Одни методы отмечают десятки белков в отдельных клетках, другие дают подробные цветные срезы структуры ткани, а новые инструменты фиксируют активность генов в тысячах точек по срезу опухоли. SPIFEE рассматривает всё это как разные виды наблюдения за одним и тем же «районом». Он представляет каждый образец в виде графа: узлы обозначают ключевые элементы микроокружения опухоли — такие как типы клеток, визуальные паттерны ткани или молекулярные пути — а рёбра фиксируют, как эти элементы взаимодействуют в пространстве. Важный момент: SPIFEE не сводит взаимодействие к единому числу вроде «расстояния». Вместо этого каждое ребро хранит небольшой график (кривую), описывающий, насколько сильно две сущности смешиваются или отталкиваются друг от друга на разных расстояниях, сохраняя тем самым гораздо более богатую пространственную информацию.
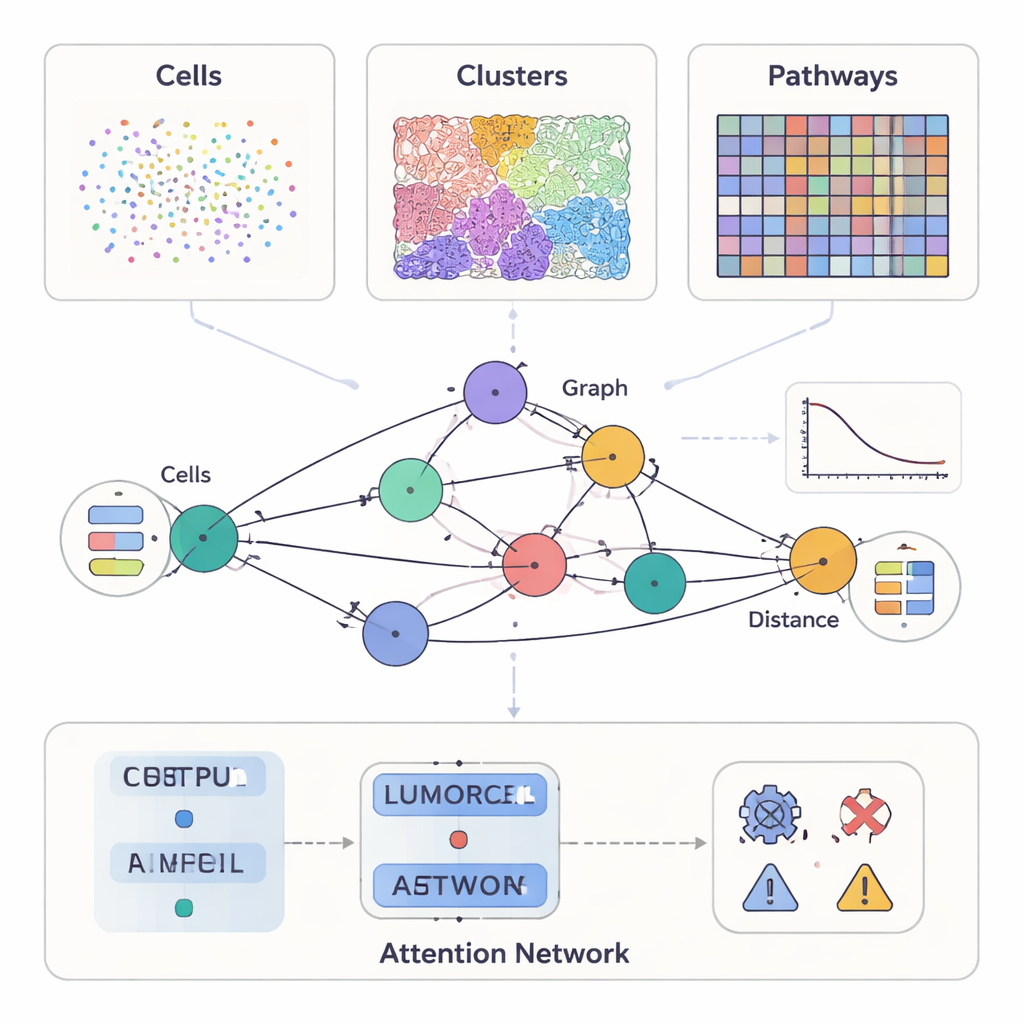
Гибкий инструмент для разных типов данных о раке
Авторы протестировали SPIFEE на нескольких больших независимых наборах данных по разным технологиям и масштабам. В образцах поджелудочной железы, помеченных мультиплексной иммунофлуоресценцией, каждый узел графа соответствовал типу клетки, а признаки узлов были получены из одноядерной/одно-клеточной РНК-секвенирования, суммирующего типичные коммуникативные свойства этих клеток. В срезах рака лёгкого, окрашенных рутинным методом гематоксилин-эозин, узлы представляли повторяющиеся визуальные паттерны ткани, автоматически обнаруженные системой самоконтролируемого обучения. В третьем случае стандартные слайды лёгкого были преобразованы с помощью глубокого обучения в виртуальную пространственную транскриптомику, и узлы SPIFEE соответствовали молекулярным путям, таким как гипоксия, эстрогеновый или JAK–STAT сигнальные каскады, с признаками, выведенными из активности генов. Во всех этих сценариях единая рамочная модель могла принимать разные типы узлов и при этом строить сопоставимые пространственные графы.
Поиск взаимодействий, которые отделяют разные исходы
После построения графа SPIFEE пропускает его через графовую сеть внимания — разновидность нейронной сети, которая учится не только предсказывать исход (например, подтип рака, риск смерти или различие между раком и нераковым воспалением), но и выделять, какие рёбра имели наибольшее значение для этого прогноза. В ткани поджелудочной железы SPIFEE точнее предыдущих методов на графах различал хронический панкреатит и аденокарциному поджелудочной протоки. Модель последовательно акцентировала взаимодействия, связанные с эпителиальными (опухелеподобными) клетками и регуляторными Т-клетками, антигенпредставляющими клетками и хелперными Т-клетками, указывая на иммуносупрессивное окружение, более выраженное при раке, чем при воспалении. В срезах аденокарциномы лёгкого SPIFEE выявил конкретные стромально-опухолевые паттерны, чьи взаимодействия коррелировали с более благоприятной или неблагоприятной выживаемостью, что позволяет предположить: «пограничные зоны» между опухолью и поддерживающей тканью несут важные прогностические подсказки, которые стандартные анализы могут пропускать.
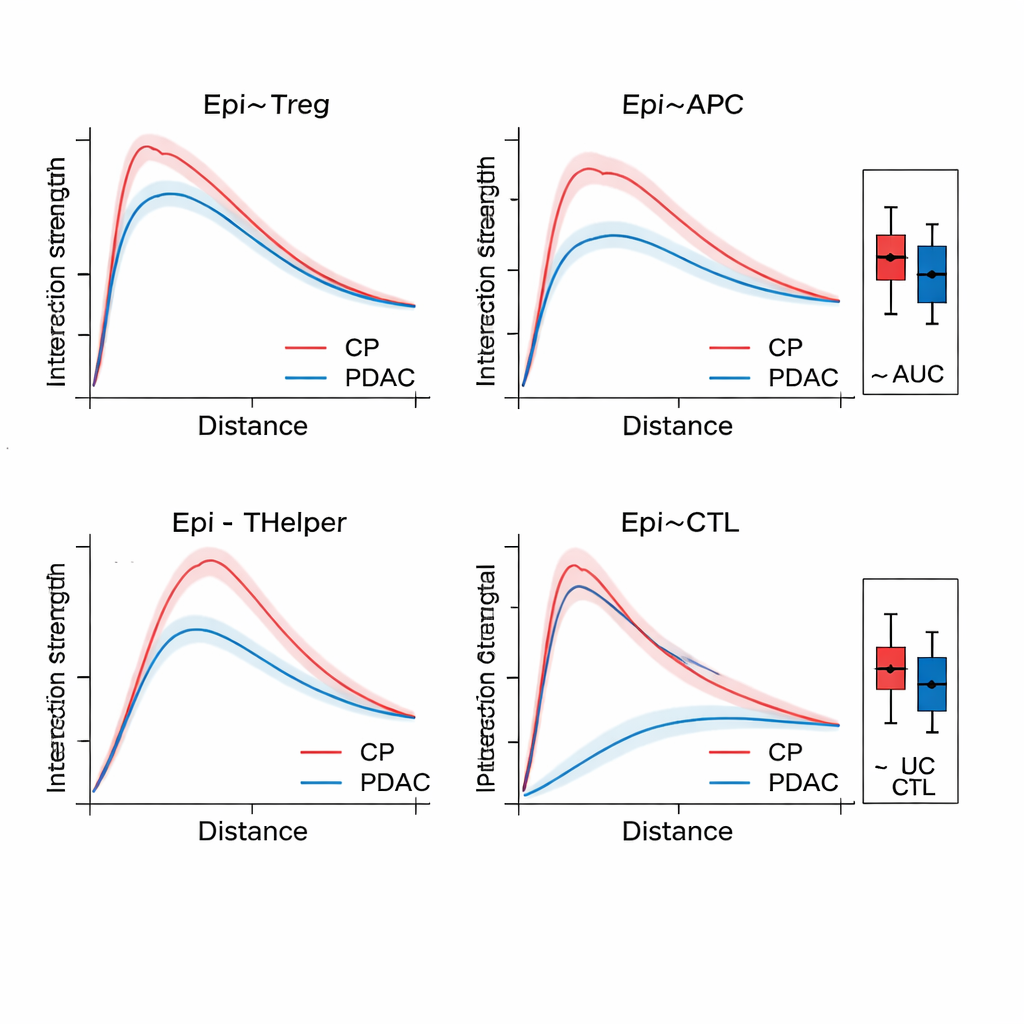
Чтение молекулярного перекрёстного общения по рутинным срезам
Возможно, самое примечательное: SPIFEE смог извлечь значимые взаимодействия путей из обычных патологических изображений после их преобразования в прогнозируемые карты активности генов. Рассматривая пути как узлы и их пространственную со-локализацию как функциональные рёбра, метод выделил пары, такие как гипоксия с EGFR или JAK–STAT с PI3K — комбинации, уже известные как движущие силы иммунного бегства и лекарственной устойчивости в раке лёгкого. Также были подчеркнуты эстроген-связанные пути в аденокарциноме лёгкого и некоторые иммунные и стрессовые пути в плоскоклеточных опухолях, что соответствовало шаблонам, наблюдаемым в массивной РНК-секвенировании и в независимом наборе реальных пространственных транскриптомных данных. Это указывает на то, что даже при приближённом молекулярном измерении пространственные паттерны на рутинных слайдах всё ещё несут восстановимые сигналы о том, как ключевые пути взаимодействуют в живых опухолях.
Что это значит для будущей онкологической помощи
Для неспециалиста главный вывод таков: SPIFEE предлагает новый способ считывать «социальную жизнь» раковых клеток напрямую с изображений и молекулярных карт. Кодируя то, как связи меняются с расстоянием, вместо того чтобы сводить их к единичным оценкам, и используя нейросети с механизмом внимания для ранжирования наиболее значимых взаимодействий, эта рамочная модель может выявлять комбинации клеток, тканевых паттернов и путей, которые отличают типы рака и предсказывают выживаемость. Хотя эти результаты требуют биологической и клинической валидации, подходы вроде SPIFEE указывают на будущее, в котором рутинные образцы опухолей принесут не просто статичные снимки, а динамичные карты «горячих точек» взаимодействий, помогающие в диагностике, стратификации риска и в перспективе — в выборе персонализированной терапии.
Цитирование: Tsang, A.P., Krishnan, S.N., Kulkarni, R. et al. Encoding functional edges in graphs to model spatially varying relationships in the tumor microenvironment. npj Artif. Intell. 2, 27 (2026). https://doi.org/10.1038/s44387-026-00075-5
Ключевые слова: микроокружение опухоли, пространственная транскриптомика, графовые нейронные сети, патология рака, взаимодействия клеток