Clear Sky Science · ru
Нейросеть с учётом метаболизма выявляет пути, влияющие на эффективность и токсичность антибактериальных комбинаций
Почему это важно для повседневного здоровья
По мере того как всё больше инфекций перестаёт отвечать на привычные антибиотики, врачи всё чаще прибегают к сочетаниям препаратов. Но смешивание лекарств — палка о двух концах: правильная пара может устранить стойкие бактерии, а неправильная — повредить органы, такие как почки и печень. В этой работе предложен новый вычислительный подход под названием CALMA, призванный помочь учёным и клиницистам находить комбинации препаратов, одновременно мощные против микробов и менее вредные для пациентов.
Борьба с микробами без метода проб и ошибок
Традиционно поиск удачных антибиотических комбинаций подразумевает тестирование огромного числа пар или троек препаратов в лаборатории и на пациентах. Число возможных сочетаний растёт взрывоподобно с добавлением каждого нового препарата, что делает полное экспериментальное исследование нереалистичным. К тому же большинство существующих инструментов учитывают только, насколько сильно комбинации убивают бактерии, игнорируя возможный ущерб для тканей человека. Авторы утверждают, что для проектирования лучших схем лечения необходимо учитывать обе стороны уравнения: эффективность против патогенов и безопасность для людей.
Умная модель, понимающая клеточную химию
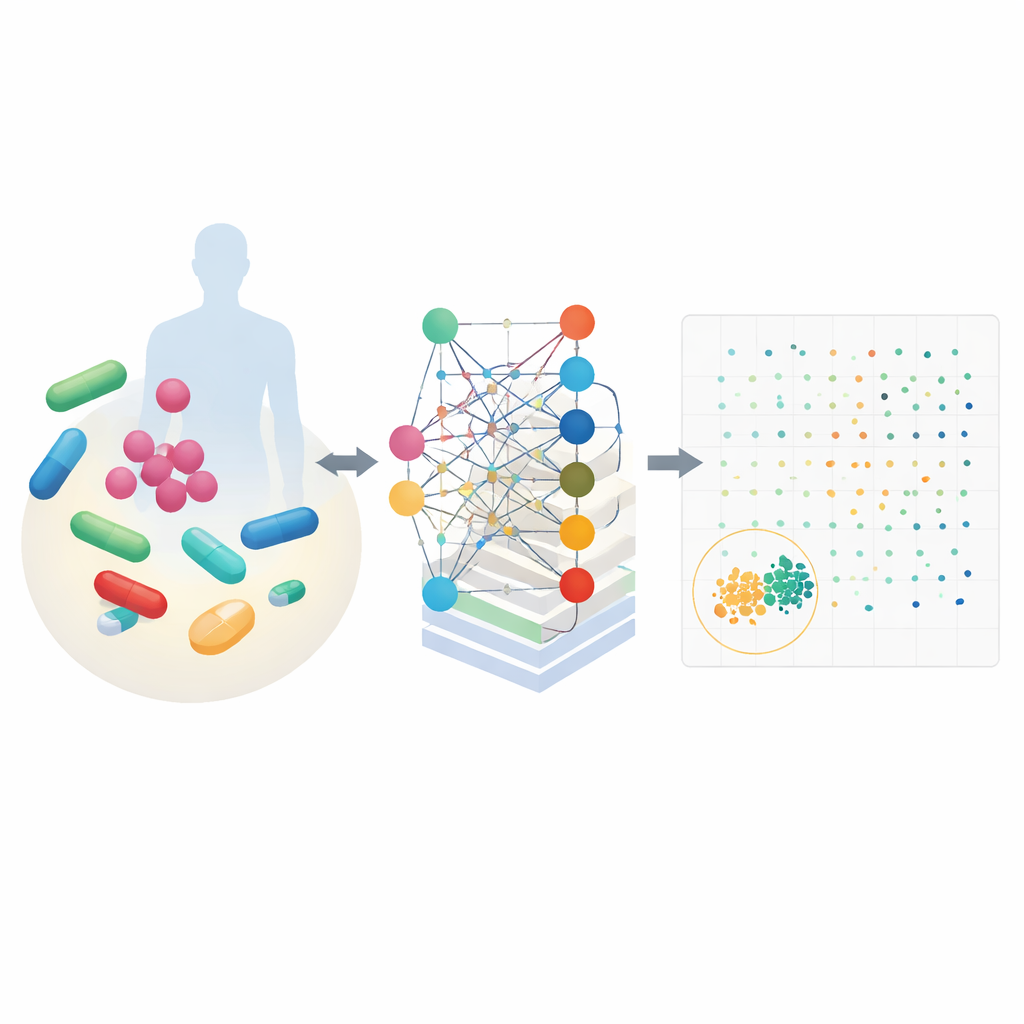
CALMA сочетает две мощные идеи. Во-первых, она использует подробные карты клеточного метаболизма, описывающие, как организмы превращают питательные вещества в энергию и строительные блоки. Эти карты, составленные для бактерий вроде Escherichia coli и возбудителя туберкулёза, моделируют, как тысячи химических реакций меняются под действием препарата. Во-вторых, CALMA подаёт эти симуляции в искусственную нейронную сеть, структура которой отражает метаболические пути. Группируя информацию по известным биологическим маршрутам — например, по выработке энергии или переработке нуклеотидов — модель учится находить связи между конкретными путями и либо эффективным уничтожением бактерий, либо вредными побочными эффектами для человеческих клеток.
Сканирование ландшафта лекарственных смесей
Используя данные предыдущих экспериментов и большие базы по безопасности, исследователи обучили CALMA присваивать каждой комбинации два показателя: один — за силу действия против бактерий, другой — за вероятность токсичности у людей. Нанесение этих показателей на график создаёт ландшафт, где лучшие кандидаты находятся в нижнем левом углу — сильные против микробов и щадящие для человеческих клеток. Применив CALMA к 35 клинически значимым препаратам, инструмент сократил примерно 600 возможных пар до небольшого набора перспективных вариантов, уменьшив объём экспериментальных испытаний примерно на 97 процентов. Среди лучших предложений оказались комбинации с такими распространёнными антибиотиками, как азитромицин, ванкомицин, изониазид и триметоприм.
От компьютерных предсказаний к лабораторным тестам и реальным пациентам
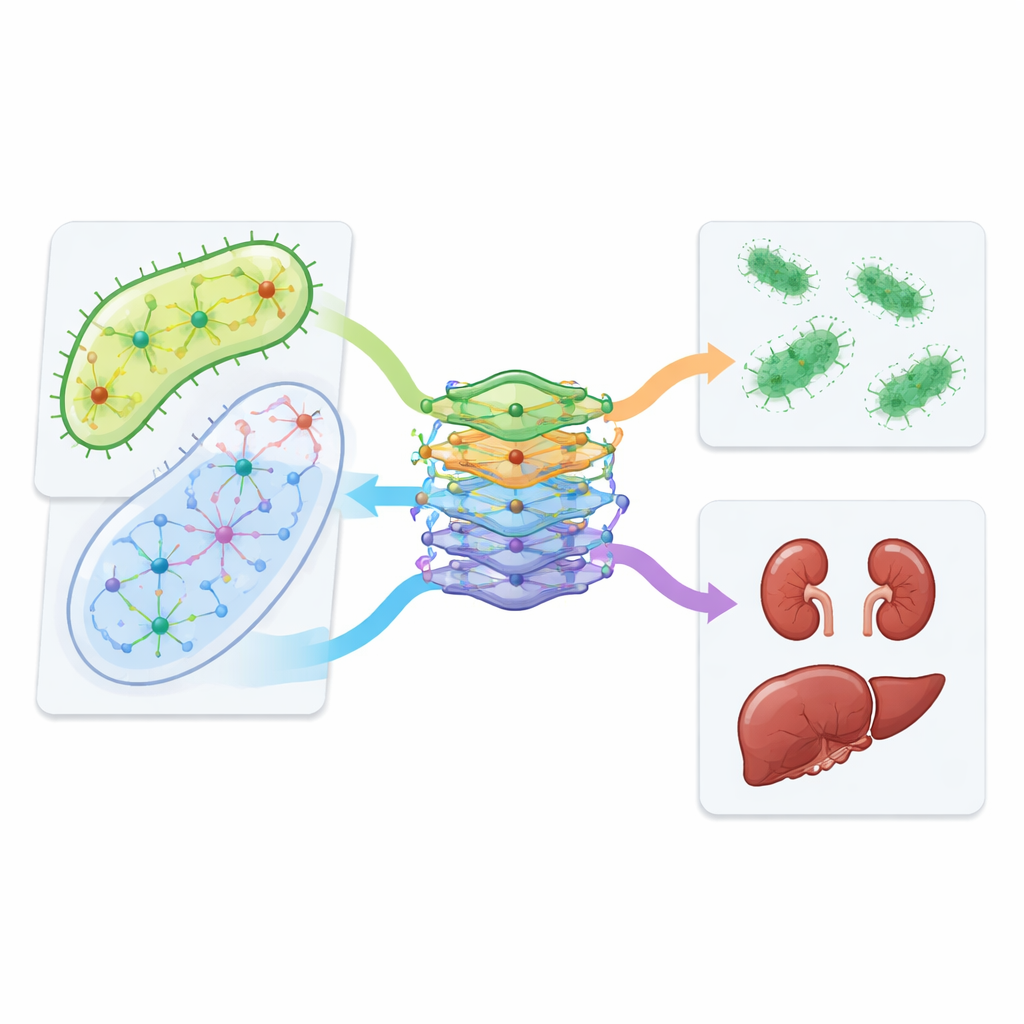
Команда перешла от симуляций к проверке нескольких предсказанных комбинаций на клеточных линиях почки и печени. Они обнаружили, что некоторые пары, включая азитромицин с ванкомицином и изониазид с триметопримом, были менее токсичны для человеческих клеток, чем отдельные препараты, при этом сохраняли активность против E. coli. Конструкция CALMA также позволила исследователям выяснить, какие метаболические пути обуславливают токсичность. Путь, участвующий в утилизации строительных блоков ДНК — так называемый нуклеотидный салваж — выделился как ключевой: его изменение в клеточных экспериментах меняло степень вреда от некоторых комбинаций. Наконец, авторы проанализировали медицинские записи сотен тысяч пациентов и обнаружили, что у людей, получавших азитромицин вместе с ванкомицином, реже фиксировались проблемы с почками по сравнению с пациентами, лечившимися только ванкомицином, что согласуется с лабораторными данными.
Что это означает для будущих методов лечения
Для неспециалиста CALMA можно представить как интеллектуальный фильтр, который понимает достаточно биологии, чтобы предложить, какие сочетания препаратов стоит проверять в первую очередь. Вместо того чтобы слепо смешивать антибиотики в надежде на лучшее, исследователи могут сосредоточиться на комбинациях, которые модель предсказывает как нацеленные на уязвимые места бактерий и при этом сохраняющие важные человеческие пути. Хотя метод зависит от доступных данных и далёк от совершенства, он предлагает более рациональный путь к разработке комбинированных терапий. Со временем инструменты наподобие CALMA могут помочь врачам безопаснее лечить резистентные инфекции, сократить метод проб и ошибок в разработке лекарств и даже быть адаптированы к другим заболеваниям, где сочетания лечения и побочных эффектов играют важную роль.
Цитирование: Arora, H.S., Lev, K., Robida, A. et al. A Metabolism-Informed Neural Network Identifies Pathways Influencing the Potency and Toxicity of Antimicrobial Combinations. npj Drug Discov. 3, 11 (2026). https://doi.org/10.1038/s44386-026-00042-9
Ключевые слова: комбинации антибиотиков, токсичность лекарств, искусственные нейронные сети, метаболизм, антибактериальная устойчивость