Clear Sky Science · ru
Генерация 3D‑молекул с ограничениями по взаимодействиям с использованием диффузионной модели позволяет моделировать фармакофоры на основе структуры для дизайна лекарств
Почему так трудно проектировать лучшие лекарства
Современное открытие лекарств часто сводится к тому, чтобы заставить небольшую молекулу войти в белок как ключ в замок. Но ключ должен делать не только это: он должен образовывать правильный набор крошечных притяжений — например слабых электрических взаимодействий и гидрофобных участков — чтобы препарат связывался прочно и специфично. Химическая вселенная астрономически велика, намного превышая содержимое нынешних баз данных, поэтому исследователи ищут более умные способы создавать новые «ключи» с нуля, сохраняя при этом эти важные схемы контактов.
Обучить компьютер понимать, что действительно важно
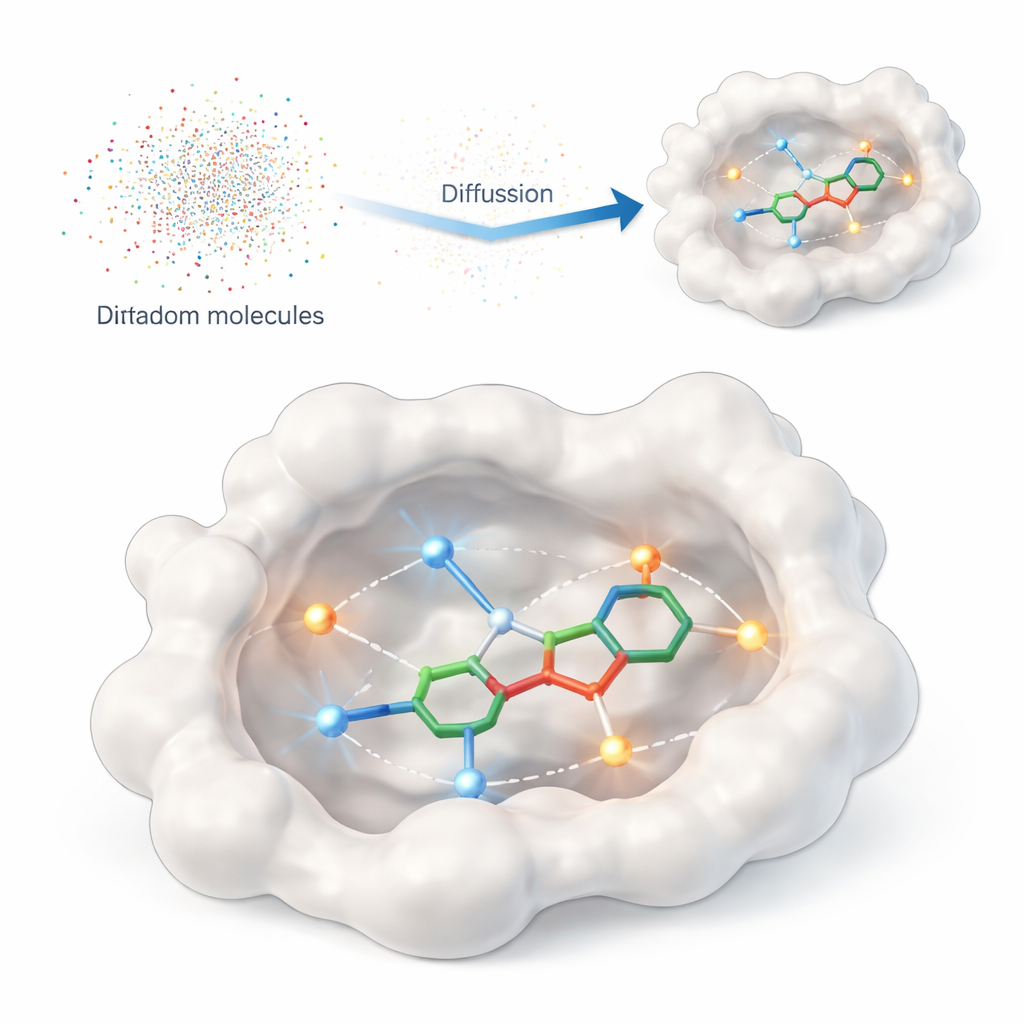
В этой работе представлена DiffPharma — вычислительная платформа, генерирующая трёхмерные молекулы, похожие на лекарства, непосредственно внутри сайта связывания белка. Вместо того чтобы просить алгоритм перебирать огромные каталоги существующих соединений, DiffPharma создаёт новые молекулы атом за атомом, руководствуясь тем, как они должны взаимодействовать с белком. Метод основан на современном классе генеративных моделей — диффузионных моделях, которые стартуют от случайного шума и постепенно «очищают» его в структурированный объект — в данном случае в 3D‑молекулу, расположенную в кармане белка.
Кодировка «рукопожатия» белка
Чтобы указать модели, что важно на поверхности белка, авторы представляют ключевые контакты в виде небольших «частиц взаимодействия», разбросанных вдоль путей между белком и эталонной молекулой. Выделяются два распространённых типа взаимодействий: водородные связи, действующие как направленные магниты между конкретными атомами, и гидрофобные контакты, где маслянистые участки собираются вместе, избегая воды. Отдельные нейросети изучают геометрию и химию каждого типа взаимодействия, а также общую форму кармана связывания; специальная архитектура слияния затем объединяет эти представления в единое согласованное «видение», которое направляет генерацию молекул.
Насколько хорошо это имитирует реальные шаблоны связывания?
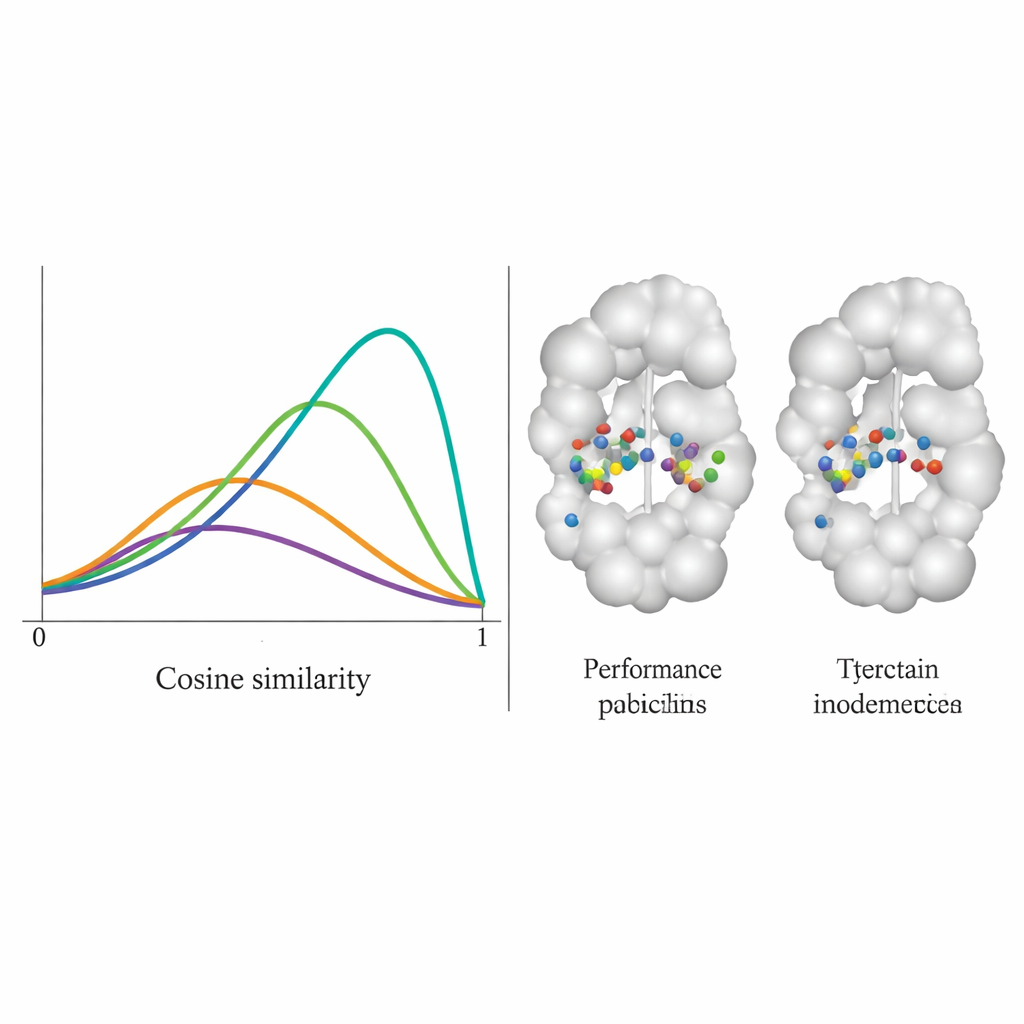
Команда протестировала DiffPharma на 100 различных парах белок–молекула и проверяла, насколько точно новые молекулы воспроизводят оригинальные схемы контактов по остаткам. Для оценки использовали меру косинусного сходства от 0 до 1, где 1 означает полное совпадение. Распределение DiffPharma имело пик около 0.9, то есть в среднем те же остатки белка образовывали те же типы ключевых взаимодействий, что и в эталонных структурах — существенно лучше по сравнению с шестью конкурующими методами. Важно, что модель добивалась этого, по‑прежнему порождая разнообразные молекулярные формы, а сгенерированные соединения сохраняли реалистичные длины связей, углы и общую 3D‑геометрию, характерные для реальных стабильных молекул.
От теории к практическим кандидатам в лекарства
Помимо бенчмарков, авторы проверили, может ли DiffPharma проектировать правдоподобные кандидаты для реальных мишеней. Для двух хорошо изученных ферментов — киназы AKT и β‑лактамазы, связанной с антибиотикорезистентностью — метод генерировал молекулы, сохраняя существенные схемы взаимодействий известных лигандов, но часто используя разные химические каркасы, что является желательной формой «скачка по каркасам» в медицинской химии. В более требовательном исследовании на главной протеазе SARS‑CoV‑2 DiffPharma направляли с помощью конкретных выборов взаимодействий, а затем изучали при помощи молекулярной динамики и оценок энергии связывания. Молекулы, сгенерированные при более строгих ограничениях по взаимодействиям, формировали более стабильные комплексы и иногда демонстрировали более благоприятные предсказанные энергии связывания, чем известный эталонный ингибитор. Примечательно, что система даже заново обнаружила этот эталонный препарат — несмотря на то что он никогда не встречался в обучающей выборке — исключительно на основе структуры белка и инструкций по взаимодействиям.
Что это значит для будущих лекарств
Для неспециалиста DiffPharma можно представить как умный инструмент проектирования, учитывающий 3D‑структуру: имея форму кармана белка и желаемую схему «рукопожатий», он предлагает химически правдоподобные «ключи», которые подходят и взаимодействуют нужным образом. Хотя метод ещё не оптимизирует все свойства, необходимые лекарству — такие как растворимость или метаболизм — он надёжно сохраняет ключевую карту контактов на поверхности белка и исследует новые области химического пространства за пределами существующих каталогов. Такой подход, управляемый взаимодействиями, может помочь исследователям быстрее перейти от структурных данных о белках, связанных с болезнью, к разнообразным, реалистичным отправным точкам для экспериментальной разработки лекарств.
Цитирование: Sako, M., Yasuo, N. & Sekijima, M. Interaction-constrained 3D molecular generation using a diffusion model enables structure-based pharmacophore modeling for drug design. npj Drug Discov. 3, 8 (2026). https://doi.org/10.1038/s44386-026-00040-x
Ключевые слова: структурно-обоснованный дизайн лекарств, молекулярные генеративные модели, моделирование фармакофора, взаимодействия белок–лиганд, главная протеаза SARS-CoV-2