Clear Sky Science · ru
Искусственный интеллект в соревновательной докинге для виртуального скрининга и предсказания эффективности соединений
Более умные поиски новых лекарств
Поиск новых препаратов похож на поиск иголки в стоге сена, состоящем из миллионов молекул. В этом исследовании показано, как последние достижения в области искусственного интеллекта могут ускорить и удешевить этот поиск, помогая учёным предсказывать, какие молекулы с наибольшей вероятностью прикрепятся к белку, связанному с заболеванием, и действительно сработают как лекарства. Вместо того чтобы тестировать по одной молекуле в лаборатории, авторы используют модели ИИ, чтобы устраивать виртуальные состязания между молекулами и позволять победителям подниматься наверх.
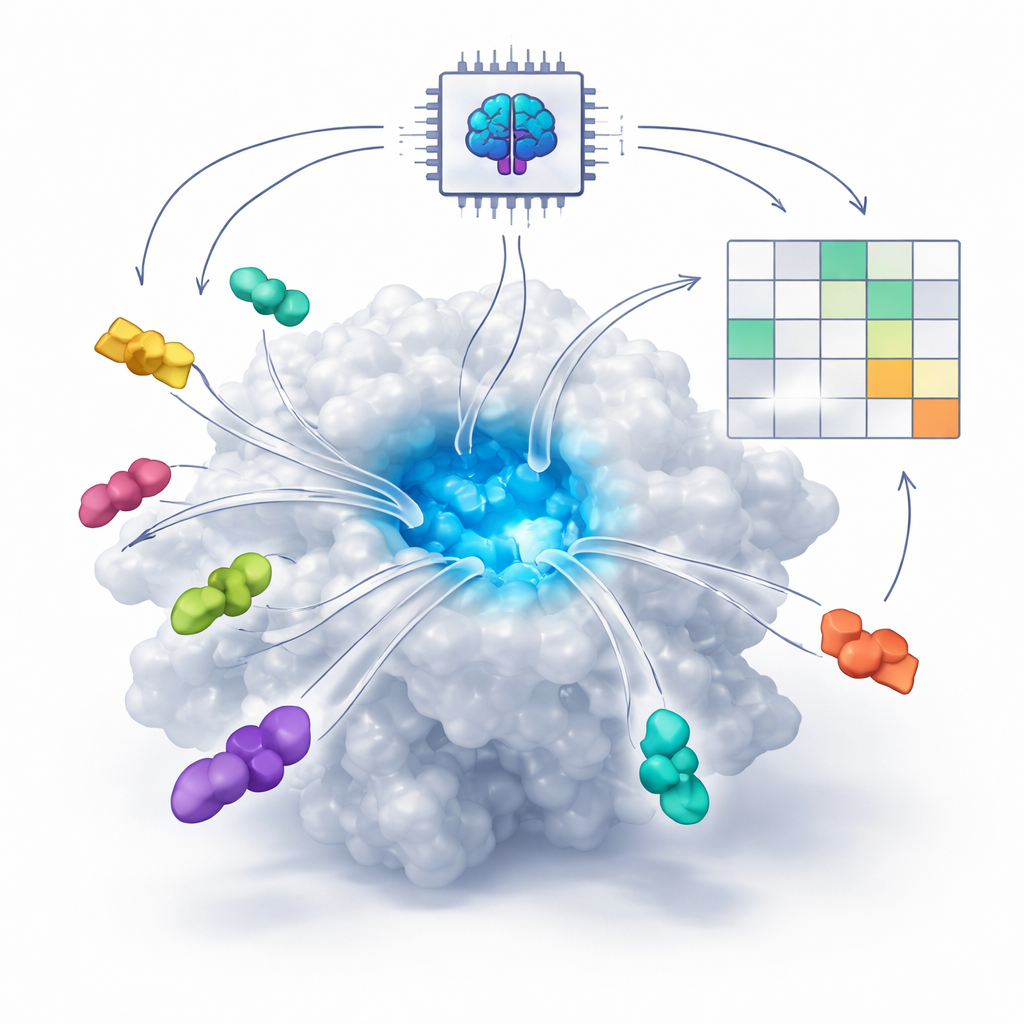
Как ИИ учится видеть соответствие «замок‑и‑ключ»
Многие современные лекарства действуют, помещаясь в крошечные карманы на белках, как ключ в замке. Традиционно компьютерные программы пытались предсказать это соответствие с помощью физических уравнений, оценивающих силы между атомами. Однако в последние годы новые системы ИИ, основанные на диффузионных моделях совместного сворачивания — такие как AlphaFold3 и Boltz — обучились на огромном числе известных структур белок–молекула. Эти системы теперь могут «представлять», как белок и потенциальный препарат могут совместно свернуться в трёх измерениях, даже когда экспериментальной структуры нет. Главный вопрос, который ставят авторы, заключается в том, могут ли эти инструменты ИИ делать не только правдоподобные картинки, но и отличать хорошие лекарства от плохих?
Истинные связывающие против притворщиков
Команда сначала протестировала 16 хорошо изученных белков и более сложный бактериальный фермент — ДНК-гиразу. Для каждого белка они попросили модели ИИ расположить как известные активные ингибиторы, так и набор посторонних «внецелевых» молекул в одном и том же сайте связывания. Вместо того чтобы полагаться на одно предсказание, они оценивали, насколько последовательно ИИ размещал каждую молекулу в многочисленных запусках. Истинные ингибиторы, как правило, возвращались в одно и то же положение и ориентацию снова и снова, образуя кластеры в пределах нескольких триллионных долей метра друг от друга. Неактивные молекулы блуждали сильнее и часто оказывались дальше от кармана. Эта простая идея — сходимость позы — оказалась сильным сигналом того, что соединение действительно подходит к своему белковому мишени.
Преобразование докинга в очное соревнование
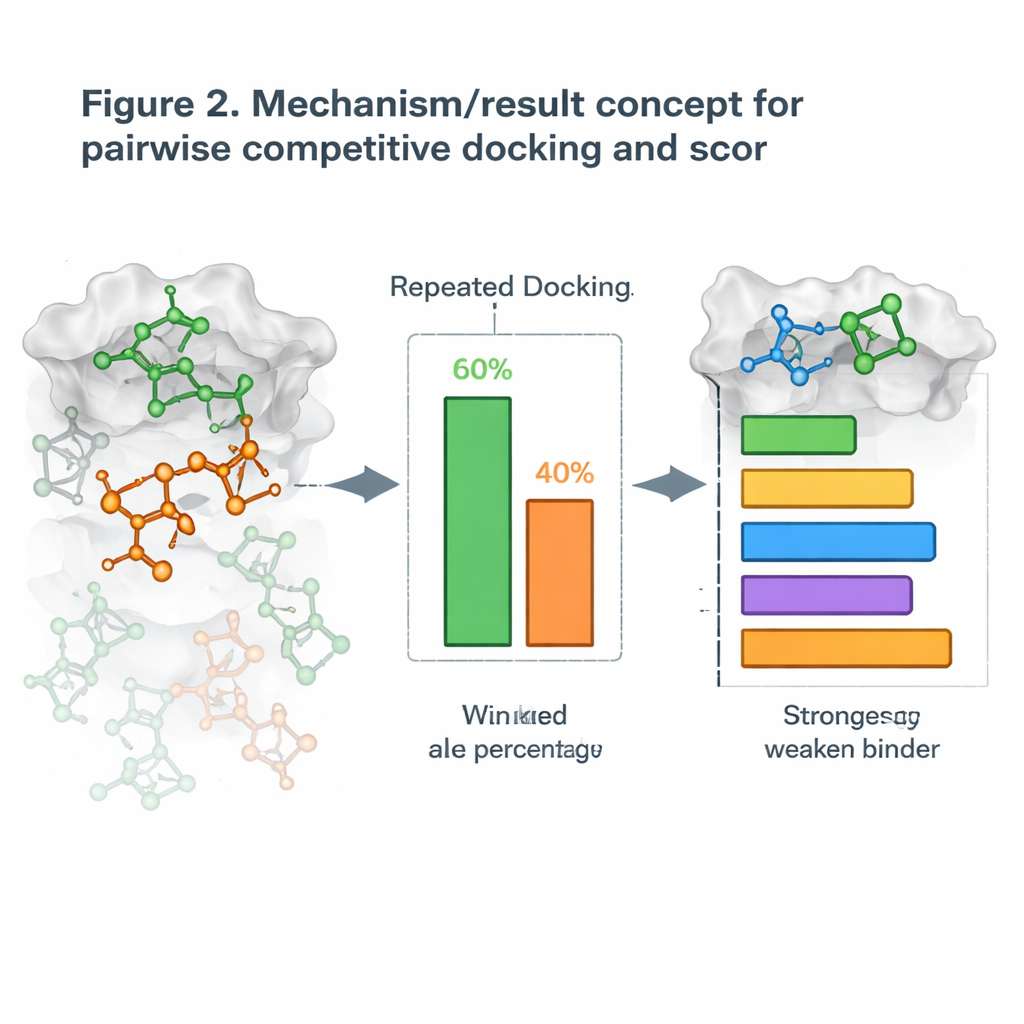
Исходя из этого, авторы предложили новую стратегию, которую назвали парным соревновательным докингом. Вместо докинга одной молекулы за раз они докингуют по две кандидатуры одновременно вместе с белком и позволяют им «сражаться» за один и тот же карман. После множества повторных запусков молекула, занимающая сайт чаще, объявляется победителем этой пары. Запустив все возможные пары, они формируют таблицу побед/поражений и вычисляют для каждой молекулы показатель Competitive Docking Score, подобно ранжированию игроков в круговом турнире. При сравнении этих оценок с реальными измерениями силы блокирования мишеней рейтинги часто хорошо совпадали, а для некоторых белковых систем достигалось почти идеальное соответствие.
От виртуального скрининга к разработке лучших антибиотиков
ДНК-гираза, фермент, необходимый бактериям, послужила подробным тестовым объектом. У этого белка есть несколько карманов, на которые нацелены разные классы антибиотиков, в том числе широко используемые фторхинолоны. Модели ИИ обычно могли правильно размещать каждый класс препаратов в соответствующем кармане, а показатели соревновательного докинга примерно отражали их измеренную активность. Затем авторы масштабировали подход до виртуального скрининга более 3000 одобренных препаратов, спрашивая, какие молекулы лучше всего конкурируют за сайт фторхинолонов. Их двухэтапная стратегия — сначала использовать «все сразу» конкуренцию, чтобы отобрать вероятных победителей, а затем фильтровать по тому, насколько плотно они сконцентрированы в кармане — значительно обогатила набор истинных фторхинолонов и отсеяла более слабые кандидаты. Наконец, они использовали генератор молекул на базе ИИ, чтобы предложить новые структуры, похожие на фторхинолоны, и применили соревновательный докинг, чтобы найти несколько соединений с ещё лучшим предсказанным связыванием и приемлемыми лекарственно-подобными свойствами.
Обещания, ограничения и что это значит для пациентов
Исследование показывает, что современные модели ИИ могут делать не только правдоподобные структуры белок–лекарство: в соревновательном режиме они могут помогать ранжировать соединения так, что это часто отражает реальные экспериментальные данные. Это не заменяет лабораторную работу — эффективность по‑прежнему сильно зависит от конкретного белка, некоторые карманы неверно предсказываются, и модели ИИ могут давать сбои для очень больших или необычных молекул. Но по мере улучшения этих моделей и их обучающих данных подходы вроде парного соревновательного докинга могли бы сделать ранние этапы разработки лекарств значительно эффективнее. Для пациентов это в перспективе может означать более быстрое создание целевых препаратов, включая новые антибиотики, идущие в ногу с устойчивыми к ним бактериями.
Цитирование: Mirgaux, M., Barcelli, V., Chua, A.C.Y. et al. AI-guided competitive docking for virtual screening and compound efficacy prediction. npj Drug Discov. 3, 6 (2026). https://doi.org/10.1038/s44386-026-00039-4
Ключевые слова: ИИ в разработке лекарств, виртуальный скрининг, молекулярный докинг, связывание белок-лиганд, создание антибиотиков