Clear Sky Science · ru
Разработка протокола для противодействия спонтанной ин витро активации кишечных фибробластов с использованием планирования экспериментов
Почему важно не допускать чрезмерной активности клеток, восстанавливающих кишечник
При хронических заболеваниях кишечника, таких как болезнь Крона, рубцовая ткань может постепенно сужать просвет кишечника до тех пор, что пища едва проходит, что часто приводит к хирургическим вмешательствам. Это образование рубцов, называемое фиброзом, вызывается поддерживающими клетками — фибробластами, которые становятся гиперактивными и откладывают чрезмерное количество внеклеточного матрикса. Чтобы понять этот процесс и в перспективе предотвратить его, ученым необходимы фибробласты, выращенные в лаборатории. Но есть проблема: простые пластиковые чашки, используемые в большинстве лабораторий, сами по себе переводят эти клетки в ненатурально активное состояние, что затрудняет изучение ранних этапов перехода от нормального к фиброзному состоянию.
Когда лабораторная посуда посылает неверный сигнал
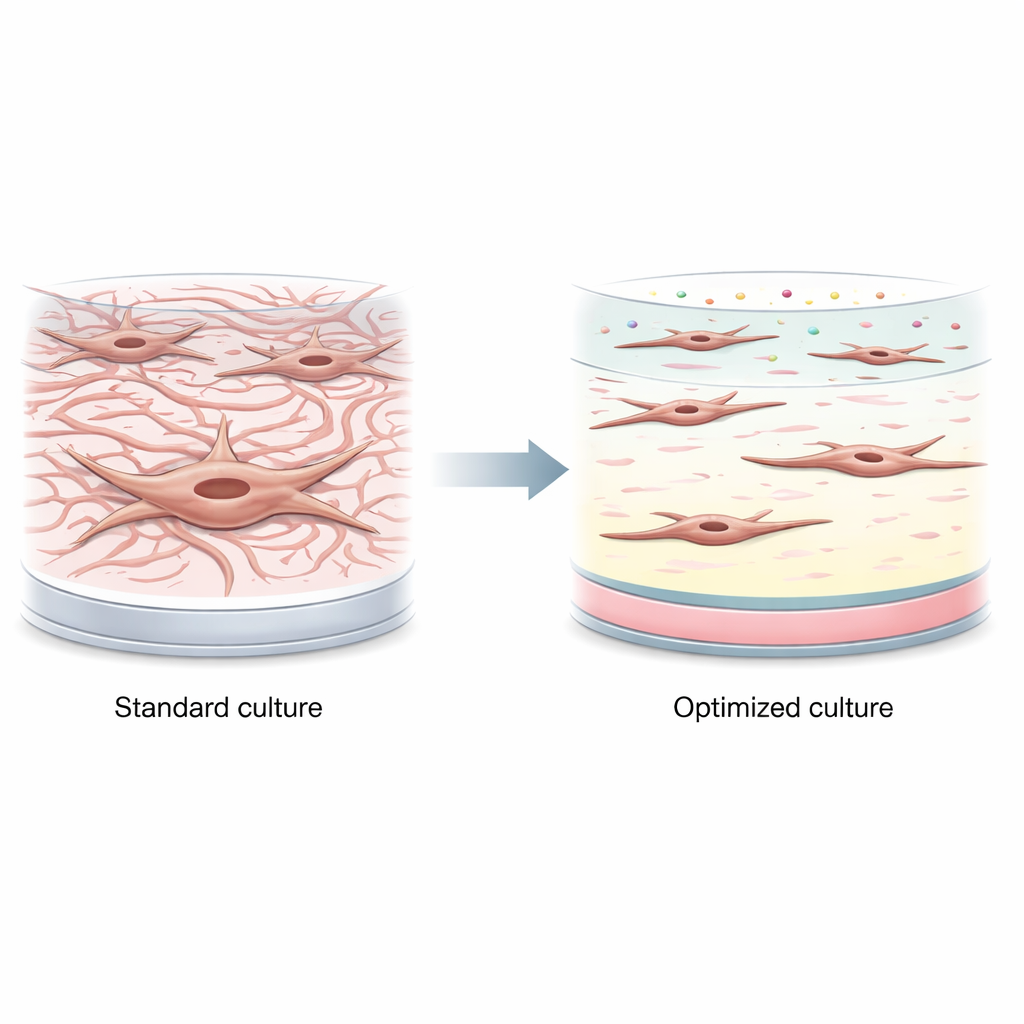
Авторы сначала показали, как быстро кишечные фибробласты активируются на стандартном пластике для культуры тканей. Уже через 24 часа как установленная клеточная линия, так и первичные клетки от доноров обоих полов переходили из спокойного состояния в активную, мышеподобную форму. Они вырабатывали высокие уровни белков, связанных с сокращением и формированием рубцов, таких как α-гладкомышечный актин и белок активации фибробластов, даже без добавления воспалительных стимулов. Это означает, что многие существующие лабораторные модели могут стартовать из состояния, которое уже похоже на позднюю стадию болезни, а не на ранние, обратимые изменения.
Испытание отдельных ингредиентов недостаточно
Чтобы успокоить клетки, команда исследовала компоненты их естественного окружения в кишечнике, включая ключевые белки матрикса (коллаген I и III и ламинин) и растворимые факторы (витамин D и базальный фактора роста фибробластов, FGF). Их пробовали по отдельности — как покрытия поверхности или как добавки в среду. Некоторые условия снижали маркеры активации: например, умеренные дозы витамина D значительно уменьшали один из основных маркеров фиброза, а определенная плотность покрытий давала слабый эффект. Но эти преимущества сопровождались проблемами, такими как снижение выживаемости клеток при более высоких дозах витамина D, и в целом одиночные манипуляции не обеспечивали надежного поддержания низкой активности фибробластов.
Позволив статистике исследовать пространство возможностей
Вместо изменения одного параметра за раз исследователи применили формальный подход «планирования экспериментов», чтобы эффективно просеять множество комбинаций. Они варьировали пять входных факторов — три белка матрикса плюс витамин D и FGF — в широком диапазоне доз, получив 42 тщательно подобранных условия культивирования. Для каждого условия измеряли четыре показателя, связанные с формированием рубца: ключевой маркер активации, секреция основного матричного белка (фибронектин), рост клеток и выживаемость. Статистические модели затем выявили, какие факторы и какие их сочетания оказывают наибольшее влияние. Витамин D проявил себя как мощный, но чувствительный к дозе фактор, влияющий на все показатели, тогда как FGF в целом снижал активацию и поддерживал рост и выживаемость клеток. Коллаген I, коллаген III и ламинин определяли, как эти растворимые сигналы интерпретируются клетками: некоторые комбинации значительно подавляли активацию сильнее, чем любой отдельный фактор.
Создание рецепта для спокойных, но здоровых фибробластов
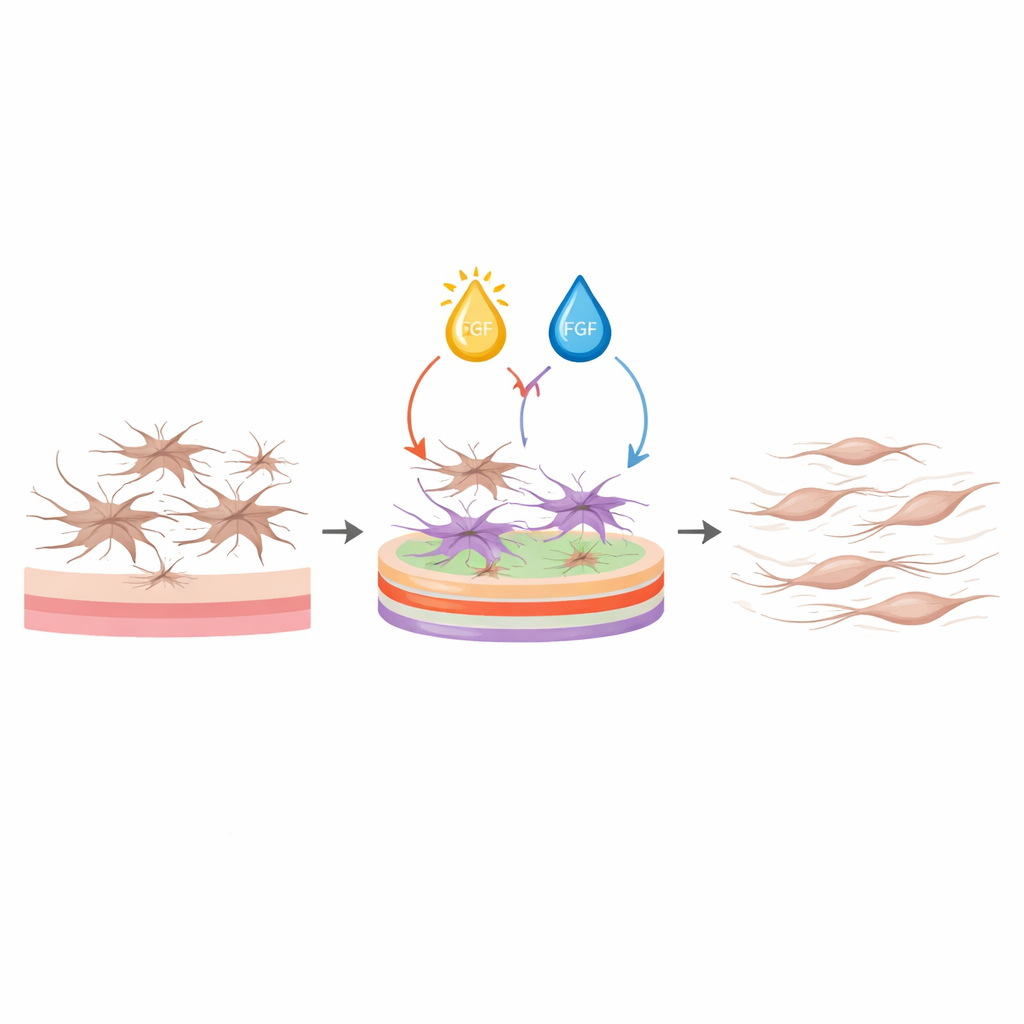
Используя эти модели, команда попросила программное обеспечение найти условия, которые одновременно снизят маркеры активации и продукцию матрикса при сохранении жизнеспособности клеток, без требования низкой пролиферации. Лучший рецепт сочетал высокую плотность коллагена I, низкую плотность коллагена III и высокий уровень ламинина на поверхности выращивания, вместе со средними концентрациями витамина D и высоким уровнем FGF в среде. При этом протоколе фибробласты оставались тонкими и веретенообразными вместо распластанных или звездообразных, экспрессировали значительно более низкие уровни генов и белков, связанных с сокращением и фиброзом, и секретировали гораздо меньше коллагена и фибронектина. Одновременно их жизнеспособность оставалась такой же или лучше, чем у клеток на обычном пластике. Важно, что эти эффекты наблюдались как в модельной клеточной линии, так и в первичных фибробластах от доноров обоих полов, что показывает устойчивость протокола.
Что это значит для будущих исследований кишечного фиброза
Тщательно настроив «окружение» кишечных фибробластов — и поверхность, к которой они прикрепляются, и факторы, которые их омывают — это исследование предлагает простой протокол, позволяющий поддерживать эти клетки в неактивном, но здоровом состоянии с использованием стандартных лабораторных материалов. Для исследователей это обеспечивает чистую исходную платформу, на которую можно добавлять специфические воспалительные или механические сигналы и наблюдать, как начинается фиброз, вместо работы с клетками, которые уже похожи на рубцовые. В более широком смысле работа демонстрирует, как статистическое планирование экспериментов может выявлять тонкие, неинтуитивные комбинации ингредиентов, которые укрощают сложные клеточные поведения, прокладывая путь к лучшим моделям формирования рубцов и, в конечном счете, к более целевым стратегиям предотвращения или обращения кишечного фиброза.
Цитирование: Mohammadalizadeh, Z., Sudi, S., Basto Moreno, D.A. et al. Developing a protocol to counteract spontaneous in vitro activation of intestinal fibroblasts using design of experiments. npj Biomed. Innov. 3, 25 (2026). https://doi.org/10.1038/s44385-026-00079-5
Ключевые слова: кишечный фиброз, активация фибробластов, протокол культивирования клеток, витамин D и FGF, планирование экспериментов