Clear Sky Science · ru
Вывод аномалий сигнальных путей по гистопатологическим изображениям с помощью логически ограниченного гетерогенного графа знаний «гены–пути»
Видеть скрытые клеточные сигналы на слайдах рака
Когда врачи рассматривают рак под микроскопом, они в основном видят формы и цвета, а не сложные молекулярные «разговоры», происходящие внутри клеток. Тем не менее эти невидимые сигнальные «диалоги» между генами и путями часто определяют, как опухоль растет и как она может отреагировать на лечение. В этом исследовании представлена новая система искусственного интеллекта, которая анализирует обычные патологические изображения и выводит, какие маршруты клеточной коммуникации, или пути, нарушаются — предлагая способ заглянуть в молекулярное поведение без дополнительных лабораторных тестов.
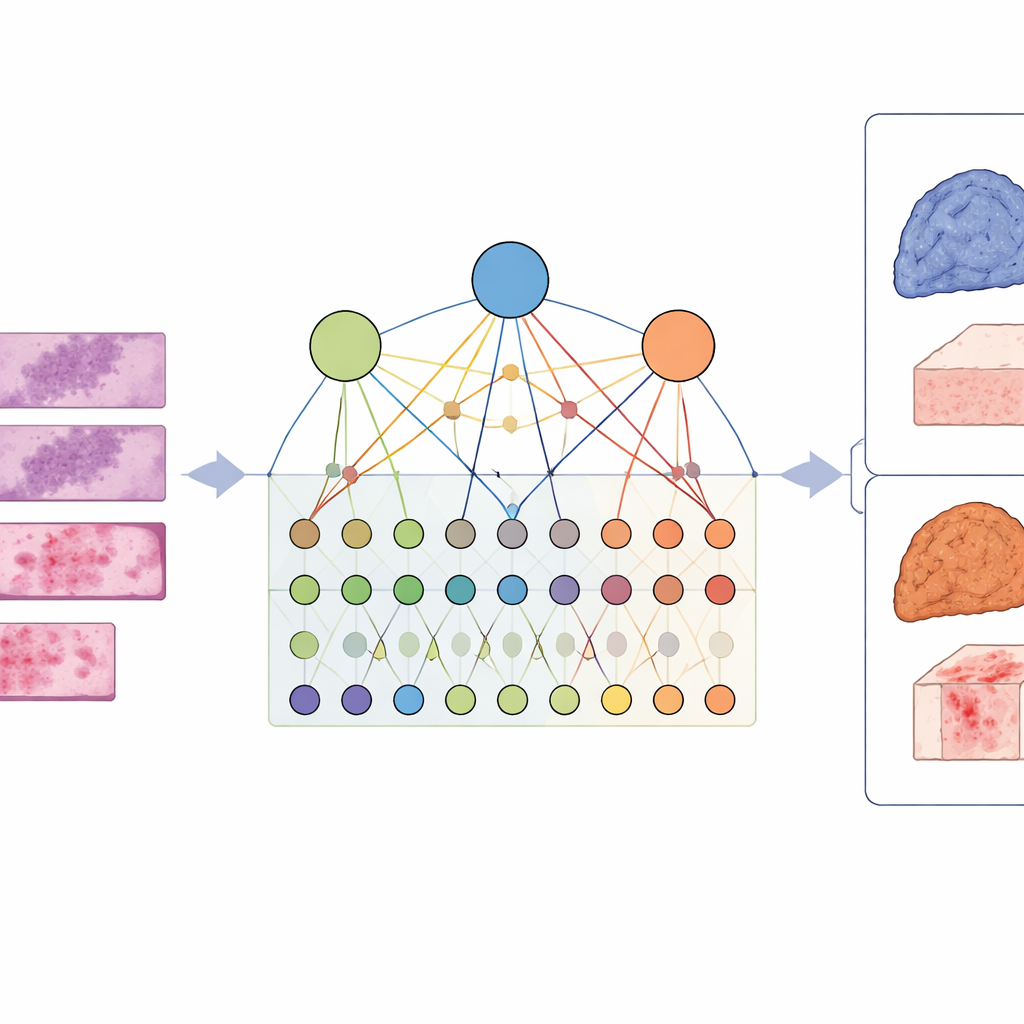
От подсказок одного гена к более широкой картине
Традиционные подходы пытаются предсказать статус отдельных генов по изображениям тканей: мутирован тот или иной ген или нет? Это полезно, но рак редко зависит от одного дефектного гена. Группы генов работают совместно, нарушая целые сигнальные пути, контролирующие рост, выживание и иммунитет. Авторы утверждают, что концентрация на отдельных генах упускает эту кооперативную динамику и может не объяснить, почему опухоли выглядят и ведут себя так, как они это делают на микроскопических снимках.
Построение карты между изображениями, генами и путями
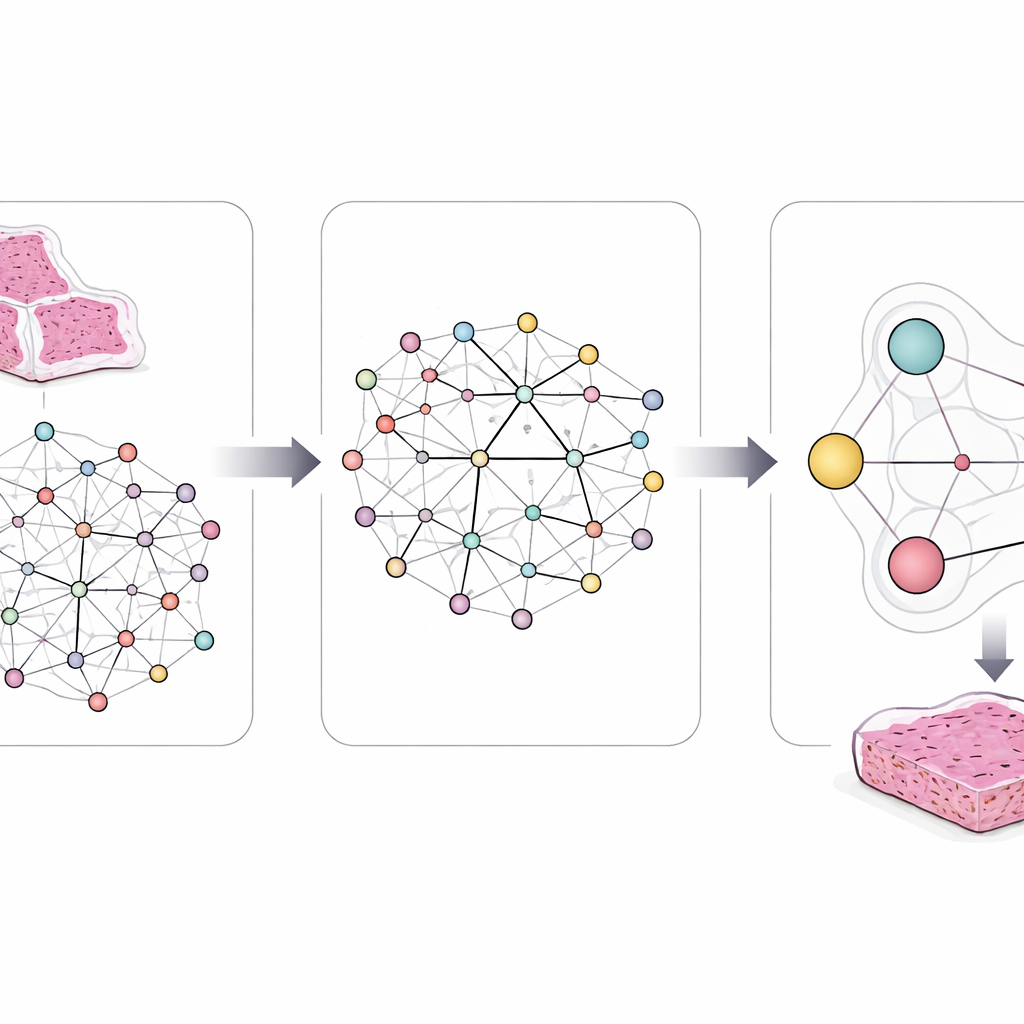
Чтобы уловить эту сложность, исследователи разработали фреймворк LCG-HGNN, который связывает три уровня информации. Сначала они разбивают каждое целое гистологическое стекло с аденокарциномой легкого на множество мелких фрагментов и представляют эти фрагменты в виде графа, где соседние или сходные по внешнему виду области соединены между собой. Затем они связывают маркеры генов с сигнальными путями, используя общепризнанные биологические базы данных, строя второй граф, который кодирует, какие гены принадлежат каким путям. Наконец, модель ИИ пропускает информацию через этот объединенный граф, так что шаблоны на изображениях, гены и пути влияют друг на друга, а не рассматриваются по отдельности.
Обучение системы с учётом известной биологии
Ключевое новшество в том, что модели не разрешено учиться свободно без направляющих ограничений. Авторы встраивают чёткие, похожие на правила утверждения, выведённые из десятилетий исследований рака. Например, некоторые мутации почти никогда не встречаются вместе в одной опухоли, а одни пути находятся выше или ниже других по цепочке сигналов. Они кодируют такие правила как логические ограничения, которые мягко направляют внутренние связи и предсказания ИИ. Если модель предлагает комбинацию изменений генов и путей, противоречащую известной биологии или сходству между слайдами пациентов, эти правила подталкивают её к более реалистичным альтернативам.
Проверка точности по сравнению с существующими методами
Команда оценивала свою систему на более чем 1600 слайдах рака легкого, связанных с генетическими данными. Они сравнили её со стандартными моделями глубокого обучения, ориентированными на отдельные гены, и с более продвинутыми методами, которые обрабатывают множество генов одновременно, но игнорируют структуру путей. По нескольким важным путям, включая те, что вовлечены в сигналы роста клеток и опорную матрицу ткани, новая модель точнее предсказывала изменения в группах генов и аномалии путей. Она также выделяла фрагменты изображения, чья внешность близко соответствовала реальным клиническим примерам, известным как ассоциированные с конкретными мутациями, что указывает на то, что модель фокусируется на значимых микроскопических паттернах, а не на случайных особенностях изображения.
Почему это важно для пациентов
Для неспециалиста главный итог в том, что этот подход превращает обычный патологический слайд в богатый источник молекулярной информации. Вместо того чтобы назначать отдельные, часто дорогие генетические тесты для каждой потенциальной мишени, врачи в конечном итоге смогут использовать такие модели для скрининга нарушенных путей прямо по уже имеющимся изображениям. Хотя методу ещё необходима более масштабная проверка в реальных условиях и он пока не заменяет геномное тестирование, он указывает на будущее, в котором вид в микроскопе становится окном во внутреннюю схему опухоли — помогая направлять более точное и биологически обоснованное лечение рака.
Цитирование: Yu, Y., Shi, W., Chen, X. et al. Inferring signaling pathway abnormalities from histopathological images via logic-constrained gene-pathway heterogeneous knowledge graph. npj Biomed. Innov. 3, 23 (2026). https://doi.org/10.1038/s44385-026-00078-6
Ключевые слова: раковые пути, ИИ для гистопатологии, графовые нейронные сети, аденокарцинома легкого, цифровая патология