Clear Sky Science · ru
Использование in vitro со-культур для разработки бактериальной инженерии в лечении солидных опухолей
Почему бактерии в онкологии могут быть важны для вас
Такие методы лечения рака, как операция, химио- и радиотерапия, спасают жизни, но часто сопровождаются тяжёлыми побочными эффектами и нередки случаи неэффективности лечения. Оригинальная идея — привлечь живые бактерии как точные инструменты, которые могут находить и атаковать солидные опухоли изнутри. В этой статье объясняется, как учёные создают лабораторные тестовые системы — где человеческие клетки и бактерии растут вместе — чтобы разработать более безопасные и умные бактериальные терапии до их применения у пациентов.
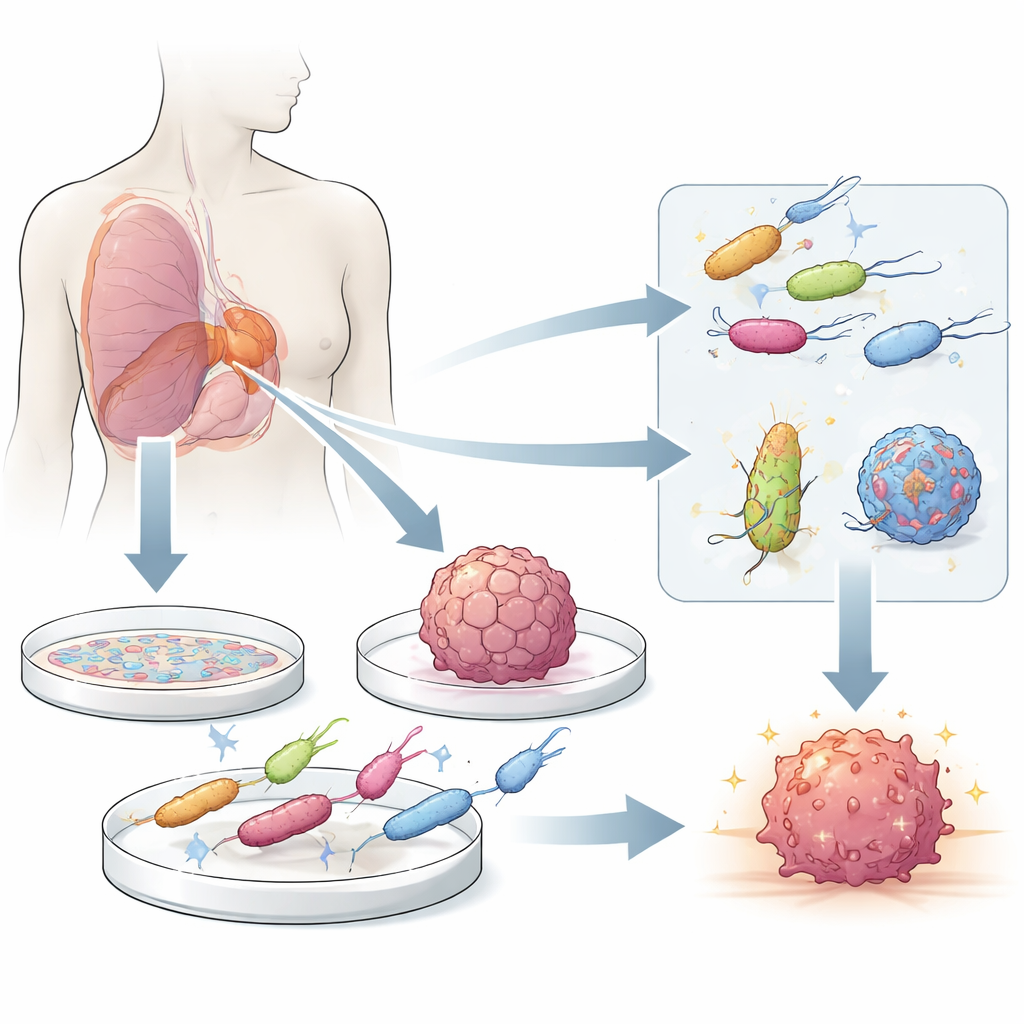
Крошечные помощники, ищущие опухоли
Некоторые бактерии естественно предпочитают суровую, бедную кислородом среду внутри солидных опухолей по сравнению со здоровыми тканями. Проникая через проницаемые сосуды опухоли или «перемещаясь» вместе с иммунными клетками, эти микробы устремляются к мёртвым и умирающим клеткам в центре опухоли, где они могут размножаться и иногда вызывать гибель раковых клеток и локальные иммунные реакции. Современная генная инженерия превращает эти природные штаммы с «тропизмом к опухоли» в живые носители, способные доставлять лекарства, иммунные стимуляторы или другие полезные молекулы прямо туда, где они наиболее нужны, а работы по ослаблению их патогенных свойств повышают безопасность.
Создание реалистичных лабораторных мини-опухолей
Чтобы понять и улучшить эти «живые лекарства», учёным нужны модельные системы, максимально воспроизводящие процессы в человеческом организме. Простые плоские слои клеток легко выращивать и они полезны для быстрой скрининговой работы, но в них отсутствует сложная структура и градиенты кислорода, характерные для настоящих опухолей. Трехмерные модели, такие как сфероиды из линий раковых клеток и органоиды, выращенные из тканей пациента, лучше воспроизводят ключевые черты — живую наружную оболочку, спокойную внутреннюю зону и мертвый центр. Когда бактерии смешивают непосредственно с такими мини-опухолями, исследователи могут наблюдать, как они проникают, где накапливаются и насколько эффективно работают запрограммированные лекарственные схемы в условиях, напоминающих опухоль пациента.
Разделение клеток для изучения сигналов
Другие конструкции со-культуры уделяют меньше внимания физическому контакту и больше — невидимым химическим обменам между бактериями и человеческими клетками. В системах с трансуэллами пористая мембрана разделяет две камеры так, что мелкие молекулы проходят через неё, а клетки остаются по своим сторонам. Это позволяет, например, проверить, как штамм бактерий превратил безвредное соединение в газ с опухолеубивающим эффектом, который диффундировал к близлежащим раковым клеткам. Микрофлюидные чипы — миниатюрные устройства с каналами и отделениями — добавляют ещё один уровень реализма. Они могут управлять потоком жидкости, уровнями кислорода и временными параметрами, позволяя инженерным бактериям расти, синхронно лизироваться и многократно омывать раковые клетки терапевтическими молекулами, точно отслеживая ответы обеих сторон с течением времени.
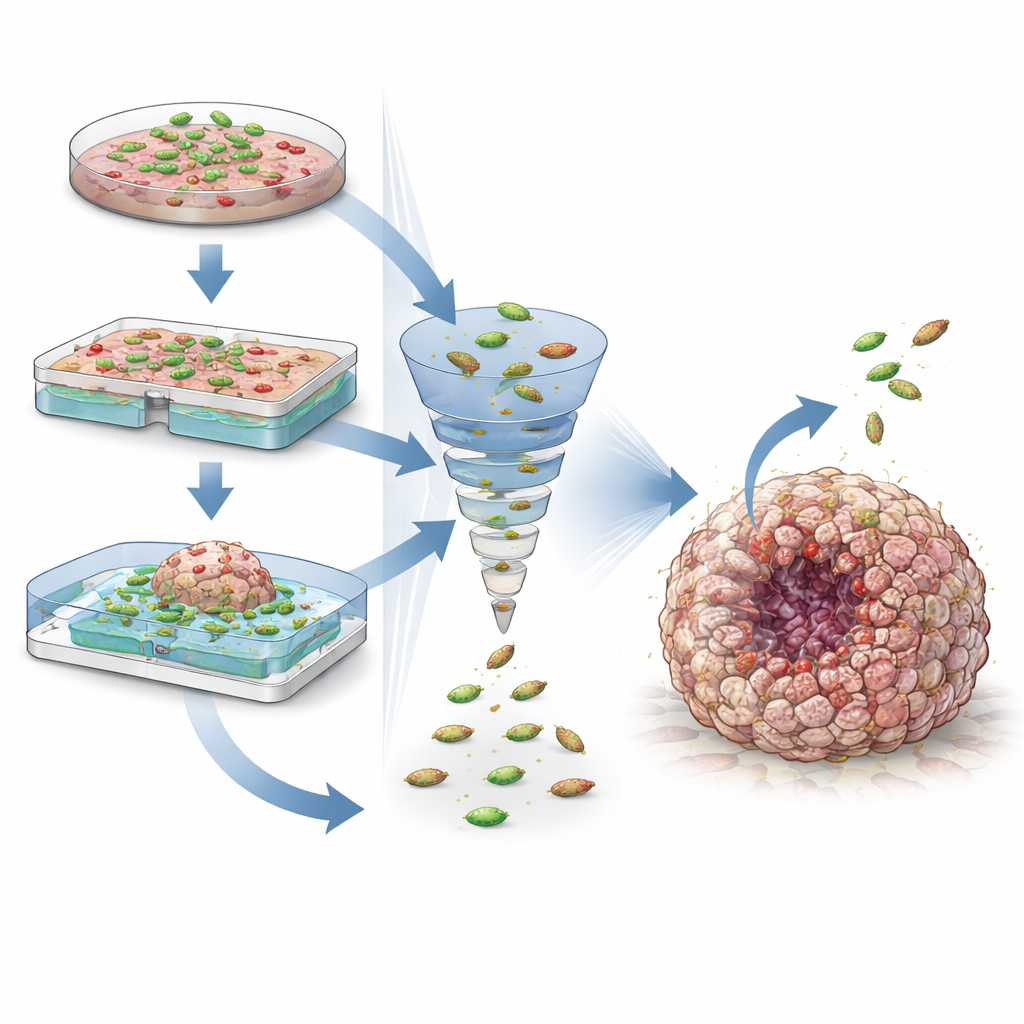
Заглядывая в экосистему опухоли
Модели со-культуры также используют для изучения взаимодействий бактерий с более широкой экосистемой опухоли. Органоиды, полученные от отдельных пациентов, могут сохранять многие генетические особенности и ответы на лекарства исходной опухоли, что открывает возможности для персонализированного тестирования бактериальных терапий. Добавление иммунных клеток в такие культуры показывает, как бактерии могут усиливать или подавлять антираковый иммунитет и как они могут сочетаться с препаратами‑ингибиторами контрольных точек. В то же время эти модели выявляют проблемы безопасности, например бактериальные токсины, повреждающие ДНК и потенциально способные способствовать возникновению рака. Путём настройки условий культивирования, уровней кислорода и методов измерения — от живой визуализации до секвенирования ДНК — исследователи могут системно исследовать эти преимущества и риски.
От лабораторного стола до палаты больного
Несмотря на многообещающие результаты на животных моделях, лишь немногие бактериальные терапии рака показали очевидную пользу в клинических испытаниях на людях. Авторы утверждают, что более разумное использование систем со-культуры может сократить этот разрыв. Лучше учитывая межпациентные различия, сложность опухолей и предшествующее лечение, эти модели способны выявить наиболее перспективные инженерные штаммы, способы их сочетания с существующими препаратами и точки возможного провала. Они также подчёркивают необходимость общих стандартов, чтобы лаборатории по всему миру могли сравнивать результаты, а регуляторы — с большей уверенностью оценивать безопасность и эффективность. Проще говоря, тщательно спроектированные лабораторные мини-опухоли, выращенные бок‑о‑бок с бактериями, предлагают мощный инструмент для оттачивания этих «умных микробов», повышая шансы на то, что будущие пациенты получат бактериальные терапии, одновременно более безопасные и более эффективные.
Цитирование: Foschini, S., Wright, J.A., Woods, S.L. et al. Use of in vitro co-culture models to inform bacterial engineering for the treatment of solid tumours. npj Biomed. Innov. 3, 21 (2026). https://doi.org/10.1038/s44385-026-00075-9
Ключевые слова: бактериальная терапия рака, опухолевые органоиды, модели со-культуры, синтетическая биология, микроокружение опухоли