Clear Sky Science · ru
3D биофабрикованные in vitro модели как новые методологии подхода для альтернатив животным
Переосмысление методов тестирования новых лекарств
На протяжении почти столетия большинство новых препаратов тестировали на животных до начала клинических испытаний на людях. Однако более 9 из 10 лекарственных кандидатов, которые кажутся безопасными в опытах на животных, всё равно терпят неудачу у людей. В этой статье рассматривается, как новое поколение 3D «биопечатных» человеческих тканей может изменить эту ситуацию — предлагая более точные и гуманные способы прогнозирования реакции организма на лекарства и потенциально ускоряя доставку безопасных терапий пациентам.

От лабораторных животных к тестированию, ориентированному на человека
Недавнее законодательство США, известное как FDA Modernization Act 2.0, убрало автоматическое требование тестировать каждый новый препарат на животных. Вместо этого регуляторы теперь могут принимать «Новые методики подхода» — тестовые системы, ориентированные на человека и разработанные для более точного прогнозирования реакции реальных пациентов. Среди таких подходов выделяется 3D биопечать. Она использует специализированные принтеры для размещения живых человеческих клеток и мягких гелеобразных материалов в сложных формах, имитирующих настоящие ткани и мини-органы. Процесс часто начинается с медицинских изображений, таких как КТ или МРТ, которые дают чертёж. Учёные затем подбирают подходящие биоматериалы, смешивают нужные типы клеток для получения печатаемой «биоинктони», и печатают послойные или объемные конструкции, которые созревают в функциональные модели тканей в биореакторах.
Как 3D биопечать строит живые ткани
Биопечать — это не единая технология, а семейство методов. Принтеры типа «струйной печати» распыляют крошечные капли жидкости с клетками для создания тонких слоёв с высокой детализацией, что делает их полезными для миниатюрных тканей, таких как кожные пластыри или барьеры лёгких. Экструзионные принтеры выдавливают непрерывные нити более густых биоинков, которые могут содержать множество клеток и поддерживающих волокон, позволяя строить более крупные и прочные структуры, например клапаны сердца, модели опухолей печени или сосудистые сети. Более новый класс методов, называемый фотополимеризацией в ванне, направляет узорчатый свет в жидкость, чтобы затвердить сложные формы без проталкивания клеток через сопла. Варианты этого подхода умеют формировать микронные детали, печатать целый небольшой орган за секунды или даже формировать ткани внутри прозрачной ванны, сохраняя клетки живыми.
Замена и усовершенствование тестов лекарств
Эти напечатанные ткани уже применяют для переосмысления цепочки разработки лекарств. На ранних этапах открытия пациент- или болезнь-специфические конструкции — например биопечатные модели опухолей — позволяют исследователям проверять множество кандидатов в реалистичной 3D-среде, которая лучше отражает человеческое заболевание, чем плоские слои клеток в чашке Петри. На доклиническом этапе напечатанные кожа, лёгкие и печень показывают большую точность, чем животные, при выявлении токсичности или побочных эффектов, специфичных для человека. Некоторые исследования идут дальше, печатая «клинические испытания на чипе», где ткани из клеток разных доноров подвергают воздействию лекарства параллельно, выявляя, кто может получить пользу, а кто — вред. Регуляторы теперь поощряют компании предоставлять данные из этих моделей наряду с животными исследованиями, формируя доказательную базу для более широкого принятия.
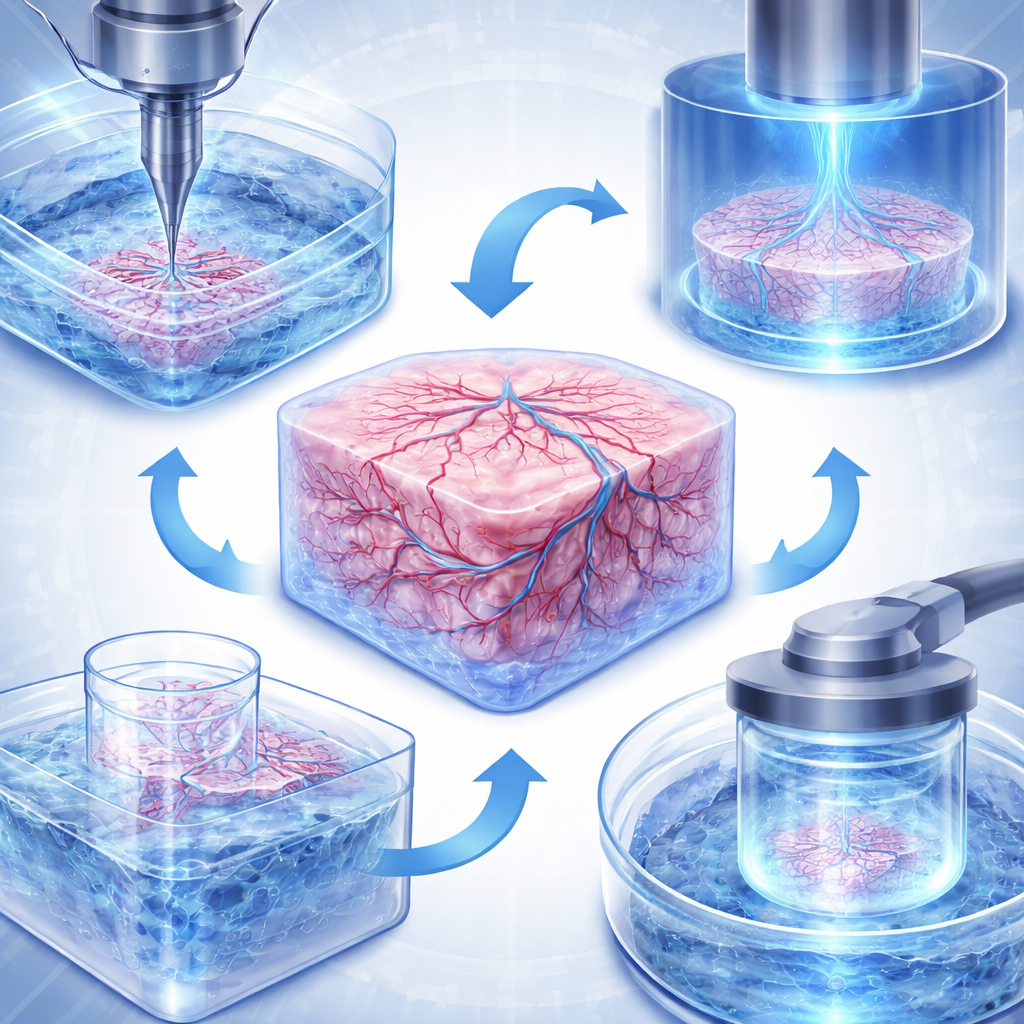
Инжиниринг органов без тела
Несмотря на быстрый прогресс, остаётся несколько препятствий, прежде чем биопечатные ткани смогут регулярно заменять животные тесты. Одной из основных проблем является сосудистое снабжение: настоящие органы содержат сети сосудов от крупных артерий до тончайших капилляров, тогда как напечатанные конструкции должны преодолеть естественное ограничение расстояния, на которое кислород и питательные вещества могут диффундировать. Исследователи решают это новыми стратегиями печати, создающими разветвлённые каналы; опорными ваннами, которые удерживают мягкие ткани на месте во время формирования мелких сосудов; и сверхбыстрыми объемными принтерами, которые создают плотные клеточные структуры прежде, чем клетки начнут испытывать стресс. Ещё одна проблема — реалистичность: живые ткани состоят из множества типов клеток, окружённых сложными химическими сигналами и часто под влиянием микробиома и отдалённых органов. Продвинутые модели теперь комбинируют несколько популяций клеток, контролируемые градиенты кислорода и pH, и даже связанные «мультиорганные» системы, которые соединяют кишечник, печень, иммунную систему и ткани мозга потокящей средой для имитации реакций всего организма.
Гуманное и предсказуемое будущее разработки лекарств
В совокупности эти достижения указывают на будущее, в котором высокоточные модели тканей на основе человека станут центральными в оценке лекарств. Статья делает вывод о том, что 3D биопечать превращается из нишевой лабораторной техники в ключевой инструмент для создания стандартизированных, готовых к регуляторному применению тестовых систем. Чтобы полностью реализовать этот потенциал, учёным и регуляторам нужно согласовать, где и как должны применяться эти модели, доказать их надёжность в предсказании исходов у людей и решить оставшиеся технические задачи, такие как создание стабильной васкуляризации и анатомически сложных органов. Если это удастся, такой сдвиг может сократить зависимость от тестирования на животных, уменьшить дорогостоящие провалы на поздних этапах разработки и доставить более безопасные и эффективные терапии, лучше отражая биологию, которая имеет наибольшее значение: нашу собственную.
Цитирование: Hua, W., Gaharwar, A.K. 3D biofabricated in vitro models as new approach methodologies for animal alternatives. npj Biomed. Innov. 3, 20 (2026). https://doi.org/10.1038/s44385-026-00073-x
Ключевые слова: 3D биопечать, альтернативы тестированию на животных, разработка лекарств, модель тканей, объемная биопечать