Clear Sky Science · ru
Инженерная модификация макрофагов для противораковой иммунотерапии: новые инсайты и терапевтический потенциал
Преобразование «уборочной бригады» организма в борцов с раком
Наш организм насыщен макрофагами — бродящими «уборщиками», которые поглощают микробы и погибшие клетки. В этом обзорном материале рассматривается, как учёные учатся перенаправлять эти клетки против рака. Поскольку макрофаги многочисленны внутри опухолей, в том числе в тех, что устойчивы к современным иммунотерапиям, понимание и инженерная трансформация макрофагов могут открыть новые опции для пациентов с трудноизлечимыми опухолями.
Много лиц одного типа клеток
Макрофаги — не фиксированный тип клеток; они способны менять облик. Они могут поступать из кровотока или уже обитать в тканях, и, поселившись, реагировать на местные сигналы. В опухолях ассоциированные с ними макрофаги могут либо помогать уничтожать раковые клетки, либо, что парадоксально, способствовать росту и распространению опухоли. Раньше исследователи пытались уместить их в две категории — «M1» (режим атаки) и «M2» (режим восстановления или поддержки). Новые генетические и пространственные методы картирования показывают гораздо более богатый спектр состояний, с многочисленными подгруппами и поведением, варьирующим в зависимости от опухоли и локализации. Даже клетки, ранее считавшиеся однозначно «про-опухолевыми», в некоторых контекстах могут мобилизовать Т-клетки и поддерживать противораковый иммунитет.
Ощущая окружение и пожирая раковые клетки
Макрофаги не только воспринимают химические сигналы; они также чувствуют физический мир вокруг себя. Проползая через плотную сеть белков в опухоли, протискиваясь между клетками и испытывая жидкостные силы, они ощущают жёсткость и деформацию через специализированные рецепторы, такие как Piezo1. Эти механические сигналы в сочетании с классическими иммуными сигналами способны смещать макрофагов в более воспалительные или более успокаивающие состояния. Функционально макрофаги могут поглощать раковые клетки, затем расщеплять их и демонстрировать фрагменты (антигены) Т-клеткам, создавая мост между врождённым и адаптивным иммунитетом. Раковые клетки защищаются, посылая «не ешь меня» сигналы, наиболее известный из которых — молекула поверхности CD47, связывающаяся с тормозным механизмом макрофагов. Препараты, блокирующие это взаимодействие, находятся во многих клинических исследованиях, усиливая очистку раковых клеток, но требуя тонкой настройки, чтобы не навредить здоровым клеткам.
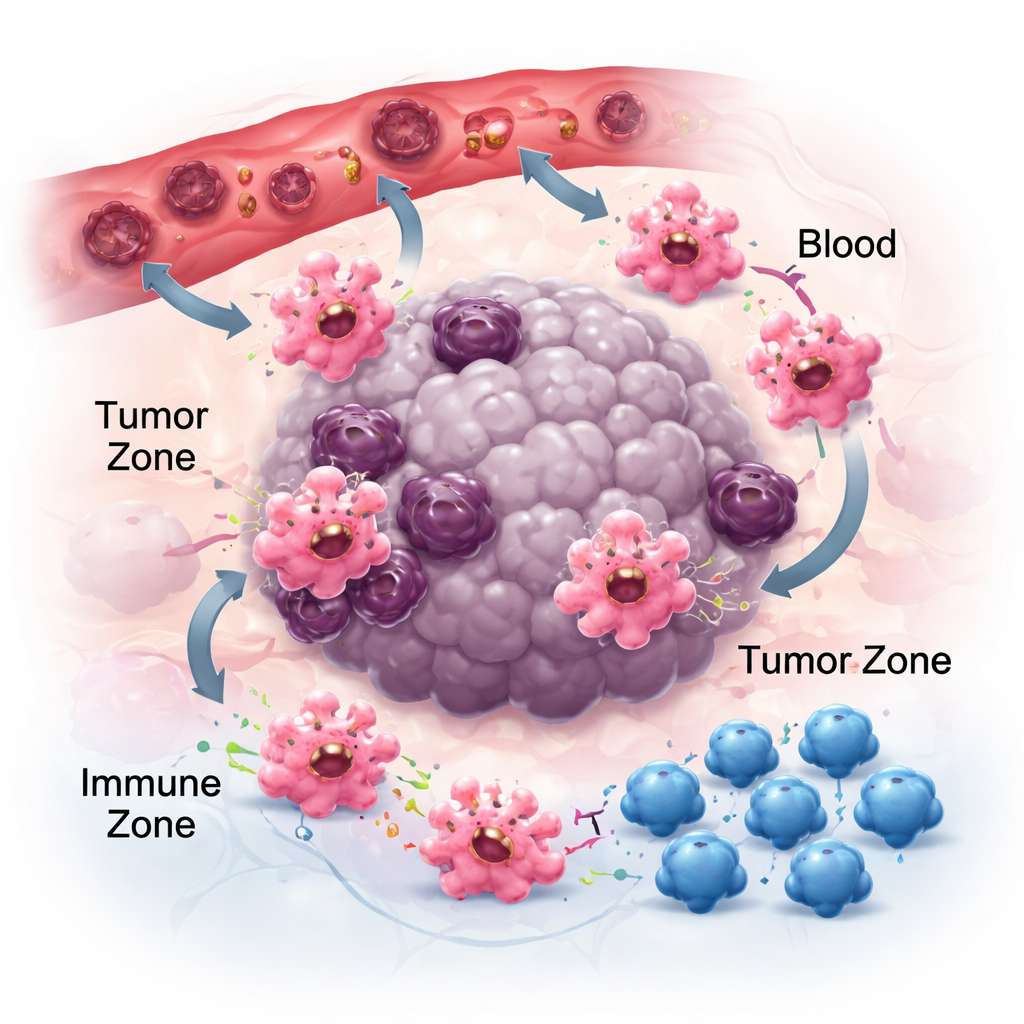
Движение, прикрепление и общение в опухолевом окружении
Чтобы иметь значение в лечении рака, макрофаги должны сначала достичь опухолей, а затем разместиться в подходящих нишах. Они следуют химическим путям — хемокинам и факторам роста — выпускаемым раковыми и окружающими клетками. Пары вроде CCR2–CCL2 помогают привлекать их в опухоли, и препараты, блокирующие эти сигналы, могут сокращать накопление макрофагов, хотя не полностью, что указывает на роль других привлекающих факторов, таких как CSF-1 и VEGF. Оказавшись на месте, то, как макрофаги прикрепляются к местному матриксу, также формирует их поведение. Их рецепторы адгезии, интегрины, не только служат «клеем»; они усиливают воспалительные сигналы и могут подтолкнуть клетки к более антиопухолевым состояниям. Одновременно макрофаги выделяют крошечные пакеты — внеклеточные везикулы, несущие РНК и белки — к соседним клеткам. В зависимости от типа опухоли эти везикулы могут либо притуплять иммунитет и способствовать распространению, либо укреплять противоопухолевые ответы, что подчёркивает контекстно-зависимую природу коммуникации макрофагов.
Перепрограммирование макрофагов генами и материалами
Поскольку макрофаги естественно лучше проникают в солидные опухоли, чем многие Т-клетки, исследователи сейчас перепроектируют их как «живые лекарства». Одна генетическая стратегия заимствует подход из терапии Т-клеток с химерными антигенными рецепторами (CAR): добавление синтетического рецептора для создания CAR-макрофагов (CAR-M). Эти дизайнерские клетки распознают маркёры опухоли, более эффективно поглощают раковые клетки, разрушают окружающий матрикс, выделяют провоспалительные сигналы и активируют Т-клетки, представляя опухолевые антигены. Ранние клинические испытания на людях CAR‑М, направленных против HER2, демонстрируют обнадеживающую безопасность и биологическую активность, хотя потребуется больше работы, чтобы доказать выраженные и длительные преимущества. Параллельно негенетические подходы используют частицы и «ранец‑пласты» из липидов или полимеров. Макрофаги могут поглощать загруженные лекарством наночастицы и переносить их глубоко в опухоль как троянские кони, или носить прицепленные на поверхности пласты, которые медленно высвобождают иммуномодулирующие сигналы, помогая сохранять противоопухолевую идентичность без перегрузки внутреннего содержимого. Также испытываются везикулы, производимые макрофагами, как естественные безклеточные носители для доставки.
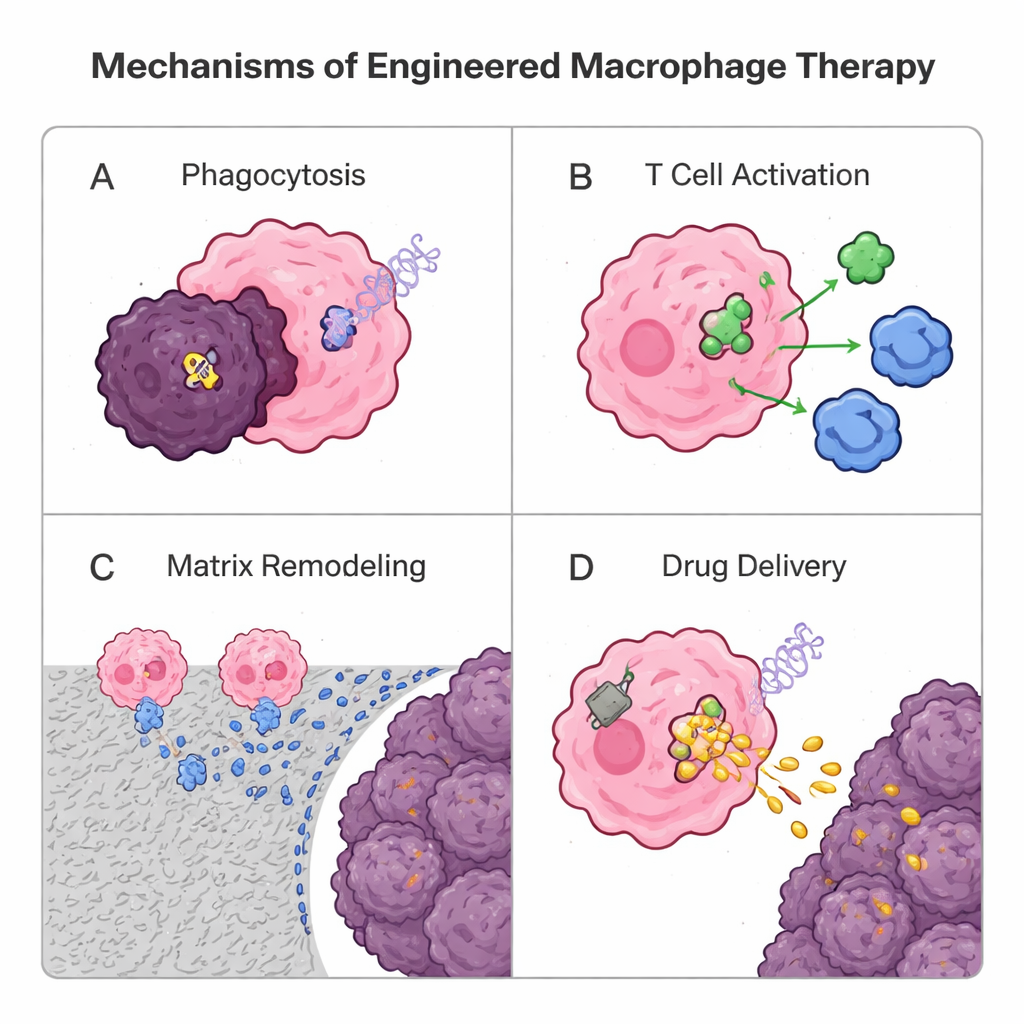
Предстоящие вызовы и поводы для оптимизма
Несмотря на перспективы, терапии на основе макрофагов должны преодолеть практические препятствия. Производство достаточного количества однородных клеток у пациентов требует времени и больших затрат, и после инфузии эти клетки не живут и не размножаются бесконечно. Их присущая пластичность, хотя и полезна с биологической точки зрения, затрудняет удержание их в антиопухолевом режиме в сложной, супрессивной опухолевой микроокружении. Авторы утверждают, что продвинутые биоинженерные модели — 3D-культуры, органоиды и системы «орган-на-чипе», имитирующие реальные механические свойства тканей — будут решающими для понимания и прогнозирования поведения инженерных макрофагов у пациентов. Тем не менее их природная способность проникать в солидные опухоли, поедать раковые клетки и активировать Т-клетки, в сочетании с ранними данными о безопасности, указывает на то, что терапии на основе макрофагов могут стать важным новым оружием, особенно против «холодных» опухолей, которые сегодня сопротивляются большинству иммунотерапий.
Цитирование: Block, A., Liu, X., Zhang, D. et al. Engineering macrophages for cancer immunotherapy: emerging insights and therapeutic potential. npj Biomed. Innov. 3, 18 (2026). https://doi.org/10.1038/s44385-026-00072-y
Ключевые слова: иммунотерапия макрофагами, опухолевая микроокружение, CAR-макрофаги, фагоцитоз, доставка препаратов с помощью наночастиц