Clear Sky Science · ru
Оптимизация индукции воспаления в кишечных эпителиальных органоидах, полученных от недоношенных новорождённых
Почему это важно для уязвимых новорождённых
Дети, рожденные очень преждевременно, сталкиваются с опасным сочетанием: незрелый кишечник и быстро меняющееся сообщество микробов. Вместе они могут вызвать неконтролируемое воспаление, которое повреждает кишечник и приводит к угрожающим жизни состояниям, таким как некротизирующий энтероколит. Поскольку прямые эксперименты на недоношенных младенцах невозможны, учёным нужны реалистичные лабораторные модели их кишечника, чтобы выяснить, что вызывает воспаление и как его остановить. В этом исследовании такая модель была усовершенствована с помощью миниатюрных выращенных в лаборатории кишечных тканей, что даёт более ясный инструмент для изучения, какие микробные сигналы переводят нормальную защиту в вредное воспаление.
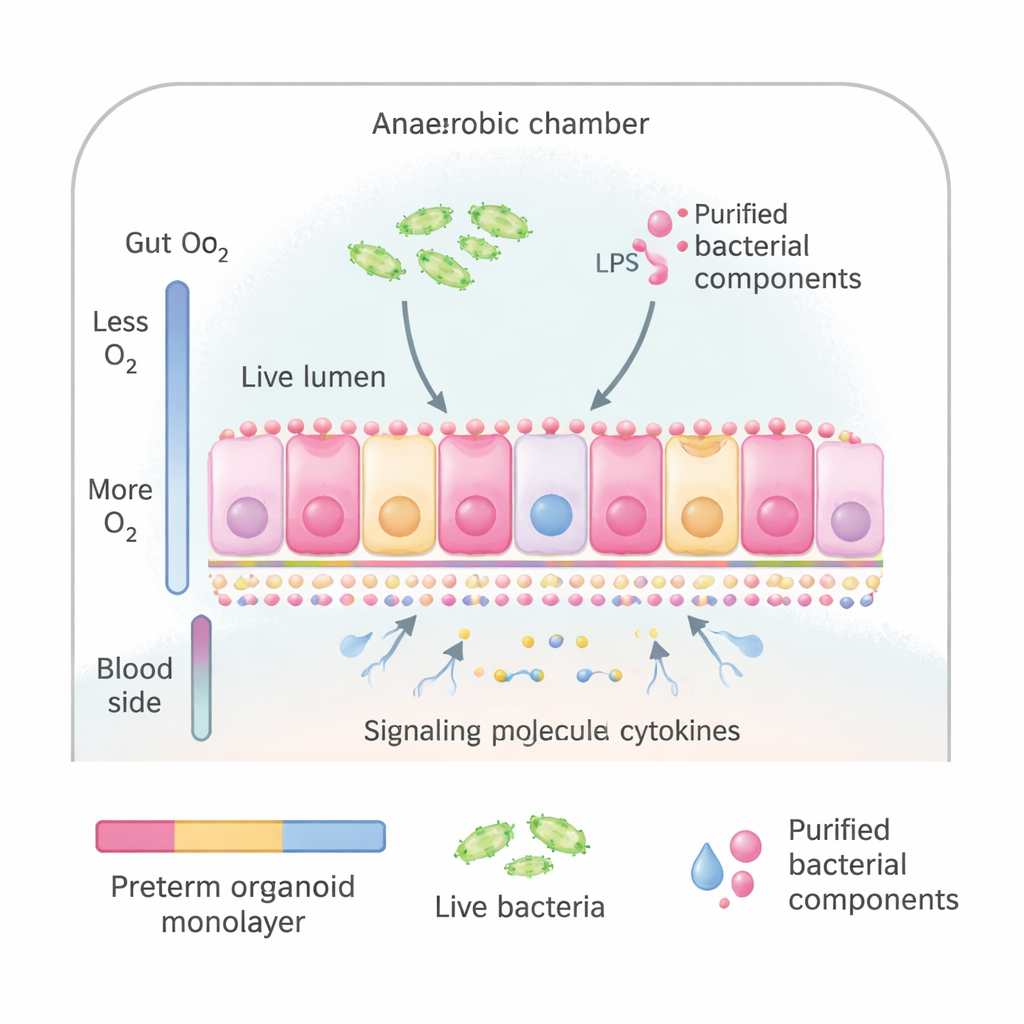
Выращивание кишечника недоношенного в чашке Петри
Исследователи использовали кишечные органоиды — миниатюрные версии слизистой кишечника, выращенные из стволовых клеток, взятых у недоношенных младенцев во время хирургических вмешательств. Эти органоиды можно расправить в тонкий слой клеток, который по внешнему виду и функциям очень похож на внутреннюю поверхность тонкой кишки, включая правильную ориентацию верхней (обращённой к содержимому) и нижней (обращённой к кровотоку) стороны. Команда поместила эти слои в специальную систему культурального выращивания, имитирующую естественный градиент кислорода в кишечнике: низкий уровень кислорода на стороне, обращённой к микробам, и более высокий — на стороне, обращённой к крови. Это позволило подвергнуть «кишечную» поверхность воздействию либо целых бактерий, взятых у недоношенных младенцев, либо очищенных бактериальных компонентов, известных как сигналы для иммунной системы.
Испытание того, что лучше всего вызывает воспалительный отклик
Учёные сравнили несколько способов спровоцировать воспаление: смесь живых бактерий, часто обнаруживаемых у больных недоношенных младенцев; те же бактерии, убитые нагреванием; и два очищенных бактериальных сигнала — липополисахарид (LPS) из клеточных оболочек бактерий и флагеллин из их жгутиков. Они измеряли высвобождение IL‑8, сигнального белка, привлекающего иммунные клетки и служащего общим маркером воспаления, а также использовали масштабный белковый анализ, чтобы увидеть, как изменилась внутренняя биохимия клеток кишечника. Удивительно, но ни живые, ни убитые бактерии в этой системе существенно не повышали уровень IL‑8, даже спустя 24 часа. Напротив, флагеллин и особенно комбинация флагеллина и LPS вызвали заметный подъём IL‑8 уже через три часа, что показывает, что эти очищенные сигналы надёжно включают воспалительное состояние.
Поиск наиболее реалистичной и эффективной схемы
Чтобы лучше соответствовать реальной биологии кишечника, команда затем учла, где естественно действует каждый сигнал. LPS обычно распознаётся на стороне эпителия, обращённой к содержимому кишки, тогда как флагеллин главным образом детектируется со стороны ткани. Используя значительно более низкие, более физиологичные дозы, чем в ранних экспериментах, они наносили LPS на верхнюю (люмен‑ориентированную) сторону и флагеллин на нижнюю (кровоориентированную) сторону слоя органоида. Это простое изменение вызвало сильный и широкий ответ уже через три часа: с обеих сторон ткани выделялись многочисленные воспалительные медиаторы — включая IL‑8, TNF и несколько хемокинов. Одновременно сотни клеточных белков изменили свою концентрацию, указывая на масштабную активацию защитных путей.
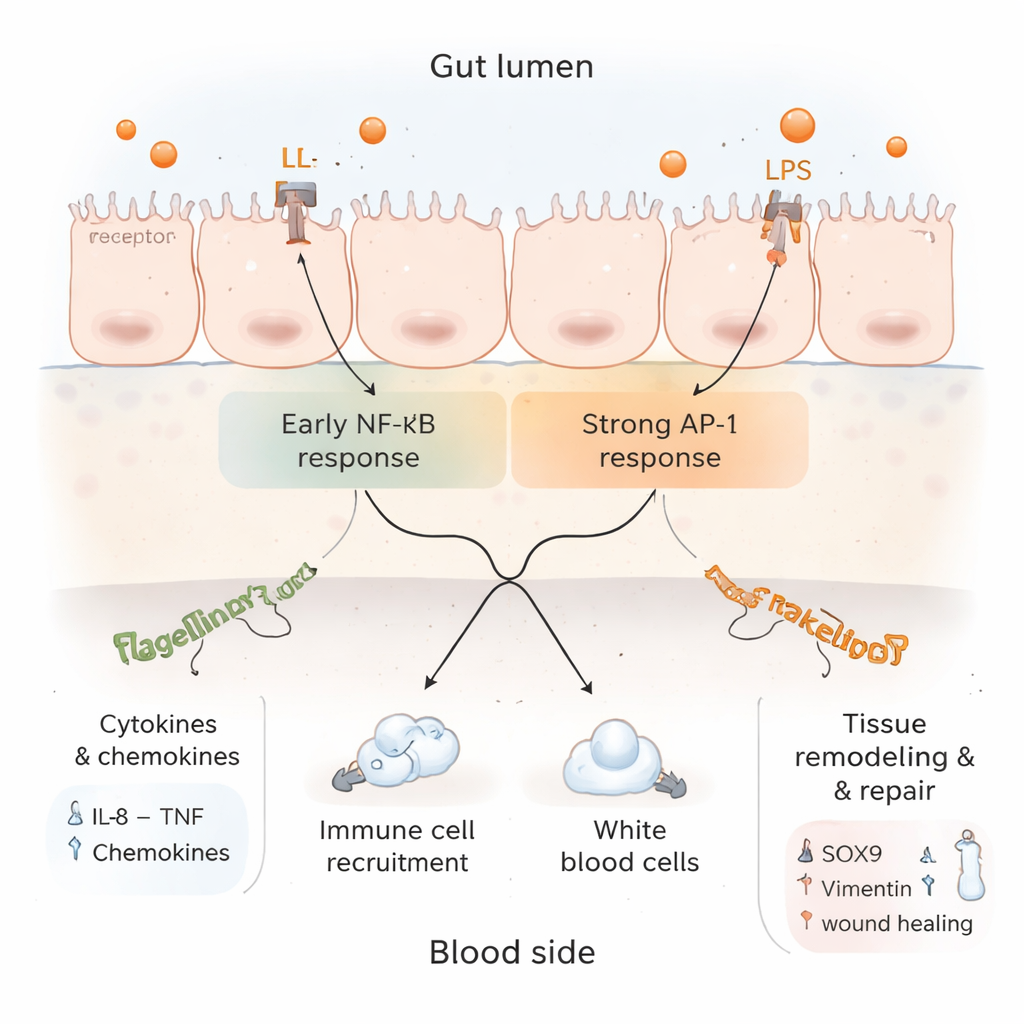
Воспаление, тормозящие механизмы и восстановление в одной модели
Глубокий анализ белковых данных выявил сложную картину. С одной стороны, усиливались маркеры активного воспаления и привлечения иммунных клеток, активировались сигнальные пути, связанные с TNF и IL‑17 — обоими важными для кишечной иммунной защиты. С другой стороны, несколько компонентов классического пути NF‑κB, который управляет многими провоспалительными генами, оказались понижены, тогда как альтернативный путь с участием AP‑1 оставался активным. Это говорит о том, что после первоначальной тревоги ткань начинает включать механизмы «торможения», чтобы предотвратить неконтролируемое повреждение. Одновременно увеличивались белки, связанные с регенерацией тканей, перестройкой структуры и контролируемой гибелью клеток, что намекает, что слизистая не только воспалена, но и пытается перестроиться и зажить.
Что это значит для будущих терапий
Систематически сравнив разные микробные стимулы, дозировки, положения введения и времена воздействия, авторы приходят к выводу, что трёхчасовое экспонирование низкой дозой LPS со стороны люмена в сочетании с флагеллином со стороны, обращённой к крови, является наиболее надёжным и воспроизводимым способом индуцировать воспаление в кишечных органоидах, полученных от недоношенных детей. Эта усовершенствованная модель фиксирует не только вспышку воспаления, но и встроенные механизмы контроля, толерантности и восстановления у уязвимого недоношенного кишечника. Она даёт практическую схему для других лабораторий, чтобы изучать, как конкретные микробы, лекарства или нутриенты могут усугублять или смягчать кишечное воспаление у крайне недоношенных младенцев — важный шаг к более безопасным и целевым стратегиям предотвращения разрушительных кишечных заболеваний в этой уязвимой группе.
Цитирование: Chapman, J.A., Frey, A.M., Dueñas, M.E. et al. Optimising the induction of inflammation within preterm infant-derived intestinal epithelial organoids. npj Gut Liver 3, 5 (2026). https://doi.org/10.1038/s44355-026-00054-2
Ключевые слова: кишечник недоношенного ребёнка, кишечные органоиды, воспаление кишечника, микробиом, некротизирующий энтероколит