Clear Sky Science · ru
Неравновесная хемомеханическая трансдукция: АТФ‑приводимое распутывание белков в 26S протеасоме
Как крошечный механизм поддерживает порядок среди наших белков
Внутри каждой клетки микроразрушитель под названием 26S протеасома постоянно утилизирует повреждённые или больше не нужные белки, сохраняя клетку здоровой. В центре этого комплекса находится кольцеобразный мотор, который расходует химическое топливо (АТФ), чтобы захватывать, распутывать и втягивать белки в центральную камеру для разрезания. В этой статье с помощью продвинутых компьютерных симуляций показано, как мотор преобразует химическую энергию в механическое движение, предоставляя детализированную количественную картину процесса, лежащего в основе старения, заболеваний мозга, иммунитета и рака.
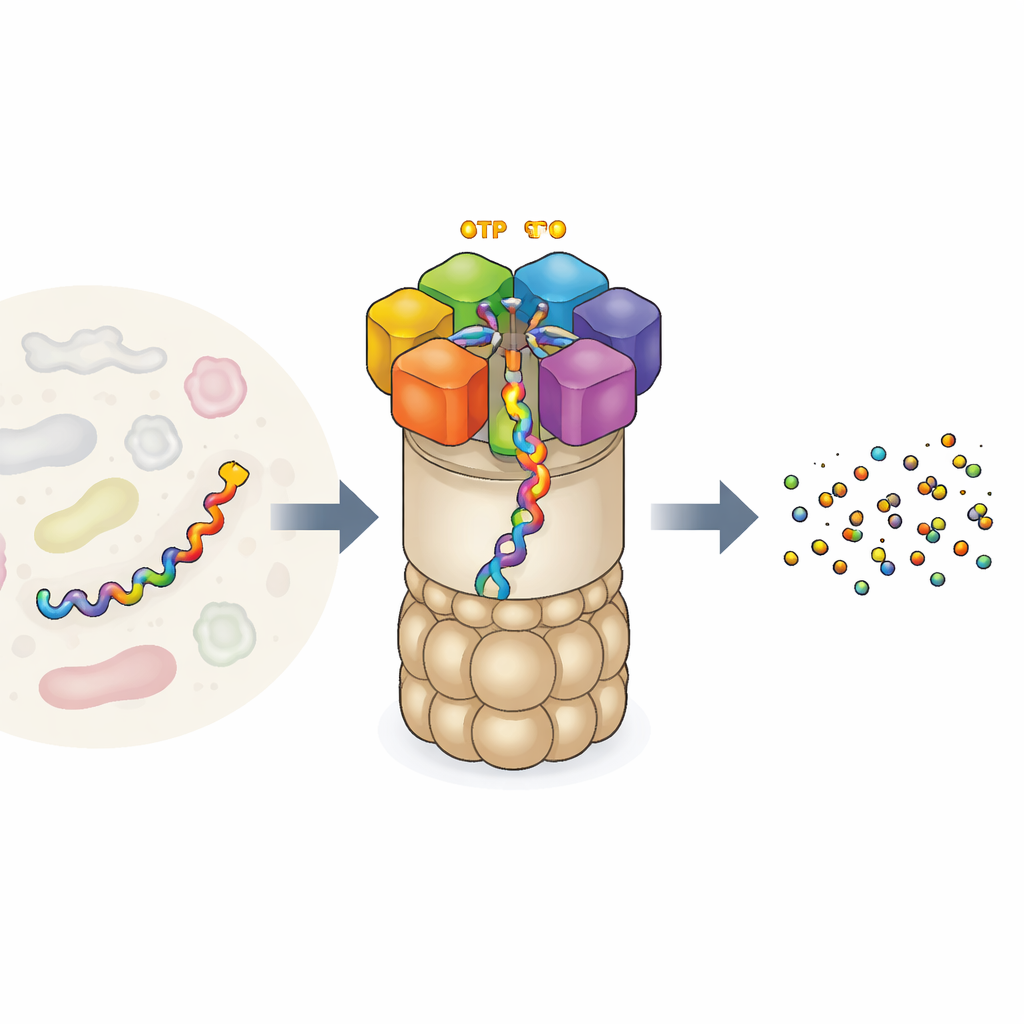
Завод по утилизации белков в клетке
26S протеасома — одна из крупнейших и самых сложных белковых машин в клетке. Она состоит из бочкообразного ядра, которое разрезает белки, и регуляторной крышки, что распознаёт, какие белки уничтожать. У входа расположен кольцевой ряд из шести разных моторных субъединиц. Каждая субъединица может связывать АТФ — универсальную энергетическую валюту клетки — и использовать эту энергию, чтобы захватить полипептидную цепь и втянуть её в ядро для разрушения. Этот мотор не действует хаотично: предыдущие эксперименты предполагали, что шесть субъединиц работают согласованно, в «передаче руки», передавая белок подобно альпинистам на верёвке. Но эксперименты давали лишь несколько снимков этого процесса, оставляя открытыми вопросы о полной последовательности движений и о том, как именно сжигание топлива связано с механической работой.
Моделирование молекулярной перетягивания каната
Авторы построили вероятностную компьютерную модель, которая рассматривает мотор как систему, перескакивающую между множеством возможных конфигураций, в то время как молекулы АТФ и её продуктов связываются и отсоединяются. Они определили 30 основных конформаций кольца, в которых одна, две или три моторные субъединицы теряют захват белка, а также особое плотно закрытое состояние, в котором все шесть удерживают цепочку. С помощью стандартного алгоритма для моделирования случайных химических событий они отслеживали сотни тысяч шагов, в которых происходили связывание АТФ, гидролиз АТФ и изменения формы мотора. Из этих прогонов они смогли предсказать, как быстро белок проталкивается при разных условиях, например при изменении концентраций АТФ, его потраченной формы АДФ и нерасщепляемого аналога АТФ, часто используемого в экспериментах.
Когда слишком много топлива замедляет мотор
Симуляции воспроизвели несколько загадочных экспериментальных наблюдений. С повышением уровней АТФ от низких значений мотор тянет белки быстрее, потому что связывание топлива является самым медленным шагом. Но выше примерно 1 миллимоля скорости достигают максимума и затем падают: кольцо проводит больше времени в застрявшей, не‑перемещающей состояние, в котором все шесть субъединиц заняты АТФ, но белок не продвигается. Добавление АДФ или нерасщепляемого аналога АТФ устойчиво замедляет мотор, потому что эти молекулы конкурируют с АТФ за посадочные карманы, но не могут завершить полный рабочий ход. Модель также предсказывает поведение мотора при встрече с очень туго свернутыми участками белка, которые выступают в роли препятствий. В таких случаях мотор тратит больше времени на борьбу с сопротивлением, и общая скорость деградации падает — это согласуется с измерениями на искусственно стабилизированных доменах белков.
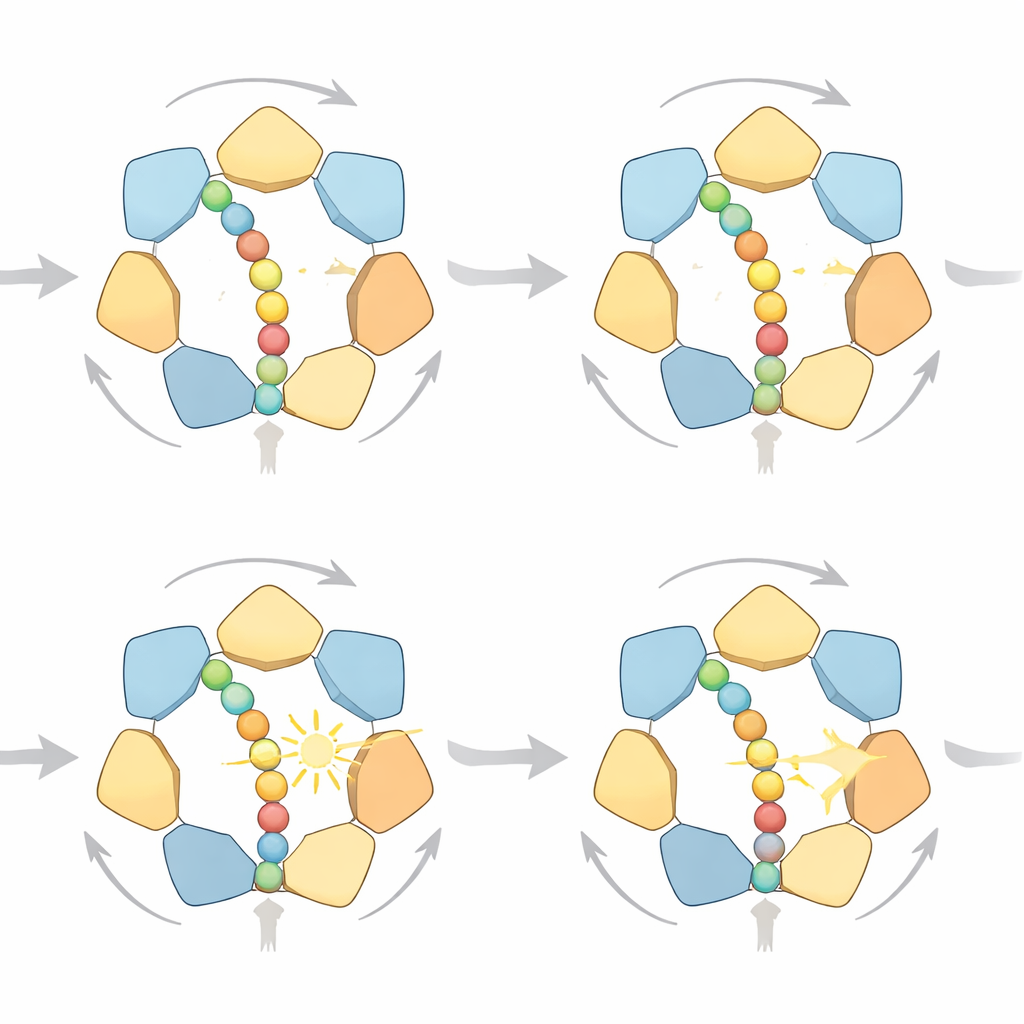
Многообразие шагов
Анализируя детально смоделированные траектории, исследователи обнаружили, что кольцо не следует единственному жёсткому циклу. Напротив, существуют несколько высоковероятных путей, которые все соблюдают одно и то же направленное правило «передачи руки»: субъединицы у выхода кольца отпускают белок после гидролиза АТФ, поднимаются на вершину спиральной лестницы субъединиц и снова захватывают цепочку выше по спирали. Иногда белок продвигается на один маленький шаг, иногда на два, в зависимости от того, сколько субъединиц отпускают одновременно. При обилии топлива доминируют одношаговые движения, потому что они тратят меньше работы против противодействующих сил; при дефиците топлива модель предсказывает более частые двухшаговые прыжки. Симуляции также связывают механическую нагрузку с химическим состоянием мотора: по мере увеличения сопротивления и торможения белка в большем числе из шести посадочных карманов накапливается АДФ — точно то, что наблюдают структуры высокого разрешения.
Использование энергии и общие принципы конструкции
Модель позволяет авторам отобразить, как энергия мотора возрастает при гидролизе АТФ и падает, когда эта энергия превращается в движение. Они рассчитывают кривую эффективности, показывающую, что мотор работает лучше всего при промежуточной встречной силе: при слишком небольшом сопротивлении он зря расходует АТФ; при слишком большом — почти останавливается. Сравнивая свои предсказания с данными о родственных машинах разрушения белков у бактерий и дрожжей, команда обнаружила очень похожие тренды в том, как нерасщепляемый аналог АТФ замедляет эти моторы. Это указывает на то, что многие члены одного семейства кольцевых ферментов, вероятно, разделяют общий, консервативный механизм натяжения белков.
Почему это важно для здоровья и болезней
Преобразовав разрозненные структурные снимки и биохимические измерения в единую проверяемую схему, эта работа в количественном виде показывает, как крошечный молекулярный мотор превращает химическое топливо в силу для утилизации клеточных белков. Модель не только объясняет широкий спектр существующих экспериментов, но и делает предсказания о том, как изменения уровней топлива, механической нагрузки или мутации мотора могут изменить скорость разрушения белков. Поскольку похожие машины функционируют во всех формах жизни и играют ключевую роль в состояниях от нейродегенерации до рака, понимание их внутренней работы на этом уровне может в конечном счёте помочь в разработке препаратов, которые настраивают, усиливают или селективно блокируют эти микроскопические разрушители.
Цитирование: Wu, D., Ouyang, Q., Wang, H. et al. Nonequilibrium chemomechanical transduction of ATP-driven protein unfolding in the 26S proteasome. npj Biol. Phys. Mech. 3, 4 (2026). https://doi.org/10.1038/s44341-026-00034-w
Ключевые слова: протеасома, мотор AAA+ АТФазы, деградация белков, молекулярные машины, хемомеханическая связь