Clear Sky Science · ru
Микроорган в микрофлюидном биосенсоре для непрерывного мониторинга уровня глюкозы in vivo
Почему это важно для людей с диабетом
Для людей с диабетом 1 типа современные системы «искусственной поджелудочной» по-прежнему требуют постоянного внимания — нужно отмечать приемы пищи, реагировать на сигналы тревоги и беспокоиться о ночных гипогликемиях. В этом исследовании рассматривается принципиально другой тип датчика глюкозы, который не опирается на один фермент или на математическую модель, а заимствует крошечный живой компонент самой системы регуляции сахара в организме: скопления панкреатических клеток, называемые островками. Позволяя этим мини-органам делать то, что эволюция оптимизировала для них, исследователи стремятся создать более умные и безопасные мониторы глюкозы, которые в перспективе смогут работать более автономно в фоновом режиме.
Крошечный орган как живой сенсор
Большинство современных биосенсоров обнаруживают вещества с помощью очищенных молекул или одноклеточных линий. Они реагируют на одно конкретное вещество и затем передают необработанный сигнал программному обеспечению, которое пытается его интерпретировать. Авторы утверждают, что такой подход игнорирует мощный встроенный «компьютер»: микроорганы, такие как панкреатические островки, которые естественным образом одновременно воспринимают множество сигналов и превращают их в скоординированный ответ. Каждый островок содержит несколько типов гормон-продуцирующих клеток, которые постоянно взаимодействуют друг с другом. Вместе они поддерживают уровень сахара в крови в узком, безопасном диапазоне, реагируя не только на глюкозу, но и на аминокислоты, гормоны кишечника и стресса, а также на недавнюю историю колебаний уровня сахара. По их мнению, эта встроенная сложность может быть использована для получения более богатой и надежной информации, чем от простого датчика на основе глюкозооксидазы.
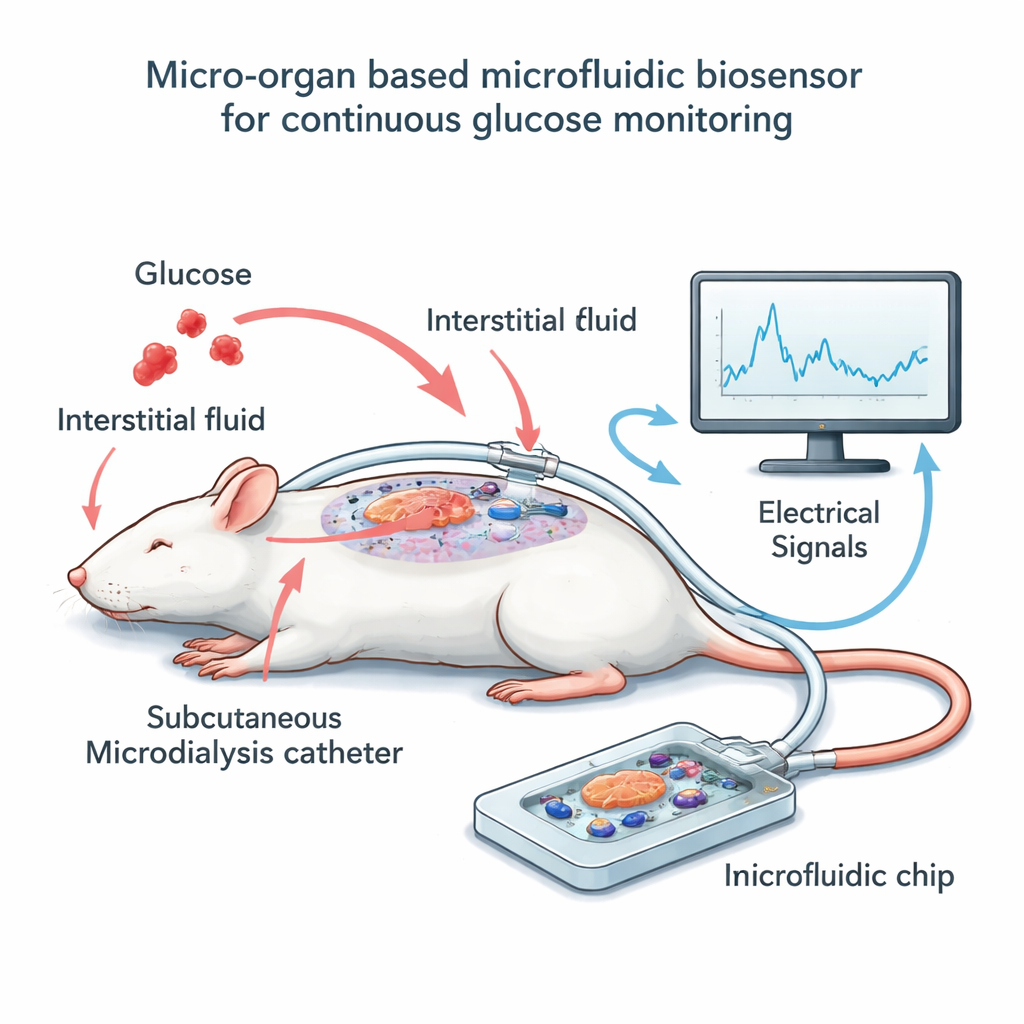
Создание системы «чип+катетер»
Чтобы проверить эту идею, команда собрала небольшое устройство вне тела, в котором размещены несколько десятков островков мыши поверх сетки микроскопических электродов. Вместо того чтобы напрямую погружать эти клетки в кровь, они использовали технику микродиализа: тонкий гибкий катетер располагается прямо под кожей анестезированных крыс и медленно отбирает окружающую тканевую жидкость, которая в целом повторяет изменения уровня сахара в крови, но с небольшим запаздыванием. Низкий постоянный поток прогоняет эту жидкость по узкому каналу над островками на чипе. По мере роста и падения концентрации глюкозы в диализате островки меняют свою электрическую активность, которую электроды регистрируют как медленные волнообразные сигналы. Параллельно исследователи периодически измеряли глюкозу в крови крыс и в диализате, что позволило сопоставить электрические показания с реальным уровнем сахара во времени.
Как живой сенсор реагировал на изменения сахара
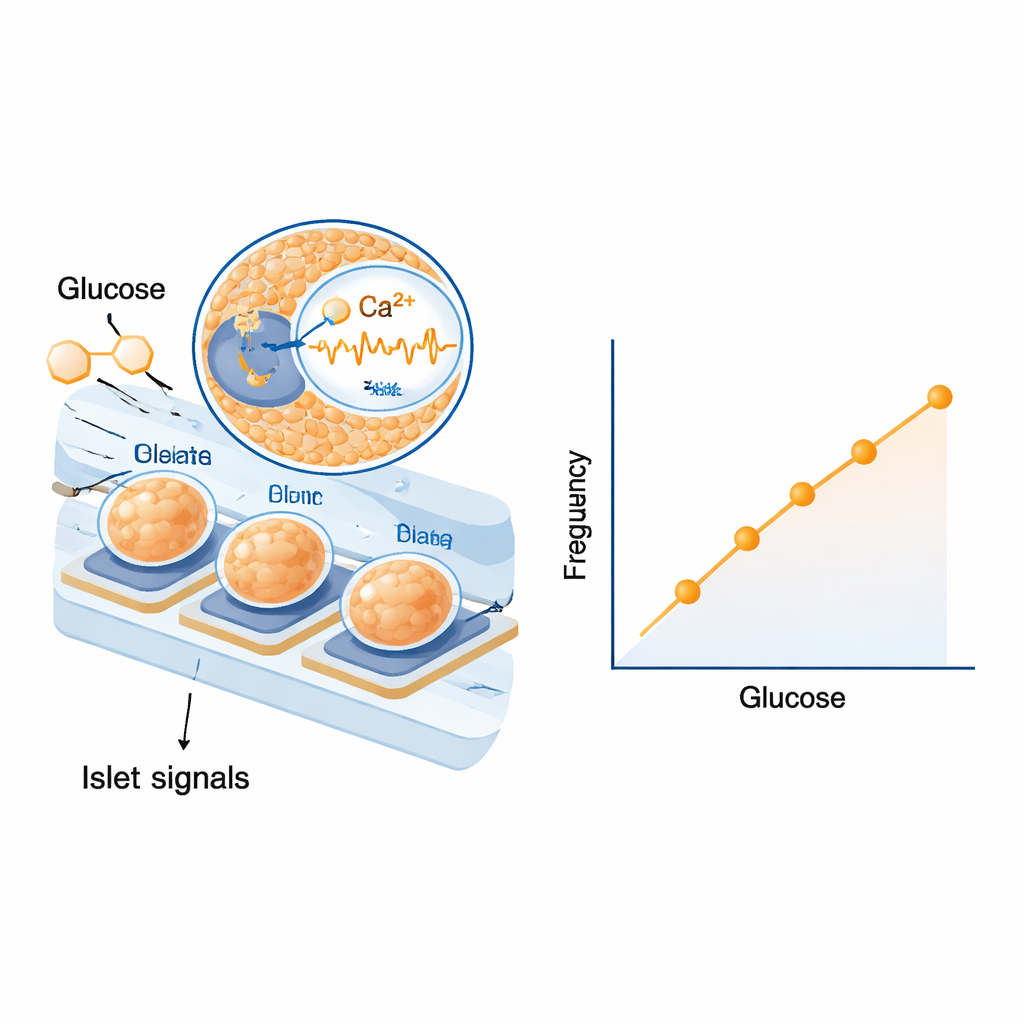
Сначала ученые проверили, могут ли островки на электродах реагировать на реальные компоненты крови, а не на простые лабораторные растворы. Их подвергали воздействию сыворотки человека и крыс с разными уровнями глюкозы и наблюдали отчетливые, градуированные изменения как в частоте, так и в размере их электрических волн. Ответы были достаточно сильными, чтобы различать небольшие ступени концентрации сахара в диапазоне, важном для диабета. Затем эксперименты перенесли на крыс: вводили инъекцию глюкозы, чтобы повысить уровень сахара, а позже вводили инсулин, чтобы его понизить. С учетом времени, необходимого для перехода глюкозы из крови в тканевую жидкость и через трубки, они обнаружили, что частота медленных электрических сигналов островков поднимается и опускается почти синхронно с уровнем сахара в крови. Статистический анализ по нескольким животным показал удивительно плотную и воспроизводимую зависимость между частотой сигналов и уровнем глюкозы, тогда как амплитуда сигналов, хоть и информативна, оказывалась несколько более вариабельной.
Встроенные биологические механизмы безопасности
Важным преимуществом использования целых островков, а не одной молекулы, является то, что их поведение уже включает механизмы безопасности, сформированные эволюцией. Ранние работы и намеки из этого исследования показывают, что островки сильнее реагируют при падении глюкозы, чем при ее повышении — форма «гистерезиса», которая помогает защититься от опасной гипогликемии. Электрические паттерны также формируются соседними типами клеток, которые могут усиливать или ослаблять выделение инсулина в зависимости от потребностей организма. Поскольку чип просто «слушает» эти интегрированные сигналы без добавления красителей или генетических модификаций, он может записывать данные в течение дней, не повреждая клетки. Авторы отмечают технические задачи впереди, такие как избегание воздушных пузырей, обеспечение долговременной работы микродиализа и выбор типа человеческих или стволовых островков, которые в конечном счете следует использовать. Тем не менее компьютерные имитации с использованием хорошо зарекомендовавшей себя модели диабета предполагают, что такой сенсор на базе островков может сравняться или даже превзойти современные мониторы глюкозы в сложных условиях.
Что это может означать для будущего ухода при диабете
Эта работа демонстрирует, что несколько панкреатических микроорганов, живущих на небольшом чипе и соединенных с телом тонким катетером, могут непрерывно отслеживать уровень сахара в крови у живых животных по своей естественной электрической «переписке». Для неспециалиста ключевая мысль в том, что вместо того чтобы просить простой химический датчик измерить глюкозу и затем заставлять компьютер догадываться, что это значит для организма, этот подход напрямую слушает тот же тип живой ткани, который обычно решает, сколько инсулина выделить. Если его доработать и сделать практичным для людей, такие живые биосенсоры могли бы стать ядром по-настоящему автономных систем искусственной поджелудочной — устройств, которые незаметно предугадывают потребности организма и снижают ежедневную нагрузку при управлении диабетом.
Цитирование: Puginier, E., Pirog, A., de Gannes, F.P. et al. A micro-organ based microfluidic biosensor for continuous monitoring of glucose levels in vivo. npj Biosensing 3, 12 (2026). https://doi.org/10.1038/s44328-025-00077-4
Ключевые слова: непрерывный мониторинг глюкозы, искусственная поджелудочная, панкреатические островки, микрофлюидный биосенсор, диабет 1 типа